
デカメチルシリコセン((C 5 Me 5 ) 2 Si)は、第14族の サンドイッチ化合物である。主族 シクロペンタジエニル錯体の一例であり、メタロセンと関連しているが、中心原子としてpブロック元素を含む。無色で空気に敏感な固体であり、真空下で昇華する。[1]
合成
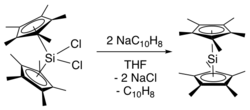
デカメチルシリコセンの最初の合成は、1986年にユッツィらによって報告された[2]。この合成法では、ビス(ペンタメチルシクロペンタジエニル)シリコン(IV)ジクロリドを2当量のナフタレン化ナトリウムで還元し、デカメチルシリコセン、ナフタレン、塩化ナトリウムを生成した。立体的に密集したビス(ペンタメチルシクロペンタジエニル)シリコン(IV)ジクロリドの生成には、tert-ブチルリチウムを用いた(C 5 Me 4 H) 2 SiCl 2の二重脱プロトン化から始まり、得られた(C 5 Me 4 Li) 2 SiCl 2 をヨウ化メチルで処理するという複数の段階を踏む必要があった[3] 。
デカメチルシリコセンは、ヘキサン、ベンゼン、塩素化溶媒などの非プロトン性溶媒に可溶です。分子量測定の結果、デカメチルシリコセンはベンゼン中でモノマーとして存在することがわかりました。1 H NMRスペクトルでは1つの鋭いシグナルが示され、13 C-{ 1 H}スペクトルでは環炭素とメチル基炭素の2つのシグナルが示され、溶液中での5回対称構造とペンタメチルシクロペンタジエニル基のη 5配位が提案されていることと整合しています。[2]
最近の合成法では、N-ヘテロ環カルベン安定化シリレンから塩メタセシスによってデカメチルシリコセンを直接生成する。[4]この合成経路では、出発物質であるビス(ペンタメチルシクロペンタジエニル)シリコン(IV)ジクロリドの合成を回避できる。この合成法では、NHC安定化シリレン(NHC=C[N-(C 6 H 3 –2,6- iPr 2 )CH] 2)をペンタメチルシクロペンタジエンのカリウム塩で-30 °C (-22 °F) で処理し、続いてデカメチルシリコセンを-60 °C (-76 °F) でヘキサンに抽出してNHCとKCl副生成物を除去した。

構造と結合
デカメチルシリコセンのX線結晶構造解析によって決定された構造には、2つの異性体が2:1の比率で含まれています。[ 2 ] [1]主異性体は、曲がったメタロセンを思わせるC s構造を採用しており、シクロペンタジエニル面が約25°の角度を形成し、メチル基が互い違いに配置されています。この異性体では、シリコン上の孤立電子対は立体化学的に活性であると説明され、シリコン原子から各Cp*重心までの距離は2.12Åです。マイナー異性体は、デカメチルフェロセン と同じD 5d構造を採用しており、シクロペンタジエニル環が互いに平行で、メチル基が互い違いに配置されています。シリコン原子から各Cp*重心までの距離は2.11Åです。2つの異性体が存在するのは、パッキング効果によるものと考えられています。[2]
親シリコセン (C 5 H 5 ) 2 Si に対して行われた計算研究により、分子を D 5d形状から C 2v (曲がった、水素原子が重なった) または C s (曲がった、水素原子がずらされた) 形状に歪ませると、非常に小さな (~4 kJ/mol) エネルギー変化が起こることが明らかになりました。[5]定性的な分子軌道図は、 HOMOがシリコン (3s)-シクロペンタジエニル反結合特性を持ち、LUMO がシリコン (3p)-シクロペンタジエニル反結合特性を持つことを予測しています。[5] NBO 計算は定性的な分子軌道図からの予測と一致しており、HOMO と LUMO の両方でシリコンとシクロペンタジエニル配位子の間に反結合特性を示しています。計算されたNBO価電子軌道占有数は、シクロペンタジエニル配位子とシリコン3s、3px、3py軌道の間に有意な結合が生じることを示唆している。[5]
比較すると、カルボセンの同族体であるシリコンは、2p軌道に比べて3p軌道の半径方向の広がりが大きいため、シクロペンタジエニル配位子とより強く結合すると計算されている。さらに、3s軌道と3p軌道のエネルギー的分離は2s軌道と2p軌道のエネルギー的分離よりも大きいため、スピン共鳴が少なくなり、各シクロペンタジエニル配位子がシリコン原子にη 1で結合するシリレン構造への変形の好ましさが低下する。 [5] 分子内原子(AIM)計算はこの見解と整合している。中心のシリコン原子と1つのシクロペンタジエニル炭素間の電子密度のラプラシアンプロットは、カルボセンの同等の計算と比較して、中心原子への電荷の局在が少ないことを示している。[5]
反応性
デカメチルシリコセンはアルデヒドやケトンと反応し、ケイ素(IV)中心原子と、アルデヒドまたはケトンの2当量間で形成された炭素-炭素結合を有する生成物を与える。得られた2つのアルコキシドはケイ素原子に配位し、五員環を形成する。[6]これらの反応の過程で、 シクロペンタジエニル環の配位はη 5からη 1へと変化する。
デカメチルシリコセンが炭素-窒素三重結合と反応すると、ペンタメチルシクロペンタジエンチル環のハプティシティに同様の変化が生じる。有機シアネートやチオシアネートと反応すると、炭素-炭素結合が形成され、結果として生じる有機フラグメントは2つのアニオン性窒素を介してケイ素原子に配位する。[7]デカメチルシリコセンは、BrCNや(Me
3Si)CN を酸化付加して、Br または Me 3 Si 配位子とともにシアン化物配位子を持つシリコン (IV) 生成物を形成する。
デカメチルシリコセンは[HOEt
2][紀元前
6F
5)
4]。プロトン化により、1当量のペンタメチルシクロペンタジエンが脱離し、 [B(C
6F
5)
4]−
. [4]
ペンタメチルシクロペンタジエニルシリコン(II)カチオンは、様々なシクロペンタジエニル塩と反応して置換シリコセンを生成する。この方法で合成されたシリコセン誘導体には、 (Me 5 C 5 )((i-Pr) 5 C 5 ) Si 、((Me 5 C 5 ) (1,3,4-Me 3 H 2 C 5 )Si、(Me 5 C 5 )(H 5 C 5 )Siなどがある。[8]後者は-50℃(-58°F)で安定だが、-30℃(-22°F)で分解し始める。さらに、ペンタメチルシクロペンタジエニルシリコン(II)カチオンは金属前駆体と反応して、金属-シリコン多重結合を持つ錯体を生成することができる。[4]
参考文献
- ^ ab Jutzi、ピーター;ホルトマン、ウド。カンネ、ディーター。クルーガー、カール。ブロム、リチャード。グライター、ロルフ。ハイラ=クリスピン、イザベラ(1989-09-01)。 「デカメチルシリコセン — 最初の安定なケイ素(II)化合物: 合成、構造、結合」。ケミッシェ ベリヒテ。122 (9): 1629 ~ 1639 年。土井:10.1002/cber.19891220906。ISSN 1099-0682。
- ^ abcd ジュッツィ、ピーター;カンネ、ディーター。クルーガー、カール (1986-02-01)。 「デカメチルシリコセン - 合成と構造」。英語版のAngewandte Chemie国際版。25 (2): 164.土井:10.1002/anie.198601641。ISSN 1521-3773。
- ^ ピーター・ジュッツィ;カンネ、ディーター。ハーストハウス、マイク。ハウズ、アンドリュー J. (1988-07-01)。 「モノとビス(η1-ペンタメチルシクロペンタジエニル)シラン – 合成、構造と固有シャフト」。ケミッシェ ベリヒテ。121 (7): 1299–1305。土井:10.1002/cber.19881210714。ISSN 1099-0682。
- ^ abc Ghana, Priyabrata; Arz, Marius I.; Schnakenburg, Gregor; Straßmann, Martin; Filippou, Alexander C. (2017-10-19). 「金属–シリコン三重結合:SiX2(NHC)から[Si(η5-C5Me5)]+へのアクセスとシリリジン錯体[TpMe(CO)2MoSi(η3-C5Me5)](TpMe = κ3-N,N′,N"-ヒドリドトリス(3,5-ジメチル-1-ピラゾリル)ボレート)への変換」. Organometallics . 37 (5): 772– 780. doi :10.1021/acs.organomet.7b00665. ISSN 0276-7333.
- ^ abcde Schoeller, Wolfgang W.; Friedrich, Oliver; Sundermann, Andreas; Rozhenko, Alexander (1999-05-01). 「カルボセン (C5R5)2C とシリコセン (C5R5)2Si (R = H, Me) の幾何学的および電子的構造」. Organometallics . 18 (11): 2099– 2106. doi :10.1021/om980737l. ISSN 0276-7333.
- ^ ピーター・ジュッツィ;アイケンバーグ、ディルク。ブンテ、エルンスト=アウグスト。メールケ、アンドレアス。ノイマン、ベアテ。シュタムラー、ハンス・ゲオルク (1996-04-02)。 「デカメチルシリコセンの化学: 代表的なアルデヒドおよびケトンとの反応」。有機金属。15 (7): 1930 ~ 1934 年。土井:10.1021/om950897m。ISSN 0276-7333。
- ^ Jutzi, Peter; Eikenberg, Dirk; Neumann, Beate; Stammler, Hans-Georg (1996-08-20). 「デカメチルシリコセンの化学:炭素−窒素三重結合種との反応」. Organometallics . 15 (17): 3659– 3663. doi :10.1021/om960338v. ISSN 0276-7333.
- ^ Jutzi, Peter (2014-07-21). 「ペンタメチルシクロペンタジエニルシリコン(II)カチオン:合成、特性評価、および反応性」. Chemistry – A European Journal . 20 (30): 9192– 9207. doi :10.1002/chem.201402163. ISSN 1521-3765. PMID 24986115.