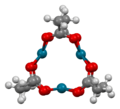
酢酸パラジウム(II)
 | |||
2.jpg/440px-Pd(OAc)2.jpg) | |||
| |||
| 名前 | |||
|---|---|---|---|
| IUPAC名 酢酸パラジウム(II) | |||
| その他の名前 パラジウムジアセテートヘキサキス(アセタト)トリパラジウムビス(アセタト)パラジウム | |||
| 識別子 | |||
| |||
3Dモデル(JSmol) |
| ||
| ケムスパイダー |
| ||
| ECHA 情報カード | 100.020.151 | ||
| EC番号 |
| ||
PubChem CID | |||
| RTECS番号 |
| ||
| ユニイ |
| ||
CompToxダッシュボード(EPA) | |||
| |||
| |||
| プロパティ | |||
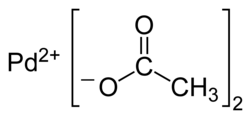
| パラジウム(CH 3 COO) 2 | |||
| モル質量 | 224.51 g/モル | ||
| 外観 | 茶色の黄色の固体 | ||
| 密度 | 2.19 g/cm 3 | ||
| 融点 | 205℃(401°F; 478 K)で分解する | ||
| 低い | |||
| 構造 | |||
| 単斜晶系 | |||
| 正方形平面 | |||
| 0日 | |||
| 危険 | |||
| 労働安全衛生(OHS/OSH): | |||
主な危険 | 非危険物とみなされる | ||
| GHSラベル: [ 1 ] | |||
   | |||
| 危険 | |||
| H317、H318、H410 | |||
| P261、P272、P273、P280、P302+P352、P305+P351+P338 | |||
| 安全データシート(SDS) | [1] | ||
| 関連化合物 | |||
その他の陰イオン | 塩化パラジウム(II) | ||
その他の陽イオン | 酢酸白金(II) | ||
特に記載がない限り、データは標準状態(25 °C [77 °F]、100 kPa)における材料のものです。 | |||
酢酸パラジウム(II)は、化学式[Pd(O 2 CCH 3 ) 2 ] n(略称[Pd(OAc) 2 ] n)で表されるパラジウムの化合物です。類似の白金化合物よりも反応性が高く、nの値に応じて多くの有機溶媒に溶解するため、有機反応の触媒として広く用いられています。[ 2 ]
構造
パラジウム原子と酢酸配位子の化学量論比が1:2の化合物は、分子状および高分子状で存在し、固体および溶液状態では三量体状が優勢です。Pdはどちらの形態でもほぼ平面正方配位を形成します。
1965年にジェフリー・ウィルキンソンらによって合成され、後に1970年にスカプスキーとスマートによって単結晶X線回折によって特徴付けられた酢酸パラジウム(II)は、赤褐色の固体で、単斜晶板として結晶化する。パラジウム原子の正三角形からなる三量体構造を有し、各原子対は2つの酢酸基によって蝶型に架橋されている。[ 3 ] [ 4 ]
酢酸パラジウム(II)は淡いピンク色の形でも調製できる。粉末X線回折によると、この形はポリマー状である。[ 5 ]
準備
三量体状の酢酸パラジウムは、パラジウムスポンジを酢酸と硝酸の混合液で処理することによって調製できる。混合硝酸酢酸(Pd 3 (OAc) 5 NO 2 )による汚染を防ぐため、過剰量のパラジウムスポンジ金属または窒素ガス流が必要となる。[ 6 ] [ 7 ]
- Pd + 4 HNO 3 → Pd(NO 3 ) 2 + 2 NO 2 + 2 H 2 O
- Pd(NO 3 ) 2 + 2 CH 3 COOH → Pd(O 2 CCH 3 ) 2 + 2 HNO 3
三量体酢酸塩と比較して、硝酸塩・酢酸塩混合体は溶解度と触媒活性が異なります。この不純物の混入を防ぐ、あるいはその量を制御することは、酢酸パラジウム(II)の信頼性のある使用において重要な要素となります。[ 8 ]
プロピオン酸パラジウム(II)も同様に合成されます。他のカルボン酸塩は、酢酸パラジウム(II)を適切なカルボン酸で処理することで合成されます。[ 3 ]同様に、酢酸パラジウム(II)は他のカルボン酸パラジウム(II)を酢酸で処理することでも合成できます。精製された他のカルボン酸塩を出発物質とするこの配位子交換反応は、ニトロ基の混入のない酢酸パラジウム(II)を合成する代替方法でもあります。[ 8 ]
酢酸パラジウム(II)は、第一級アルコール、第二級アルコール、アミンなど、β水素化脱離反応を起こす試薬の存在下では、Pd(0)に還元されやすい。アルコール類で加熱したり、他の溶媒で長時間煮沸したりすると、酢酸パラジウム(II)はパラジウムに分解する。 [ 3 ]
触媒
酢酸パラジウムは多くの有機反応、特にアルケン、ジエン、アルキル、アリール、ビニルハロゲン化物との反応性付加物を形成する触媒である。[ 9 ]
酢酸パラジウム(II)触媒反応:
- ビニル化:例としてはヘック反応と関連プロセスが挙げられる。[ 10 ]
- 非環式ジエンの転位:例としてはコープ転位が挙げられる。
- カルボニル化反応:例えば、アリールヨウ化物、一酸化炭素、アルコールまたはフェノールからのエステルの形成。[ 11 ]
- ギ酸カリウムによるアルデヒドまたはケトンの還元アミノ化。[ 12 ]
- ワッカー法:エチレンを水で酸化してアセトアルデヒド(ポリ酢酸ビニルの前駆体)を生成する。
- アルキルおよびアリールアミンによるアリールハライド/擬似ハライドのブッフヴァルト・ハートウィッグアミノ化。 [ 13 ] [ 14 ]
- 臭化アリールを殺菌剤「ラティチュード」を含む多くの有機化合物の官能基であるトリメチルシランに変換します。
- RC 6 H 4 Br + Si 2 (CH 3 ) 6 → RC 6 H 4 Si(CH 3 ) 3 + Si(CH 3 ) 3 Br
Pd(O2CCH3 ) 2は臭化アリールの電子的性質と適合しており、他の合成方法とは異なり、この方法では高圧装置を必要としません。[ 15 ]
他のPd化合物の前駆体
酢酸パラジウムは他のパラジウム(II)化合物の製造に用いられる。例えば、アリルアルコールをアルデヒドに異性化するのに用いられる酢酸フェニルパラジウムは、以下の反応によって製造される。[ 16 ]
- Hg(C 6 H 5 )(OAc) + Pd(OAc) 2 → Pd(C 6 H 5 )(OAc) + Hg(OAc) 2
酢酸パラジウム(II)はアセチルアセトン(「acac」配位子)と反応してPd(acac) 2を生成します。
ヘルマン触媒は酢酸パラジウム(II)とトリス( o-トリル)ホスフィンとの反応によって作られる。[ 17 ]
光や熱によって酢酸パラジウムが還元され、パラジウムの薄い層が形成され、ナノワイヤやコロイドが生成されます。[ 6 ]
参照
参考文献
- ^ "520764 [Pd(OAc)2]3" . Sigma-Aldrich . 2021年12月23日閲覧。
- ^グレンバーグ, ヘレナ; フット, ジョナサン S.; バンウェル, マーティン G.; ローマン, ダニエラ・サスタック (2001). 「酢酸パラジウム(II)」.有機合成試薬百科事典. pp. 1– 35. doi : 10.1002/047084289X.rp001.pub3 . ISBN 978-0-470-84289-8。
- ^ a b c T. A. Stephenson; SM Morehouse; AR Powell; JP Heffer; G. Wilkinson (1965). 「667. パラジウム、白金、ロジウムのカルボキシレート、およびそれらの付加物」Journal of the Chemical Society(再開版) : 3632. doi : 10.1039/jr9650003632 .
- ^ Skapski, A C.; ML Smart (1970). 「三量体パラジウム(II)酢酸塩の結晶構造」. J. Chem. Soc. D (11): 658b–659. doi : 10.1039/C2970000658b .
- ^キリク、サウスダコタ州;ムラガレフ、SF;ブロヒン、AI (2004)。 「粉末X線回折データからの[Pd(CH 3 COO) 2 ] n 」。アクタクリスタログル。 C. 60 (9): m449 – m450。土井:10.1107/S0108270104016129。PMID 15345831。
- ^ a b Bakhmutov, VI; Berry, JF; Cotton, FA; Ibragimov, S.; Murillo, CA (2005). 「酢酸パラジウム(II)の非自明な挙動」. Dalton Transactions (11): 1989– 1992. doi : 10.1039/b502122g . PMID 15909048 .
- ^ 「高純度均質触媒」(PDF)エンゲルハード2005年9月オリジナル(PDF)より2006年3月17日時点のアーカイブ。 2006年2月24日閲覧。
- ^ a b Ritter, Stephen K. (2016年5月2日). 「化学者が酢酸パラジウムのユーザーガイドを発表」. Chemical & Engineering News . 94 (18): 20–21 . doi : 10.1021/cen-09418-scitech1 .
- ^ Suggs, J W.「パラジウム:有機金属化学」無機化学百科事典、R.B. King編、全8巻、チチェスター:Wiley、1994年。
- ^ Keary M. Engle; Navid Dastbaravardeh; Peter S. Thuy-Boun; Dong-Hui Wang; Aaron C. Sather; Jin-Quan Yu (2015). 「リガンド加速によるフェニル酢酸のオルト-CHオレフィン化」 . Org. Synth . 92 : 58–75 . doi : 10.15227/ orgsyn.092.0058 . PMC 4936495. PMID 27397943 .
- ^ Nikitin, Kirill V.; Andryukhova, NP; Bumagin, NA; Beletskaya, IP (1991). 「Pd触媒によるアリールヨウ化物のカルボニル化によるアリールエステルの合成」. Mendeleev Communications . 1 (4): 129– 131. doi : 10.1070/MC1991v001n04ABEH000080 .
- ^ Basu, B., Satadru J., Mosharef HB, Pralay D. (2003). 「ギ酸カリウムと触媒酢酸パラジウムを用いたアルデヒドおよびケトンの直接還元アミノ化のための簡便なプロトコル」. ChemInform . 34 (30): 555– 557. doi : 10.1002/chin.200330069 .
{{cite journal}}: CS1 maint: 複数の名前: 著者リスト (リンク) - ^ Linli He; Shawn P. Allwein; Benjamin J. Dugan; Kyle W. Knouse; Gregory R. Ott; Craig A. Zificsak (2016). 「α-カルボリンの合成」 . Org. Synth . 93 : 272. doi : 10.15227/orgsyn.093.0272 .
- ^ 「ブッフバルト・ハートウィッグクロスカップリング反応」有機化学ポータル。
- ^ Gooben, L J. 「研究分野「新しいPd触媒クロスカップリング反応」」 2006年2月28日 < http://www.mpi-muelheim.mpg.de/kofo/bericht2002/pdf/2.1.8_gossen.pdf >2007年7月12日アーカイブ、 Wayback Machine
- ^リチャード・F・ヘック. 「アリルアルコールとフェニルパラジウム酢酸塩からのアルデヒド:2-メチル-3-フェニルプロピオンアルデヒド」 .有機合成;集成第6巻、815ページ。
- ^ Herrmann, WA; Brossmer, C.; Reisinger, C.-P.; Riermeier, TH; Öfele, K.; Beller, M. (1997). 「パラダサイクル:アリールハライドのヘックビニル化のための効率的な新触媒」. Chemistry – A European Journal . 3 : 1357– 1364. doi : 10.1002/chem.19970030823 .
- ^ Herrmann, WA; Brossmer, C.; Reisinger, C.-P.; Riermeier, TH; Öfele, K.; Beller, M. (1997). 「パラダサイクル:アリールハライドのヘックビニル化のための効率的な新触媒」. Chemistry – A European Journal . 3 (8): 1357– 1364. doi : 10.1002/chem.19970030823 .