 | |
| 臨床データ | |
|---|---|
| 商号 | ブフェニル、フェブラン、アモナプス、その他 |
| AHFS / Drugs.com | Micromedex 詳細な消費者情報 |
| ライセンスデータ |
|
| 妊娠 カテゴリー |
|
投与経路 | 経口摂取 |
| ATCコード |
|
| 法的地位 | |
| 法的地位 | |
| 薬物動態データ | |
| 代謝 | 肝臓と腎臓からフェニル酢酸 |
| 消失半減期 | 0.8時間(フェニル酪酸)、1.15~1.29時間(フェニル酢酸) |
| 排泄 | 尿(フェニルアセチルグルタミンとして80~100%) |
| 識別子 | |
| |
| CAS番号 | |
| PubChem CID |
|
| ドラッグバンク | |
| ケムスパイダー | |
| ユニイ |
|
| ケッグ |
|
| チェビ | |
| チェムブル | |
| CompToxダッシュボード (EPA) |
|
| ECHA 情報カード | 100.130.318 |
| 化学および物理データ | |
| 式 | C 10 H 11 Na O 2 |
| モル質量 | 186.186 g·mol −1 |
| 3Dモデル(JSmol) |
|
| |
 北 北 はい (これは何ですか?)(確認) はい (これは何ですか?)(確認) | |
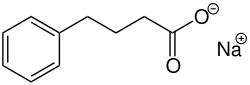
フェニル酪酸ナトリウムは、ブフェニルなどのブランド名で販売されており、芳香族脂肪酸である4-フェニル酪酸(4-PBA)または4-フェニル酪酸の塩です。[7]この化合物は、その代謝物が尿素回路の代替経路となり、過剰な窒素を排泄することから、尿素回路障害の治療に使用されます。[8] [9]
フェニル酪酸ナトリウムはヒストン脱アセチル化酵素阻害剤と化学シャペロンでもあり、それぞれ抗癌剤として、嚢胞性線維症などのタンパク質ミスフォールディング疾患への応用研究につながっています。[7]
構造と特性
フェニル酪酸ナトリウムは、芳香環と酪酸からなる芳香族脂肪酸のナトリウム塩です。フェニル酪酸ナトリウムの化学名は4-フェニル酪酸ナトリウム塩です。水溶性のオフホワイトの結晶を形成します。[4]
用途
医療用途
フェニル酪酸ナトリウムは、錠剤または粉末として経口または経鼻胃管で摂取され、非常に塩辛く苦い味がする。尿素サイクル異常症の治療薬である。尿素サイクル異常症とは、カルバモイルリン酸合成酵素I、オルニチントランスカルバミラーゼ、またはアルギニノコハク酸合成酵素の欠損により、窒素老廃物がアンモニアグルタミンとして血漿中に蓄積する(高アンモニア血症と呼ばれる状態)遺伝性疾患である。[8] [4]制御されない場合、これは知的障害および早期死亡を引き起こす。[4]フェニル酪酸ナトリウムの代謝物により、腎臓は尿素の代わりに過剰な窒素を排泄するようになり、透析、アミノ酸サプリメント、タンパク質制限食と組み合わせることで、尿素サイクル異常症を持って生まれた子供は通常12か月以上生存できる。[4]患者は生涯にわたって治療が必要になる場合がある。[4]この治療法は1990年代に研究者によって導入され、1996年4月に米国食品医薬品局(FDA)によって承認されました。[10] [11]
副作用
女性の約4分の1は、無月経または月経機能障害の副作用を経験する可能性があります。 [4]食欲不振は患者の4%に認められます。フェニル酪酸の代謝による体臭は患者の3%に認められ、不快な味覚は3%に認められます。消化器症状と、主に軽度の神経毒性の兆候は患者の2%未満に認められ、その他にもいくつかの副作用が報告されています。[4]フェニル酪酸ナトリウム治療は、フェニルアラニンの産生により母体のフェニルケトン尿症に類似する症状を呈し、胎児の脳損傷を引き起こす可能性があるため、妊娠中の投与は推奨されません。[8]
研究
尿素サイクル異常症
1980年代初頭、ジョンズホプキンス大学医学部のソール・ブルシロウ博士、マーク・バットショウ氏らは、いくつかの思いがけない発見により、フェニル酪酸ナトリウムの投与が別の窒素処理経路につながることを発見した。彼らは1970年代後半に別の先天性代謝異常症であるシトルリン血症に対するケト酸療法を研究しており、アルギニン投与により尿中窒素が増加し、血中アンモニアが減少することに気付いた。研究者らがこの発見についてノーマン・ラディン氏に相談したところ、ラディン氏は尿素排泄を減らすために安息香酸ナトリウムを使用するという1914年の論文を思い出した。1919年の別の論文ではフェニル酢酸ナトリウムが使用されていたため、研究者らは5人の高アンモニア血症患者を安息香酸とフェニル酢酸で治療し、 Science誌に論文を発表した。[8] [12] 1982年と1984年に研究者らは尿素サイクル異常症に対する安息香酸とアルギニンの使用についてNEJM誌に発表した。[8] [13] [14]フェニル酪酸ナトリウムはフェニル酢酸の臭いがないため、1990年代初頭に使用が開始された。[8] [15] [16]
化学シャペロン
嚢胞性線維症では、嚢胞性線維症膜コンダクタンス制御因子タンパク質ΔF508-CFTRの点変異により、CFTRが不安定化し、ミスフォールド状態になるため、小胞体に捕捉され、細胞膜に到達できなくなります。細胞膜におけるCFTRの欠損は、塩素イオン輸送の阻害と嚢胞性線維症の症状の発現につながります。フェニル酪酸ナトリウムは化学シャペロンとして作用し、小胞体内の変異CFTRを安定化させ、細胞表面への到達を可能にします。[17]
ヒストン脱アセチル化酵素阻害剤
ヒストン脱アセチル化酵素阻害剤としての活性から、フェニル酪酸ナトリウムは悪性神経膠腫および急性骨髄性白血病の分化誘導剤としての可能性について研究されている。[7]また、胎児ヘモグロビンの発現を誘導して欠損した成人ヘモグロビンを補充することから、一部の鎌状赤血球疾患の治療においてヒドロキシカルバミドの代替としての可能性についても研究されている。 [18] [19]小規模な研究が進行中であるが、現在までにこの化合物の癌の臨床治療への使用を裏付けるデータは公表されておらず、限定的な研究段階にとどまっている。フェニル酪酸ナトリウムは、ハンチントン病の治療選択肢としても研究されている。[20]
他の
フェニル酪酸はショウジョウバエの寿命を延ばすことと関連している。[21]
コロラド大学の研究者、カート・フリード氏とウェンボ・ゾウ氏は、フェニル酪酸がマウスのパーキンソン病の進行を阻害することを実証しました。このDJ-1遺伝子は中脳のドーパミン作動性ニューロンの死滅を防ぐ働きがあります。2011年7月現在、彼らはフェニル酪酸をヒトのパーキンソン病治療薬として試験する予定です。[22][アップデート]
薬理学

フェニル酪酸はプロドラッグです。人体内でまずフェニルブチリルCoAに変換され、その後、主に肝臓と腎臓でミトコンドリアβ酸化によって活性型フェニル酢酸へと代謝されます。[23]フェニル酢酸はグルタミンと抱合してフェニルアセチルグルタミンとなり、尿とともに排泄されます。フェニル酢酸は尿素と同量の窒素を含むため、尿素の窒素排泄代替物として用いられます。[4]
経口摂取されたフェニル酪酸ナトリウムは、15分以内に血中に検出され、1時間以内に血中濃度の最高値に達します。30分以内にフェニル酢酸に代謝されます。[4]
参考文献
- ^ 「処方薬:オーストラリアにおける新規化学物質の登録、2017年」医薬品行政庁(TGA) 2022年6月21日. 2023年4月9日閲覧。
- ^ 「処方薬と生物学的製剤:TGA年次概要2017」医薬品・医療品管理局(TGA) 2022年6月21日. 2024年3月31日閲覧。
- ^ 「カナダ保健省の新薬認可:2015年のハイライト」カナダ保健省、2016年5月4日。 2024年4月7日閲覧。
- ^ abcdefghij 「ブフェニル- フェニル酪酸ナトリウム錠 ブフェニル- フェニル酪酸ナトリウム粉末」DailyMed . 2020年3月11日. 2020年10月19日閲覧。
- ^ 「Olpruva - フェニル酪酸ナトリウムキット」DailyMed . 2022年12月22日. 2023年1月21日閲覧。
- ^ “アンモナプス EPAR”.欧州医薬品庁。 2018 年 9 月 17 日。2023 年1 月 3 日に取得。
- ^ abc Iannitti T, Palmieri B (2011年9月). 「フェニル酪酸ナトリウムの臨床および実験的応用」. Drugs in R&D . 11 (3): 227– 249. doi :10.2165/11591280-000000000-00000. PMC 3586072. PMID 21902286 .
- ^ abcdef Batshaw ML, MacArthur RB, Tuchman M (2001年1月). 「尿素サイクル異常症に対する代替経路療法:20年後」. The Journal of Pediatrics . 138 (1 Suppl): S46– S54, discussion S54–S55. doi :10.1067/mpd.2001.111836. PMID 11148549.
- ^ Walker V (2009年9月). 「遺伝性尿素回路欠損症におけるアンモニア毒性とその予防」. Diabetes, Obesity & Metabolism . 11 (9): 823– 835. doi :10.1111/j.1463-1326.2009.01054.x. PMID 19531057. S2CID 25998574.
- ^ 「ブフェニル:FDA承認医薬品」米国食品医薬品局(FDA) 2017年2月8日時点のオリジナルよりアーカイブ。 2013年10月26日閲覧。
- ^ ブフェニルFDA承認パッケージ(PDF) .米国食品医薬品局(FDA)(報告書). 2020年10月20日時点のオリジナル(PDF)からのアーカイブ。
- ^ Brusilow S, Tinker J, Batshaw ML (1980年2月). 「アミノ酸のアシル化:先天性尿素合成異常症における窒素排泄のメカニズム」. Science . 207 (4431): 659– 661. Bibcode :1980Sci...207..659B. doi :10.1126/science.6243418. PMID: 6243418.
- ^ Batshaw ML, Brusilow S, Waber L, Blom W, Brubakk AM, Burton BK, 他 (1982年6月). 「先天性尿素合成異常症の治療:老廃窒素合成および排泄の代替経路の活性化」. The New England Journal of Medicine . 306 (23): 1387– 1392. doi :10.1056/nejm198206103062303. PMID 7078580.
- ^ Brusilow SW, Danney M, Waber LJ, Batshaw M, Burton B, Levitsky L, 他 (1984年6月). 「先天性尿素合成異常症の小児における反復性高アンモニア血症の治療」. The New England Journal of Medicine . 310 (25): 1630– 1634. doi :10.1056/nejm198406213102503. PMID 6427608.
- ^ Brusilow SW (1991年2月). 「フェニルアセチルグルタミンは老廃窒素排泄の媒体として尿素の代替となる可能性がある」.小児研究. 29 (2): 147– 150. doi : 10.1203/00006450-199102000-00009 . PMID 2014149.
- ^ Tuchman M, Knopman DS, Shih VE (1990年10月). 「高オルニチン血症、高アンモニア血症、およびホモシトルリン尿症症候群を呈する成人兄弟におけるエピソード性高アンモニア血症」Archives of Neurology . 47 (10): 1134– 1137. doi :10.1001/archneur.1990.00530100104022. PMID 2222247.
- ^ Chanoux RA, Rubenstein RC (2012年7月17日). 「嚢胞性線維症におけるCFTR欠損を回避するための標的としての分子シャペロン」. Frontiers in Pharmacology . 3 (137): 137. doi : 10.3389/fphar.2012.00137 . PMC 3398409. PMID 22822398 .
- ^ Dover GJ, Brusilow S, Charache S (1994年7月). 「鎌状赤血球貧血患者におけるフェニル酪酸ナトリウム経口投与による胎児ヘモグロビン産生の誘導」Blood . 84 (1): 339– 343. doi : 10.1182/blood.V84.1.339.339 . PMID 7517215.
- ^ Trompeter S, Roberts I (2009年2月). 「小児鎌状赤血球症におけるヘモグロビンF調節」. British Journal of Haematology . 144 (3): 308– 316. doi :10.1111/j.1365-2141.2008.07482.x. PMID 19036119. S2CID 23928373.
- ^ Moumné L, Betuing S, Caboche J (2013年10月). 「ハンチントン病における遺伝子調節異常の多様な側面」. Frontiers in Neurology . 4 : 127. doi : 10.3389/fneur.2013.00127 . PMC 3806340. PMID 24167500 .
- ^ Kang HL, Benzer S, Min KT (2002年1月). 「薬剤投与によるショウジョウバエの寿命延長」. Proceedings of the National Academy of Sciences of the United States of America . 99 (2): 838– 843. Bibcode :2002PNAS...99..838K. doi : 10.1073/pnas.022631999 . PMC 117392. PMID 11792861 .
- ^ Iannitti T, Palmieri B (2011年9月). 「フェニル酪酸ナトリウムの臨床および実験的応用」. Drugs in R&D . 11 (3): 227– 249. doi :10.2165/11591280-000000000-00000. PMC 3586072 . PMID 21902286.
同著者らは、常染色体劣性若年性パーキンソン病におけるドーパミン作動性ニューロンの消失に病理学的に関連するパーキン関連エンドセリン受容体様受容体(Pael-R)の蓄積に対するフェニル酪酸の効果を調査し、(i) フェニル酪酸がPael-Rタンパク質の正常な発現を回復させ、Pael-Rの過剰発現によって引き起こされるERストレスを抑制することを示した。 (ii) フェニル酪酸は、ERストレス誘導性シグナル伝達経路の活性化とそれに続く神経細胞死を減弱させる。(iii) フェニル酪酸は、ERストレス条件下でERストレス応答を誘導できない酵母の生存率を回復させる。これらの知見から、著者は、フェニル酪酸がERに蓄積するPael-Rを含むミスフォールドタンパク質の量を直接減少させることでERストレスを抑制すると結論付けている。[175]
- ^ Kormanik K, Kang H, Cuebas D, Vockley J, Mohsen AW (2012年12月). 「フェニル酪酸の代謝における中鎖アシルCoA脱水素酵素の関与を示す証拠」. Molecular Genetics and Metabolism . 107 (4): 684– 689. doi :10.1016/j.ymgme.2012.10.009. PMC 3504130. PMID 23141465 .
