| |||
| 名前 | |||
|---|---|---|---|
| IUPAC名
1ʟ-1(OH),3,4/5-テトラヒドロキシシクロヘキサンカルボン酸[1]
| |||
| 推奨IUPAC名
(1 S ,3 R ,4 S ,5 R )-1,3,4,5-テトラヒドロキシシクロヘキサン-1-カルボン酸 | |||
| 識別子 | |||
3Dモデル(JSmol)
|
| ||
| チェビ | |||
| チェムブル | |||
| ケムスパイダー | |||
| ECHA 情報カード | 100.000.976 | ||
PubChem CID
|
| ||
| ユニイ | |||
CompToxダッシュボード (EPA)
|
| ||
| |||
| |||
| プロパティ | |||
| C 7 H 12 O 6 | |||
| モル質量 | 192.17 g/モル | ||
| 密度 | 1.35 g/cm 3 | ||
| 融点 | 168℃(334℉; 441K) | ||
| 危険 | |||
| GHSラベル: | |||
 [2] [2]
| |||
| 警告[2] | |||
| H319 [2] | |||
| P264、P280、P305+P351+P338、P337+P313 [2] | |||
| NFPA 704(ファイアダイヤモンド) | |||
特に記載がない限り、データは標準状態(25 °C [77 °F]、100 kPa)における材料のものです。
| |||
キナ酸は、化学式(CHOH) 3 (CH 2 ) 2 C(OH)CO 2 Hで表される有機化合物です。この化合物は、シクリトール、環状ポリオール、およびシクロヘキサンカルボン酸に分類されます。植物から抽出できる無色の固体です。キナ酸はコーヒーの酸味に関与しており、コーヒーの重量の約13%に含まれています。[3]
発生と準備
この化合物はキナの樹皮、コーヒー豆、ユーカリ・グロブルスの樹皮から得られます。[4]タラタンニン の成分です。
セイヨウイラクサ(Urtica dioica)も、もうひとつの一般的な供給源です。 [5]
キナ酸はクロロゲン酸の加水分解によって合成されます。キナ酸はコーヒーの酸味にも関与しています。
歴史と生合成
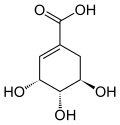
この物質は、1790年にドイツの 薬剤師フリードリヒ・クリスチャン・ホフマンによって、レールでキナから初めて単離されました。[6]動物の代謝による馬尿酸への変換は、1863年にドイツの化学者エドゥアルト・ラウテマンによって研究されました。[7]
生合成は、グルコースからエリスロース4-リン酸への変換から始まります。この4炭素基質はホスホエノールピルビン酸と縮合し、合成酵素の作用により7炭素基質である3-デオキシ-D-アラビノヘプツロソン酸7-リン酸(DAHP)を生成します。その後、デヒドロキナ酸合成酵素と脱水素酵素が関与する2つの反応を経て、DAHPが合成されます。[8]
誘導された二環式ラクトンはキニドと呼ばれます。一例として、4-カフェオイル-1,5-キニドが挙げられます。
キナ酸の脱水素化と酸化により没食子酸が得られる。[8]
応用と薬効
キナ酸は収斂剤として使われます。
この酸は医薬品の合成に用いられる多用途のキラル出発物質である。[8]これは、インフルエンザA型およびB型の治療に使用されるオセルタミビルの合成における構成要素である。
参考文献
- ^ 「シクリトールの命名法、勧告、1973年 – 勧告 – ヒドロキシル基または置換ヒドロキシル基以外の基を持つシクリトール – I-8. および I-9.2」iupac.qmul.ac.uk . 2025年3月19日閲覧。
- ^ abcd 「D-(−)-キナ酸安全データシート」Sigma-Aldrich .
- ^ ヴィアニ、リナントニオ;ペトラッコ、マリノ (2007)。 "コーヒー"。ウルマンの工業化学百科事典。土井:10.1002/14356007.a07_315.pub2。ISBN 978-3-527-30385-4。
- ^ Santos, Sónia AO; Freire, Carmen SR; Domingues, M. Rosário M.; Silvestre, Armando JD; Neto, Carlos Pascoal (2011). 「高性能液体クロマトグラフィー-質量分析法によるユーカリ・グロブルス・ラビル樹皮の極性抽出物中のフェノール成分の特性評価」Journal of Agricultural and Food Chemistry . 59 (17): 9386– 93. Bibcode :2011JAFC...59.9386S. doi :10.1021/jf201801q. PMID 21761864.
- ^ Đurović, Saša; Kojić, Ivan; Radić, Danka; Smyatskaya, Yulia A.; Bazarnova, Julia G.; Filip, Snežana; Tosti, Tomislav (2024年3月8日). 「イラクサ(Urtica dioica L.)の化学成分:フェノール性およびポリフェノール性化合物とその生理活性に関する包括的レビュー」. International Journal of Molecular Sciences . 25 (6): 3430. doi : 10.3390/ijms25063430 . ISSN 1422-0067. PMC 10970493. PMID 38542403 .
- ^ ホフマン:クレルの化学年記。 1790、II、p. 314、S. Baup: Über die Chinasäure und einige ihrer Verbindungenで引用。掲載:『Annalen der Physik und Chemie』 1833 年、p. 64–70 ( [1]、p. 64、 Google Books )。
- ^ Lautemann, E. (1863) 「Ueber die Reduction der Chinasäure zu Benzoësäure und die Verwandlung derselben in Hippursäure im therischen Organismus」 (動物体内でのキナ酸の安息香酸への還元とその馬尿酸への変換について)、Annalen der Chemie、125 : 9–13。
- ^ abc バルコ、アキレ;ベネッティ、シモネッタ。デリシ、カルメラ。マルケッティ、パオロ。ポリーニ、ジャン P.ザニラート、ヴィニシオ (1997)。 「D(-)-キナ酸: 天然物合成のためのキロンの貯蔵庫」。四面体: 非対称。8 : 3515–3545。土井:10.1016/S0957-4166(97)00471-0。
さらに読む
- 「キナ酸 - 自然由来のキラル化合物 - ドイツ、ブラウンシュヴァイクのブフラー社キニーネ工場」キナ酸。2001年3月6日時点のオリジナルよりアーカイブ。 2005年9月5日閲覧。
- 「キナ酸」Fast Health誌。 2005年9月5日閲覧。
- 「異物代謝の歴史」。2005年4月12日時点のオリジナルよりアーカイブ。2005年9月5日閲覧。
- リプリー、ジョージ、ダナ、チャールズ・A.編 (1879). .アメリカ百科事典.




