| |||
| 名前 | |||
|---|---|---|---|
| IUPAC名
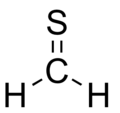
チオホルムアルデヒド
| |||
| IUPAC体系名
メタンチアル | |||
| 識別子 | |||
| |||
3Dモデル(JSmol)
|
| ||
| ケムスパイダー |
| ||
| EC番号 |
| ||
PubChem CID
|
| ||
CompToxダッシュボード (EPA)
|
| ||
| |||
| |||
| プロパティ | |||
| CH 2 S | |||
| モル質量 | 46.09 | ||
| 外観 | 未知 | ||
特に記載がない限り、データは標準状態(25 °C [77 °F]、100 kPa)における材料のものです。
| |||
チオホルムアルデヒドは、化学式CH 2 Sで表される有機硫黄化合物です。最も単純なチオアルデヒドです。この化合物は、同じ実験式を持つ安定した無色の化合物である1,3,5-トリチアンにオリゴマー化するため、凝縮状態(固体または液体)では観察されません。
これらの濃縮形態は不安定であるにもかかわらず、希薄ガスとしてのチオホルムアルデヒドは広く研究されてきた。この目的のために、チオホルムアルデヒドはジメチルジスルフィドの熱分解によって生成される。[1]この分子は星間物質 中で観測されており[2]、その基本的な性質から多くの注目を集めている。[3] チオホルムアルデヒドが鎖状や環状を形成する傾向は、二重結合則の現れである。
チオホルムアルデヒドはオリゴマー化する傾向があるが、多くの金属錯体が知られている。一例として、Os(SCH 2 )(CO) 2 (PPh 3 ) 2が挙げられる。[4]


参考文献
- ^ ジョンソン, ドナルド R.; パウエル, フランシス X.; キルヒホフ, ウィリアム H. (1971). 「チオホルムアルデヒドのマイクロ波スペクトル、基底状態構造、および双極子モーメント」. 分子分光法ジャーナル. 39 : 136– 145.書誌コード:1971JMoSp..39..136J. doi :10.1016/0022-2852(71)90284-0.
- ^ Despois, D.、「C/1995 O1(ヘール・ボップ)彗星の分子種および同位体種の電波線観測:彗星の氷の星間起源に関する示唆」『地球、月、惑星』1999年、79巻、103-124頁。
- ^ Clouthier, DJ; Ramsay, DA (1983). 「ホルムアルデヒドとチオホルムアルデヒドの分光法」. Annual Review of Physical Chemistry . 34 : 31– 58. Bibcode :1983ARPC...34...31C. doi :10.1146/annurev.pc.34.100183.000335.
- ^ Schenk, Wolfdieter A. (2011). 「小さな硫黄含有分子の配位化学:個人的な視点」Dalton Trans . 40 (6): 1209– 1219. doi :10.1039/C0DT00975J. PMID 21088787.