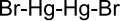| |||
| 名前 | |||
|---|---|---|---|
| IUPAC名
二臭化二水銀
| |||
| その他の名前
臭化水銀(I) 臭化
水銀 | |||
| 識別子 | |||
3Dモデル(JSmol)
|
| ||
| ケムスパイダー |
| ||
| ECHA 情報カード | 100.150.337 | ||
| EC番号 |
| ||
PubChem CID
|
| ||
| ユニイ | |||
| 国連番号 | 1634 | ||
CompToxダッシュボード (EPA)
|
| ||
| |||
| |||
| プロパティ | |||
| 水銀2臭素2 | |||
| モル質量 | 560.99グラム/モル | ||
| 外観 | 白色から黄色の正方晶系結晶 | ||
| 臭い | 無臭 | ||
| 密度 | 7.307 g/cm 3、固体 | ||
| 融点 | 405℃(761℉; 678K) | ||
| 沸点 | 約390℃(734°F; 663 K)で昇華する[1] | ||
| 3.9 x 10 −5 g/100 mL | |||
溶解度積(K sp)
|
6.4 × 10 −23 [2] | ||
| 溶解度 | エーテル、アセトン、アルコールに不溶 | ||
磁化率(χ)
|
−28.6·10 −6 cm 3 /モル | ||
| 構造 | |||
| リニア | |||
| 危険性[3] | |||
| GHSラベル: | |||
  
| |||
| 危険 | |||
| H300、H310、H330、H373、H410 | |||
| P260、P262、P264、P270、P271、P273、P280、P284、P301+P310、P302+P350、P304+P340、P310、P314、P320、P321、P322、P330、P361、P363、P391、P403+P233、P405、P501 | |||
| 引火点 | 不燃性 | ||
| 関連化合物 | |||
その他の陰イオン
|
フッ化水銀(I) 塩化水銀(I) ヨウ化水銀(I) | ||
その他の陽イオン
|
臭化亜鉛 臭化カドミウム | ||
関連化合物
|
臭化水銀(II) | ||
特に記載がない限り、データは標準状態(25 °C [77 °F]、100 kPa)における材料のものです。
| |||
臭化水銀(I)または臭化第一水銀は、水銀と臭素からなる化合物で、化学式はHg 2 Br 2です。加熱すると白から黄色に変化し[1]、紫外線を照射するとサーモンピンクの蛍光を発します。音響光学デバイスに応用されています。[4]
非常に珍しい鉱物形態はクズミナイトと呼ばれ、化学式はHg 2 (Br,Cl) 2です。
反応
臭化水銀(I)は、元素水銀を元素臭素で酸化するか、臭化ナトリウムを硝酸水銀(I)溶液に加えることによって製造されます。[1]臭化水銀(II)と元素水銀に分解します[いつ? ] [ 4]
構造
直線状のX-Hg-Hg-X単位を含む他のHg(I)(第一水銀)化合物と同様に、Hg 2 Br 2は直線状のBrHg 2 Br単位を含み、Hg-Hg結合長は249 pm(金属中のHg-Hgは300 pm)で、Hg-Br結合長は271 pmである。[5] 各Hg原子の全体的な配位は八面体であり、最も近い2つの原子に加えて、332 pmに4つの他のBr原子がある。[5]この化合物は、実際には分子化合物であるが、しばしば Hg 2 2+ 2Br − [6]と定式化される。
参考文献
- ^ abc ペリー、デール・L.; フィリップス、シドニー・L. (1995)、無機化合物ハンドブック、CRCプレス、p. 255、ISBN 0-8493-8671-3、 2008年5月30日閲覧
- ^ジョン ・ランブル( 2018年6月18日)CRC化学物理ハンドブック(99版)CRCプレス pp.5-188.ISBN 978-1138561632。
- ^ "483230 臭化水銀(I) 99.9%以上". Sigma-Aldrich . 2008年5月30日閲覧。
- ^ ab マッキンタイア、ジェーン・エリザベス; ダニエル、FM; スターリング、VM (1992) 『無機化合物辞典』第1巻、CRCプレス、314ページ、ISBN 0-412-30120-2、 2008年5月30日閲覧
- ^ ab Wells AF (1984)構造無機化学第5版 Oxford Science Publications ISBN 0-19-855370-6
- ^ コットン、F.アルバート;ウィルキンソン、ジェフリー; ムリーリョ、カルロスA.; ボッホマン、マンフレッド(1999年)、Advanced Inorganic Chemistry(第6版)、ニューヨーク:Wiley-Interscience、ISBN 0-471-19957-5