クレムソン大学のジョン・W・ハフマン研究グループは、 450種類以上のカンナビノイドを合成しました。[1] [2] [3] [4] その一部は以下のとおりです。
| 名称 | クラス | CB1におけるKi / nM | CB 2でのKi / nM | 選択性 | 構造 |
|---|---|---|---|---|---|
| JWH-004 | ナフトイルインドール | 48 ± 13 | 4 ± 1.5 | CB 2 (12x) | 
|
| JWH-007 [5] | ナフトイルインドール | 9.5 ± 4.5 | 2.9 ± 2.6 | CB 2 (3.3倍) | 
|
| JWH-009 | ナフトイルインドール | >10000 | 141 ± 14 | CB 2 (>70倍) | 
|
| JWH-011 | ナフトイルインドール | 
| |||
| JWH-015 [5] | ナフトイルインドール | 164 ± 22 | 13.8 ± 4.6 | CB 2 (12x) | 
|
| JWH-016 | ナフトイルインドール | 22 ± 1.5 | 4.3 ± 1.6 | CB 2 (5.1倍) | 
|
| JWH-018 [5] | ナフトイルインドール | 9 ± 5 | 2.9 ± 2.6 | CB 2 (3.1倍) | 
|
| JWH-019 | ナフトイルインドール | 9.8 ± 2 | 5.55 ± 2 | CB 2 (1.77倍) | 
|
| JWH-020 | ナフトイルインドール | 128 ± 17 | 205 ± 20 | CB 1 (1.6倍) | 
|
| JWH-030 | ナフトイルピロール | 87 ± 3 | 320 ± 127 | CB 1 (3.7倍) | 
|
| JWH-031 | ナフトイルピロール | 399 ± 109 | 
| ||
| JWH-032 | ナフトイルピロール | >10000 | >10000 | — | 
|
| JWH-033 | ナフトイルピロール | 666 ± 77 | 
| ||
| JWH-036 | ナフトイルピロール | 309 ± 11 | 
| ||
| JWH-042 [6] | ナフトイルインドール | >10000 | 5050 ± 192 | CB 2 | 
|
| JWH-043 [6] | ナフトイルインドール | 1180 ± 44 | 964 ± 242 | CB 2 (1.2倍) | 
|
| JWH-044 | ナフトイルピロール | >10000 | >10000 | — | 
|
| JWH-045 | ナフトイルピロール | >10000 | >10000 | — | 
|
| JWH-046 [6] | ナフトイルインドール | 343 ± 38 | 16.3 ± 4.9 | CB 2 (21x) | 
|
| JWH-047 [6] | ナフトイルインドール | 59 ± 3 | 3.47 ± 1.80 | CB 2 (17x) | 
|
| JWH-048 [6] | ナフトイルインドール | 10.7 ± 1.0 | 0.49 ± 0.13 | CB 2 (22倍) | 
|
| JWH-049 [6] | ナフトイルインドール | 55.1 ± 17.0 | 32.3 ± 2.4 | CB 2 (1.7倍) | 
|
| JWH-050 [6] | ナフトイルインドール | 342 ± 6 | 526 ± 133 | CB 1 (1.5倍) | 
|
| JWH-051 | ジベンゾピラン | 1.20 | 0.03 | CB 2 (40倍) | 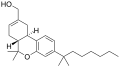
|
| JWH-056 [7] | ジベンゾピラン | >10000 | 32 ± 9 | CB 2 | 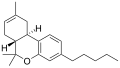
|
| JWH-057 [8] | ジベンゾピラン | 23 ± 7 | 2.9 ± 1.6 | CB 2 (8x) | 
|
| JWH-065 [7] | ジベンゾピラン | 399 ± 76 | 10 ± 2 | CB 2 (40倍) | 
|
| JWH-070 [6] | ナフトイルインドール | >10000 | >10000 | 
| |
| JWH-071 [6] | ナフトイルインドール | 1340 ± 123 | 2940 ± 852 | CB 1 (2.2倍) | 
|
| JWH-072 | ナフトイルインドール | 1050 ± 5.5 | 170 ± 54 | CB 2 (6x) | 
|
| JWH-073 | ナフトイルインドール | 8.9 ± 1.8 | 27 ± 12 | CB 1 (3x) | 
|
| JWH-076 [5] | ナフトイルインドール | 214 ± 11 | 106 ± 46 | CB 2 (2x) | 
|
| JWH-077 [6] | ナフトイルインドール | >10000 | >10000 | 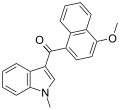
| |
| JWH-078 [6] | ナフトイルインドール | 817 ± 60 | 633 ± 116 | CB 2 (1.3倍) | 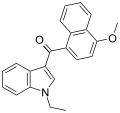
|
| JWH-079 [6] | ナフトイルインドール | 63.0 ± 3.0 | 32.0 ± 6.0 | CB 2 (2x) | 
|
| JWH-080 [6] | ナフトイルインドール | 8.9 ± 1.8 | 2.21 ± 1.30 | CB 2(4倍) | 
|
| JWH-081 [6] | ナフトイルインドール | 1.2 ± 0.03 | 12.4 ± 2.2 | CB 1 (10倍) | 
|
| JWH-082 [6] | ナフトイルインドール | 5.3 ± 0.8 | 6.40 ± 0.94 | CB 1 (1.2倍) | 
|
| JWH-083 [6] | ナフトイルインドール | 106 ± 12 | 102 ± 50 | — | 
|
| JWH-091 [9](Δ 8 - THCP) | ジベンゾピラン | 22.0 ± 3.9 | 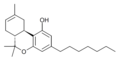
| ||
| JWH-093 [6] | ナフトイルインドール | 40.7 ± 2.8 | 59.1 ± 10.5 | CB 1 (1.45倍) | 
|
| JWH-094 [6] | ナフトイルインドール | 476 ± 67 | 97.3 ± 2.7 | CB 2 (4.9倍) | 
|
| JWH-095 [6] | ナフトイルインドール | 140 ± 4.3 | 312 ± 83 | CB 1 (2.2倍) | 
|
| JWH-096 [6] | ナフトイルインドール | 33.7 ± 2.9 | 13.3 ± 5.6 | CB 2 (2.5倍) | 
|
| JWH-097 [6] | ナフトイルインドール | 455 ± 28 | 121 ± 15 | CB 2 (3.8倍) | 
|
| JWH-098 [6] | ナフトイルインドール | 4.5 ± 0.1 | 1.9 ± 0.3 | CB 2 (2.4倍) | 
|
| JWH-099 [6] | ナフトイルインドール | 35.3 ± 9.0 | 17.8 ± 2.9 | CB 2 (2x) | 
|
| JWH-100 [6] | ナフトイルインドール | 381 ± 102 | 155 ± 74 | CB 2 (2.5倍) | 
|
| JWH-102 [7] | ジベンゾピラン | 7.9 ± 0.9 | 5.2 ± 2.0 | CB 2 (1.5倍) | 
|
| JWH-103 [7] | ジベンゾピラン | 28 ± 3 | 23 ± 7 | CB 2 (1.2倍) | 
|
| JWH-116 [10] | ナフトイルインドール | 52 ± 5 | 
| ||
| JWH-120 [5] | ナフトイルインドール | 1054 ± 31 | 6.1 ± 0.7 | CB 2 (173x) | 
|
| JWH-122 [10] | ナフトイルインドール | 0.69 ± 0.05 | 1.2 ± 1.2 | — | 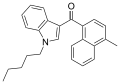
|
| JWH-124 (Δ 8 -パラヘキシル) | ジベンゾピラン | 41.0 ± 3.8 | 
| ||
| JWH-130 ( Δ8 - THCB ) | ジベンゾピラン | 65.0 ± 13 | 
| ||
| JWH-133 [7] | ジベンゾピラン | 677 ± 132 | 3.4 ± 1.0 | CB 2(200倍) | 
|
| JWH-138 [11] | ジベンゾピラン | 8.5 ± 1.4 | 
| ||
| JWH-139 [12] | ジベンゾピラン | 2290 ± 505 | 14 ± 10 | CB 2 (164x) | 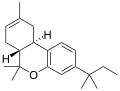
|
| JWH-142 [7] | ジベンゾピラン | 529 ± 49 | 35 ± 14 | CB 2 (15倍) | 
|
| JWH-143 [7] | ジベンゾピラン | 924 ± 104 | 65 ± 8 | CB 2 (14x) | 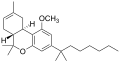
|
| JWH-145 [13] | ナフトイルピロール | 14 ± 2 | 6.4 ± 0.4 | CB 2(2.2倍) | 
|
| JWH-146 [13] | ナフトイルピロール | 21 ± 2 | 62 ± 5 | CB 2 (3.0倍) | 
|
| JWH-147 [13] | ナフトイルピロール | 11 ± 1 | 7.1 ± 0.2 | CB 2 (1.5倍) | 
|
| JWH-148 [5] | ナフトイルインドール | 123 ± 8 | 14.0 ± 1.0 | CB 2 (8x) | 
|
| JWH-149 [5] | ナフトイルインドール | 5.0 ± 2.1 | 0.73 ± 0.03 | CB 2 (6.8倍) | 
|
| JWH-150 [13] | ナフトイルピロール | 60 ± 1 | 15 ± 2 | CB 2(4倍) | 
|
| JWH-151 [5] | ナフトイルインドール | >10000 | 30 ± 1.1 | CB 2 (>333倍) | 
|
| JWH-153 [5] | ナフトイルインドール | 250 ± 24 | 11 ± 0.5 | CB 2 (23倍) | 
|
| JWH-156 [13] | ナフトイルピロール | 404 ± 18 | 104 ± 18 | CB 2(4倍) | 
|
| JWH-159 [5] | ナフトイルインドール | 45 ± 1 | 10.4 ± 1.4 | CB 2 (4.3倍) | 
|
| JWH-160 [5] | ナフトイルインドール | 1568 ± 201 | 441 ± 110 | CB 2 (3.6倍) | 
|
| JWH-161 | ジベンゾピランハイブリッド | 19.0 | 
| ||
| JWH-163 [5] | ナフトイルインドール | 2358 ± 215 | 138 ± 12 | CB 2 (17x) | 
|
| JWH-164 [5] | ナフトイルインドール | 6.6 ± 0.7 | 6.9 ± 0.2 | — | 
|
| JWH-165 [5] | ナフトイルインドール | 204 ± 26 | 71 ± 8 | CB 2 (2.9倍) | 
|
| JWH-166 [5] | ナフトイルインドール | 44 ± 10 | 1.9 ± 0.08 | CB 2 (23倍) | 
|
| JWH-167 | フェニルアセチルインドール | 90 ± 17 | 159 ± 14 | CB 1(1.77倍) | 
|
| JWH-171 | 炭化水素 | 51 | 
| ||
| JWH-175 [10] | ナフチルメチルインドール | 22 ± 2 | 
| ||
| JWH-176 [10] | 炭化水素 | 26 ± 4 | 
| ||
| JWH-180 [5] | ナフトイルインドール | 26 ± 2 | 9.6 ± 2.0 | CB 2 (2.7倍) | 
|
| JWH-181 [5] | ナフトイルインドール | 1.3 ± 0.1 | 0.62 ± 0.04 | CB 2 (2.1倍) | 
|
| JWH-182 [5] | ナフトイルインドール | 0.65 ± 0.03 | 1.1 ± 0.1 | CB 1 (1.7倍) | 
|
| JWH-184 [10] | ナフチルメチルインドール | 23 ± 6 | 
| ||
| JWH-185 [10] | ナフチルメチルインドール | 17 ± 3 | 
| ||
| JWH-186 [14] | ジベンゾピラン | 187 ± 23 | 5.6 ± 1.7 | CB 2 (33x) | 
|
| JWH-187 [14] | ジベンゾピラン | 84 ± 16 | 3.4 ± 0.5 | CB 2 (25倍) | 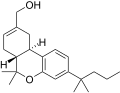
|
| JWH-188 [14] | ジベンゾピラン | 270 ± 58 | 18 ± 2 | CB 2 (15倍) | 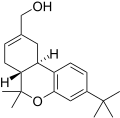
|
| JWH-189 [5] | ナフトイルインドール | 52 ± 2 | 12 ± 0.8 | CB 2 (4.3倍) | 
|
| JWH-190 [14] | ジベンゾピラン | 8.8 ± 1.4 | 1.6 ± 0.03 | CB 2 (5.5倍) | 
|
| JWH-191 [14] | ジベンゾピラン | 1.8 ± 0.3 | 0.52 ± 0.03 | CB 2 (3.5倍) | 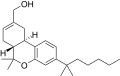
|
| JWH-192 [10] | ナフチルメチルインドール | 41 ± 13 | 
| ||
| JWH-193 [10] | ナフトイルインドール | 6 ± 1 | 
| ||
| JWH-194 [10] | ナフチルメチルインドール | 127 ± 19 | 
| ||
| JWH-195 [10] | ナフチルメチルインドール | 113 ± 28 | 
| ||
| JWH-196 [10] | ナフチルメチルインドール | 151 ± 18 | 
| ||
| JWH-197 [10] | ナフチルメチルインドール | 323 ± 98 | 
| ||
| JWH-198 [10] | ナフトイルインドール | 10 ± 2 | 
| ||
| JWH-199 [10] | ナフチルメチルインドール | 20 ± 2 | 
| ||
| JWH-200 [10] | ナフトイルインドール | 42 ± 5 | 
| ||
| JWH-201 [15] | フェニルアセチルインドール | 1064 ± 21 | 444 ± 14 | CB 2 (2.4倍) | 
|
| JWH-202 [15] | フェニルアセチルインドール | 1678 ± 63 | 645 ± 6 | CB 2 (2.6倍) | 
|
| JWH-203 [15] | フェニルアセチルインドール | 8.0 ± 0.9 | 7.0 ± 1.3 | — | 
|
| JWH-204 [15] | フェニルアセチルインドール | 13 ± 1 | 25 ± 1 | CB 1 (1.9倍) | 
|
| JWH-205 [15] | フェニルアセチルインドール | 124 ± 23 | 180 ± 9 | CB 1 (1.45倍) | 
|
| JWH-206 [15] | フェニルアセチルインドール | 389 ± 25 | 498 ± 37 | CB 1 (1.28倍) | 
|
| JWH-207 [15] | フェニルアセチルインドール | 1598 ± 134 | 3723 ± 10 | CB 1 (2.33倍) | 
|
| JWH-208 [15] | フェニルアセチルインドール | 179 ± 7 | 570 ± 127 | CB 1 (3.18倍) | 
|
| JWH-209 [15] | フェニルアセチルインドール | 746 ± 49 | 1353 ± 270 | CB 1 (1.81倍) | 
|
| JWH-210 [5] | ナフトイルインドール | 0.46 ± 0.03 | 0.69 ± 0.01 | CB 1 (1.5倍) | 
|
| JWH-211 [5] | ナフトイルインドール | 70 ± 0.8 | 12 ± 0.8 | CB 2 (5.8倍) | 
|
| JWH-212 [5] | ナフトイルインドール | 33 ± 0.9 | 10 ± 1.2 | CB 2 (3.3倍) | 
|
| JWH-213 [5] | ナフトイルインドール | 1.5 ± 0.2 | 0.42 ± 0.05 | CB 2 (3.6倍) | 
|
| JWH-215 [14] | ジベンゾピラン | 1008 ± 117 | 85 ± 21 | CB 2 (12x) | 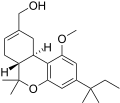
|
| JWH-216 [14] | ジベンゾピラン | 1856 ± 148 | 333 ± 104 | CB 2 (5.6倍) | 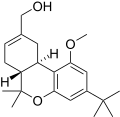
|
| JWH-217 [14] | ジベンゾピラン | >10000 | 1404 ± 66 | CB 2 (>7倍) | 
|
| JWH-220 | 炭化水素 | 19 | 
| ||
| JWH-224 [14] | ジベンゾピラン | 347 ± 34 | 28 ± 1 | CB 2 (12.3倍) | 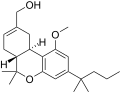
|
| JWH-225 [14] | ジベンゾピラン | >10000 | 325 ± 70 | CB 2 (>31倍) | 
|
| JWH-226 [14] | ジベンゾピラン | 4001 ± 282 | 43 ± 3 | CB 2 (93x) | 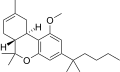
|
| JWH-227 [14] | ジベンゾピラン | 40 ± 6 | 4.4 ± 0.3 | CB 2 (9x) | 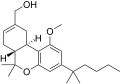
|
| JWH-229 [16] | ジベンゾピラン | 3134 ± 110 | 18 ± 2 | CB 2 (174x) | 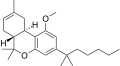
|
| JWH-230 [14] | ジベンゾピラン | 15 ± 3 | 1.4 ± 0.12 | CB 2 (10.7倍) | 
|
| JWH-233 [14] | ジベンゾピラン | 14 ± 3 | 1.0 ± 0.3 | CB 2 (14x) | 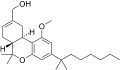
|
| JWH-234 [5] | ナフトイルインドール | 8.4 ± 1.8 | 3.8 ± 0.6 | CB 2(2.2倍) | 
|
| JWH-235 [5] | ナフトイルインドール | 338 ± 34 | 123 ± 34 | CB 2 (2.7倍) | 
|
| JWH-236 [5] | ナフトイルインドール | 1351 ± 204 | 240 ± 63 | CB 2 (5.6倍) | 
|
| JWH-237 [15] | フェニルアセチルインドール | 38 ± 10 | 106 ± 2 | CB 1(2.8倍) | 
|
| JWH-239 [5] | ナフトイルインドール | 342 ± 20 | 52 ± 6 | CB 2 (6.6倍) | 
|
| JWH-240 [5] | ナフトイルインドール | 14 ± 1 | 7.2 ± 1.3 | CB 2 (1.9倍) | 
|
| JWH-241 [5] | ナフトイルインドール | 147 ± 20 | 49 ± 7 | CB 2 (3.0倍) | 
|
| JWH-242 [5] | ナフトイルインドール | 42 ± 9 | 6.5 ± 0.3 | CB 2 (6.5倍) | 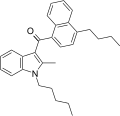
|
| JWH-243 [13] | ナフトイルピロール | 285 ± 40 | 41 ± 3 | CB 2(6.95倍) | 
|
| JWH-244 [13] | ナフトイルピロール | 130 ± 6 | 18 ± 1 | CB 2 (7.22倍) | 
|
| JWH-245 [13] | ナフトイルピロール | 276 ± 4 | 25 ± 2 | CB 2 (11x) | 
|
| JWH-246 [13] | ナフトイルピロール | 70 ± 4 | 16 ± 1 | CB 2 (4.38倍) | 
|
| JWH-247 [14] | ジベンゾピラン | 427 ± 31 | 99 ± 4 | CB 2 (4.3倍) | 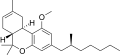
|
| JWH-248 [15] | フェニルアセチルインドール | 1028 ± 39 | 657 ± 19 | CB 2 (1.56倍) | 
|
| JWH-249 [15] | フェニルアセチルインドール | 8.4 ± 1.8 | 20 ± 2 | CB 1 (2.38倍) | 
|
| JWH-250 [15] | フェニルアセチルインドール | 11 ± 2 | 33 ± 2 | CB 1 (3x) | 
|
| JWH-251 [15] | フェニルアセチルインドール | 29 ± 3 | 146 ± 36 | CB 2 (5x) | 
|
| JWH-252 [15] | フェニルアセチルインドール | 23 ± 3 | 19 ± 1 | CB 2 (1.2倍) | 
|
| JWH-253 [15] | フェニルアセチルインドール | 62 ± 10 | 84 ± 12 | CB 1 (1.35倍) | 
|
| JWH-254 [14] | ジベンゾピラン | 4724 ± 509 | 319 ± 16 | CB 2 (14.8倍) | 
|
| JWH-256 [14] | ジベンゾピラン | 4300 ± 888 | 97 ± 18 | CB 2 (44x) | 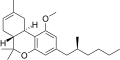
|
| JWH-258 [5] | ナフトイルインドール | 4.6 ± 0.6 | 10.5 ± 1.3 | CB 1 (2.3倍) | 
|
| JWH-259 [5] | ナフトイルインドール | 220 ± 29 | 74 ± 7 | CB 2 (3.0倍) | 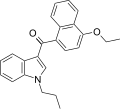
|
| JWH-260 [5] | ナフトイルインドール | 29 ± 0.4 | 25 ± 1.9 | CB 2 (1.2倍) | 
|
| JWH-261 [5] | ナフトイルインドール | 767 ± 105 | 221 ± 14 | CB 2 (3.5倍) | 
|
| JWH-262 [5] | ナフトイルインドール | 28 ± 3 | 5.6 ± 0.7 | CB 2 (5.0倍) | 
|
| JWH-265 [5] | ナフトイルインドール | 3788 ± 323 | 80 ± 13 | CB 2 (47x) | 
|
| JWH-266 [5] | ナフトイルインドール | >10000 | 455 ± 55 | CB 2 (>22倍) | 
|
| JWH-267 [5] | ナフトイルインドール | 381 ± 16 | 7.2 ± 0.14 | CB 2 (53x) | 
|
| JWH-268 [5] | ナフトイルインドール | 1379 ± 193 | 40 ± 0.6 | CB 2 (34x) | 
|
| JWH-277 [14] | ジベンゾピラン | 3905 ± 91 | 589 ± 65 | CB 2 (6.6倍) | 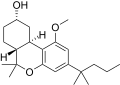
|
| JWH-278 [14] | ジベンゾピラン | 906 ± 80 | 69 ± 6 | CB 2 (13x) | 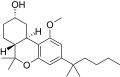
|
| JWH-292 [13] | ナフトイルピロール | 29 ± 1 | 20 ± 1 | CB 2(1.45倍) | 
|
| JWH-293 [13] | ナフトイルピロール | 100 ± 5 | 41 ± 4 | CB 2 (2.44倍) | 
|
| JWH-298 [14] | ジベンゾピラン | 812 ± 67 | 198 ± 23 | CB 2 (4.1倍) | 
|
| JWH-299 [14] | ジベンゾピラン | 415 ± 50 | 30 ± 2 | CB 2 (13.8倍) | 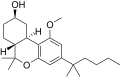
|
| JWH-300 [12] | ジベンゾピラン | 118 ± 16 | 5.3 ± 0.1 | CB 2 (22倍) | 
|
| JWH-301 [14] | ジベンゾピラン | 295 ± 64 | 48 ± 4 | CB 2 (6.1倍) | 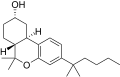
|
| JWH-302 [15] | フェニルアセチルインドール | 17 ± 2 | 89 ± 15 | CB 1(5.26倍) | 
|
| JWH-303 [15] | フェニルアセチルインドール | 117 ± 10 | 138 ± 12 | CB 1 (1.18倍) | 
|
| JWH-304 [15] | フェニルアセチルインドール | 3363 ± 332 | 2679 ± 688 | CB 2 (1.26倍) | 
|
| JWH-305 [15] | フェニルアセチルインドール | 15 ± 1.8 | 29 ± 5 | CB 1 (1.93倍) | 
|
| JWH-306 [15] | フェニルアセチルインドール | 25 ± 1 | 82 ± 11 | CB 1 (3.28倍) | 
|
| JWH-307 [13] | ナフトイルピロール | 7.7 ± 1.8 | 3.3 ± 0.2 | CB 2 (2.33倍) | 
|
| JWH-308 [13] | ナフトイルピロール | 41 ± 1 | 33 ± 2 | CB 2 (1.24倍) | 
|
| JWH-309 [13] | ナフトイルピロール | 41 ± 3 | 49 ± 7 | CB 1 (1.20倍) | 
|
| JWH-310 [14] | ジベンゾピラン | 1059 ± 51 | 36 ± 3 | CB 2 (29x) | 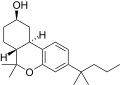
|
| JWH-311 [15] | フェニルアセチルインドール | 23 ± 2 | 39 ± 3 | CB 1 (1.70倍) | 
|
| JWH-312 [15] | フェニルアセチルインドール | 72 ± 7 | 91 ± 20 | CB 1 (1.26倍) | 
|
| JWH-313 [15] | フェニルアセチルインドール | 422 ± 19 | 365 ± 92 | CB 2 (1.16倍) | 
|
| JWH-314 [15] | フェニルアセチルインドール | 39 ± 2 | 76 ± 4 | CB 1 (1.95倍) | 
|
| JWH-315 [15] | フェニルアセチルインドール | 430 ± 24 | 182 ± 23 | CB 2 (3.36倍) | 
|
| JWH-316 [15] | フェニルアセチルインドール | 2862 ± 670 | 781 ± 105 | CB 2 (3.66倍) | 
|
| JWH-336 [12] | ジベンゾピラン | 4589 ± 367 | 153 ± 15 | CB 2 (30倍) | 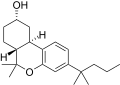
|
| JWH-338 [14] | ジベンゾピラン | >10000 | 111 ± 16 | CB 2 (>90倍) | 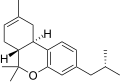
|
| JWH-339 [14] | ジベンゾピラン | >10000 | 2317 ± 93 | CB 2 (>4.3倍) | 
|
| JWH-340 [14] | ジベンゾピラン | 135 ± 6 | 30 ± 1 | CB 2 (4.5倍) | 
|
| JWH-341 [14] | ジベンゾピラン | 100 ± 8 | 10 ± 0.1 | CB 2(10倍) | 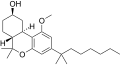
|
| JWH-346 [13] | ナフトイルピロール | 67 ± 6 | 39 ± 2 | CB 2(1.72倍) | 
|
| JWH-347 [13] | ナフトイルピロール | 333 ± 17 | 169 ± 17 | CB 2 (1.97倍) | 
|
| JWH-348 [13] | ナフトイルピロール | 218 ± 19 | 53 ± 1 | CB 2 (4.11倍) | 
|
| JWH-349 [14] | ジベンゾピラン | 376 ± 1 | 38 ± 4 | CB 2(9.9倍) | 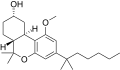
|
| JWH-350 [12] | ジベンゾピラン | 395 ± 50 | 12 ± 1 | CB 2 (33x) | 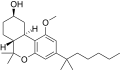
|
| JWH-351 [14] | ジベンゾピラン | >10000 | 295 ± 3 | CB 2 (>34倍) | 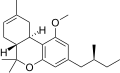
|
| JWH-352 [14] | ジベンゾピラン | >10000 | 47 ± 2 | CB 2 (>213倍) | 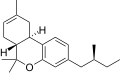
|
| JWH-353 [14] | ジベンゾピラン | 1493 ± 10 | 31 ± 1 | CB 2 (48x) | 
|
| JWH-354 [14] | ジベンゾピラン | 1961 ± 21 | 241 ± 14 | CB 2 (8.1x) | 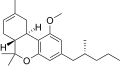
|
| JWH-355 [14] | ジベンゾピラン | 2162 ± 220 | 108 ± 17 | CB 2 (20倍) | 
|
| JWH-356 [14] | ジベンゾピラン | 5837 ± 701 | 108 ± 17 | CB 2 (54x) | 
|
| JWH-357 [14] | ジベンゾピラン | 647 ± 78 | 185 ± 4 | CB 2 (3.5倍) | 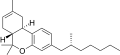
|
| JWH-358 [14] | ジベンゾピラン | 1243 ± 266 | 52 ± 3 | CB 2 (24x) | 
|
| JWH-359 | ジベンゾピラン | 2918 ± 450 | 13.0 ± 0.2 | CB 2 (220倍) | 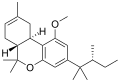
|
| JWH-360 [14] | ジベンゾピラン | 2449 ± 606 | 160 ± 8 | CB 2 (15倍) | 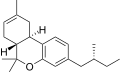
|
| JWH-361 [14] | ジベンゾピラン | 63 ± 3 | 2.7 ± 0.1 | CB 2 (23倍) | 
|
| JWH-362 [14] | ジベンゾピラン | 127 ± 8 | 34 ± 5 | CB 2 (3.7倍) | 
|
| JWH-363 [13] | ナフトイルピロール | 245 ± 5 | 71 ± 1 | CB 2 (3.45倍) | 
|
| JWH-364 [13] | ナフトイルピロール | 34 ± 3 | 29 ± 1 | CB 2 (1.17倍) | 
|
| JWH-365 [13] | ナフトイルピロール | 17 ± 1 | 3.4 ± 0.2 | CB 2 (5.0倍) | 
|
| JWH-366 [13] | ナフトイルピロール | 191 ± 12 | 24 ± 1 | CB 2 (7.96倍) | 
|
| JWH-367 [13] | ナフトイルピロール | 53 ± 2 | 23 ± 1 | CB 2 (2.30倍) | 
|
| JWH-368 [13] | ナフトイルピロール | 16 ± 1 | 9.1 ± 0.7 | CB 2 (1.76倍) | 
|
| JWH-369 [13] | ナフトイルピロール | 7.9 ± 0.4 | 5.2 ± 0.3 | CB 2 (1.52倍) | 
|
| JWH-370 [13] | ナフトイルピロール | 5.6 ± 0.4 | 4.0 ± 0.5 | CB 2 (1.40倍) | 
|
| JWH-371 [13] | ナフトイルピロール | 42 ± 1 | 64 ± 2 | CB 1 (1.52倍) | 
|
| JWH-372 [13] | ナフトイルピロール | 77 ± 2 | 8.2 ± 0.2 | CB 1 (9.39倍) | 
|
| JWH-373 [13] | ナフトイルピロール | 60 ± 3 | 69 ± 2 | CB 1 (1.15倍) | 
|
| JWH-387 [17] | ナフトイルインドール | 1.2 ± 0.1 | 1.1 ± 0.1 | — | 
|
| JWH-398 [18] | ナフトイルインドール | 2.3 ± 0.1 | 2.8 ± 0.2 | CB 1(1.22倍) | 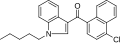
|
| JWH-416 [17] | ナフトイルインドール | 73 ± 10 | 3.3 ± 0.1 | CB 2 (22倍) | 
|
| JWH-417 [17] | ナフトイルインドール | 522 ± 58 | 13 ± 0.2 | CB 2 (40倍) | 
|
| JWH-422 [17] | ナフトイルインドール | 501 ± 48 | 20 ± 0.4 | CB 2 (25倍) | 
|
| JWH-423 [17] | ナフトイルインドール | 140 ± 10 | 6.6 ± 0.2 | CB 2 (21x) | 
|
| JWH-424 [17] | ナフトイルインドール | 21 ± 3.4 | 5.4 ± 0.2 | CB 2 (3.9倍) | 
|
| JWH-425 [17] | ナフトイルインドール | 54 ± 11 | 10 ± 0.4 | CB 2 (5.4倍) | 
|
参照
注記
- ^ Kiは、化合物のカンナビノイド受容体1型(CB 1)またはカンナビノイド受容体2型(CB 2)に対する結合親和性です
参考文献
- ^ Manera C, Tuccinardi T, Martinelli A (2008). 「カンナビノイドリガンドとしてのインドールおよび関連化合物」. Mini Rev Med Chem . 8 (4): 370–87 . doi :10.2174/138955708783955935. PMID 18473928
- ^ Wiley JL, Marusich JA, Huffman JW (2014). 「分子内の動き:合成カンナビノイドの化学構造と生体内活性の関係」. Life Sci . 97 (1): 55– 63. doi :10.1016/j.lfs.2013.09.011. PMC 3944940. PMID 24071522 .
- ^ Wiley JL、Marusich JA、Thomas BF (2017). 「コンビネーションケミストリー:新規精神活性カンナビノイドの構造活性相関」.新規精神活性物質(NPS)の神経薬理学. Current Topics in Behavioral Neurosciences. Vol. 32. pp. 231– 248. doi : 10.1007/7854_2016_17 . ISBN 978-3-319-52442-9 PMID 27753007
- ^ Banister SD, Connor M (2018). 「新規精神活性物質としての合成カンナビノイド受容体作動薬の化学と薬理学:起源」.新規精神活性物質. 実験薬理学ハンドブック. 第252巻. pp. 165– 190. doi :10.1007/164_2018_143. ISBN 978-3-030-10560-0 PMID 29980914
- ^ abcdefghijklmnopqrstu vwxyz aa ab ac ad ae af ag ah ai aj ak al am Huffman JW, Zengin G, Wu MJ, Lu J, Hynd G, Bushell K, Thompson AL, Bushell S, Tartal C, Hurst DP, Reggio PH, Selley DE, Cassidy MP, Wiley JL, Martin BR (2005年1月). 「カンナビノイドCB(1)およびCB(2)受容体における1-アルキル-3-(1-ナフトイル)インドールの構造活性相関:ナフトイル置換基の立体的および電子的効果。新規高選択性CB(2)受容体作動薬」. Bioorganic & Medicinal Chemistry . 13 (1): 89– 112. doi :10.1016/j.bmc.2004.09.050. PMID 15582455.
- ^ abcdefghijklmnopqrstu vwx Aung MM, Griffin G, Huffman JW, Wu M, Keel C, Yang B, Showalter VM, Abood ME, Martin BR (2000年8月). 「カンナビミメティックインドールのN-1アルキル鎖長がCB(1)およびCB(2)受容体結合に及ぼす影響」. Drug and Alcohol Dependence . 60 (2): 133–40 . doi :10.1016/S0376-8716(99)00152-0. PMID 10940540.
- ^ abcdefg Huffman JW, Liddle J, Yu S, Aung MM, Abood ME, Wiley JL, Martin BR (1999年12月). 「3-(1',1'-ジメチルブチル)-1-デオキシ-デルタ8-THCおよび関連化合物:CB2受容体に対する選択的リガンドの合成」. Bioorganic & Medicinal Chemistry . 7 (12): 2905–14 . doi :10.1016/s0968-0896(99)00219-9. PMID 10658595.
- ^ Huffman JW, Yu S, Showalter V, Abood ME, Wiley JL, Compton DR, Martin BR, Bramblett RD, Reggio PH (1996年9月). 「フェノール性水酸基を欠き、CB2受容体に高い親和性を示す非常に強力なカンナビノイドの合成と薬理学」. Journal of Medicinal Chemistry . 39 (20): 3875–7 . doi :10.1021/JM960394Y. PMID 8831752.
- ^ Bow EW, Rimoldi JM (2016年6月). 「古典的カンナビノイドの構造と機能の関係:CB1/CB2の調節」. Perspect Medicin Chem . 8 : 17–39 . doi :10.4137/PMC.S32171. PMC 4927043. PMID 27398024 .
- ^ abcdefghijklmno Huffman JW, Mabon R, Wu MJ, Lu J, Hart R, Hurst DP, Reggio PH, Wiley JL, Martin BR (2003年2月). 「3-インドリル-1-ナフチルメタン:新規カンナビミメティックインドールはCB(1)カンナビノイド受容体との芳香族スタッキング相互作用の証拠となる」Bioorganic & Medicinal Chemistry 11 ( 4): 539– 49. doi :10.1016/S0968-0896(02)00451-0. PMID 12538019. S2CID 29107765.
- ^ Martin BR, Jefferson R, Winckler R, Wiley JL, Huffman JW, Crocker PJ, Saha B, Razdan RK (1999年9月). 「テトラヒドロカンナビノール側鎖の操作によるアゴニスト、部分アゴニスト、アンタゴニストの同定」J Pharmacol Exp Ther . 290 (3): 1065–79 . PMID 10454479.
- ^ abcd Howlett AC, Barth F, Bonner TI, Cabral G, Casellas P, Devane WA, Felder CC, Herkenham M, Mackie K, Martin BR, Mechoulam R, Pertwee RG (2002年6月). 「国際薬理学連合. XXVII. カンナビノイド受容体の分類」.薬理学レビュー. 54 (2): 161– 202. doi :10.1124/pr.54.2.161. PMID 12037135. S2CID 8259002.
- ^ abcdefghijklmnopqrstu vwxyz aa ab Huffman JW, Padgett LW, Isherwood ML, Wiley JL, Martin BR (2006年10月). 「1-アルキル-2-アリール-4-(1-ナフトイル)ピロール:カンナビノイドCB1およびCB2受容体に対する新規高親和性リガンド」. Bioorganic & Medicinal Chemistry Letters . 16 (20): 5432–5 . doi :10.1016/j.bmcl.2006.07.051. PMID 16889960.
- ^ abcdefghijklmnopqrstu vwxyz aa ab ac ad ae af ag ah ai aj ak al am Marriott KS, Huffman JW (2008). 「カンナビノイドCB(2)受容体に対する選択的リガンド開発における最近の進歩」Current Topics in Medicinal Chemistry . 8 (3): 187– 204. doi :10.2174/156802608783498014. PMID 18289088.
- ^ abcdefghijklmnopqrstu vwxyz aa Huffman JW, Szklennik PV, Almond A, Bushell K, Selley DE, He H, Cassidy MP, Wiley JL, Martin BR (2005年9月). 「1-ペンチル-3-フェニルアセチルインドール、新たなカンナビノイド模倣インドール類」. Bioorganic & Medicinal Chemistry Letters . 15 (18): 4110–3 . doi :10.1016/j.bmcl.2005.06.008. PMID 16005223.
- ^ Huffman JW, Bushell SM, Miller JR, Wiley JL, Martin BR (2002年12月). 「1-メトキシ-、1-デオキシ-11-ヒドロキシ-、および11-ヒドロキシ-1-メトキシ-デルタ(8)-テトラヒドロカンナビノール:CB2受容体に対する新規選択的リガンド」. Bioorganic & Medicinal Chemistry . 10 (12): 4119–29 . doi :10.1016/s0968-0896(02)00331-0. PMID 12413866.
- ^ abcdefg Wiley JL, Smith VJ, Chen J, Martin BR, Huffman JW (2012). 「1-アルキル-3-(1-ナフトイル)インドールの合成と薬理学:4-および8-ハロゲン化ナフトイル置換基の立体的および電子的効果」. Bioorganic & Medicinal Chemistry . 20 (6): 2067– 2081. doi :10.1016/j.bmc.2012.01.038. PMC 3298571. PMID 22341572 .
- ^ カンナビノイド受容体. 受容体. 2009. doi :10.1007/978-1-59745-503-9. ISBN 978-1-58829-712-9。