| |||
| 名前 | |||
|---|---|---|---|
| 推奨IUPAC名
シクロヘプタ-2,4,6-トリエン-1-オン | |||
| その他の名前
シクロヘプタ-2,4,6-トリエノン
| |||
| 識別子 | |||
3Dモデル(JSmol)
|
| ||
| ケムスパイダー | |||
| ECHA 情報カード | 100.007.933 | ||
PubChem CID
|
| ||
| ユニイ | |||
CompToxダッシュボード (EPA)
|
| ||
| |||
| |||
| プロパティ | |||
| C 7 H 6 O | |||
| モル質量 | 106.12 g/モル | ||
| 密度 | 1.094 g/mL | ||
| 沸点 | 113 °C (235 °F; 386 K) (15 mmHg) | ||
| 危険 | |||
| 引火点 | > 113 °C (235 °F; 386 K) | ||
特に記載がない限り、データは標準状態(25 °C [77 °F]、100 kPa)における材料のものです。
| |||
トロポン、または2,4,6-シクロヘプタトリエン-1-オンは、有機化学において非ベンゼン系芳香族化合物として重要な役割を果たす有機化合物である。[2]この化合物は、7つの炭素原子からなる環と、3つの共役アルケン基、および1つのケトン基から構成される。関連化合物であるトロポロン(2-ヒドロキシ-2,4,6-シクロヘプタトリエン-1-オン)は、ケトン基の隣りにアルコール基(または二重結合を含むエノール基)を有する。トロポンは天然物では稀であるが、2-ヒドロキシ誘導体はトロポロンと呼ばれる。
トロポンは1951年から知られており、シクロヘプタトリエニリウムオキシドとも呼ばれています。トロポロンという名称は、 1945年にMJSデュワーによって、その芳香特性に関連して造られました。[3]
プロパティ
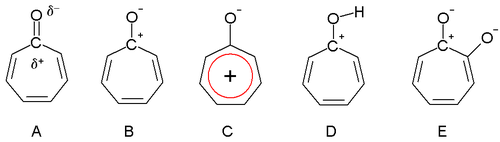
1945年、デュワーはトロポンが芳香族性を持つ可能性を提唱しました。カルボニル基はトリエン環によって分極度が増し、炭素原子に部分的な正電荷(A)を、酸素に部分的な負電荷を帯びます。極端な場合には、炭素原子は完全に正電荷を帯び(B)、芳香族6電子系 であるトロピリウムイオン環(C)を形成します。
トロポンは芳香族安定化の結果として塩基性(D)でもあります。この性質は、酸との塩形成の容易さに表れています。トロポンの双極子モーメントは4.17 Dであるのに対し、シクロヘプタノンはわずか3.04 Dです。この差は、双極子共鳴構造の安定化と整合しています。
合成
トロポンおよびその誘導体の有機合成法は数多く存在する。トロポンの合成法として特に注目されているのは、シクロヘプタトリエンの二酸化セレン 酸化による方法[4]と、トロピノンからホフマン脱離と臭素化による間接的な方法[2]である。
反応
トロポンは高温で水酸化カリウムと反応して環縮小を起こし、安息香酸となる。多くの誘導体も対応するアレーンに縮環する。[2]トロポンは、例えば臭素と反応して求電子置換反応を起こすが、この反応は1,2-付加生成物を経て進行し、求電子芳香族置換反応ではない。[2]
トロポン誘導体は求核置換反応でも求核芳香族置換反応と非常によく似た反応を起こす。[2]
トロポンは[8+3]環化でシナミルアルデヒドと反応することも発見されている[5]
ジエン文字
トロポンは、例えば無水マレイン酸とのディールス・アルダー反応においてジエンとして振舞う。[2] 同様に、鉄トリカルボニルとの付加物を形成し、これは(ブタジエン)鉄トリカルボニルに類似している。[6]
デリバティブ
| 名前 | 化学構造 | 天然資源 |
|---|---|---|
| トロポロン |  |
シュードモナス・リンドベルギ、シュードモナス・プランタリイ[7] |
| ヒノキチオール |  |
ヒノキ科の樹木[8] |
| スティピタチン酸 |  |
タラロミセス・スティピタトゥス[9] |
| トロポジチエティック酸 | 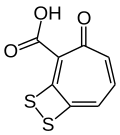 |
Phaeobacter piscinae、 Phaeobacter inhibens、 Phaeobacter gallaeciensis [10] [11] |
| コルヒチン |  |
コルチカム オータムナーレ、グロリオサ スーパーバ[12] |
その他のトロポン誘導体には、プベルロン酸、プベルリン酸、ロゼオバクチサイド、ペルナンブコン、クロトトロポン、オロバノンなどがある。[13] [14] [15] [16] [17]
参考文献
- ^ シグマアルドリッチのトロポン
- ^ abcdef ポーソン、ピーター L. (1955)。 「トロポネとトロポネ」。化学。 Rev. 55 (1): 9–136 . doi :10.1021/cr50001a002。
- ^ MJS Dewar (1945). 「スティピタチン酸の構造」. Nature . 155 (3924): 50– 51.書誌コード:1945Natur.155...50D. doi :10.1038/155050b0. S2CID 4086209.
- ^ ダーンケ、カール R.;パケット、レオ A. (1993)。「ケテン ジチオアセタールの逆電子要求ディールス アルダー付加環化。共役エノンの水素化銅促進還元。9-ジチオラノビシクロ[3.2.2]ノン-6-エン-2-オン」。組織シンセ。 71 : 181.土井:10.15227/orgsyn.071.0181。
- ^ ホモエノラートを介したトロポーネとエナルスの N-複素環カルベン触媒による [8 + 3] 環化Vijay Nair、Manojkumar Poonoth、Sreekumar Vellalath、Eringathodi Suresh、および Rajasekaran Thirumalai J. Org.化学。 ; 2006年; 71(23)、8964~8965ページ。 (注) doi :10.1021/jo0615706
- ^ Dodge, RP (1964). 「トロポン鉄トリカルボニルの結晶および分子構造」.アメリカ化学会誌. 86 (24): 5429– 5431. doi :10.1021/ja01078a013.
- ^ Liu, Na; Song, Wangze; Schienebeck, Casi M.; Zhang, Min; Tang, Weiping (2014年12月). 「天然トロポンおよびトロポロンの合成」. Tetrahedron . 70 (49): 9281– 9305. doi :10.1016/j.tet.2014.07.065. PMC 4228802. PMID 25400298 .
- ^ Saniewski, Marian; Horbowicz, Marcin; Kanlayanarat, Sirichai (2014年9月10日). 「トロポノイドの生物学的活性と農業におけるその利用に関するレビュー」. Journal of Horticultural Research . 22 (1): 5–19 . doi : 10.2478/johr-2014-0001 .
- ^ Davison, J.; al Fahad, A.; Cai, M.; Song, Z.; Yehia, SY; Lazarus, CM; Bailey, AM; Simpson, TJ; Cox, RJ (2012年5月15日). 「真菌トロポロン生合成の遺伝的、分子的、生化学的基盤」. Proceedings of the National Academy of Sciences . 109 (20): 7642– 7647. doi : 10.1073/pnas.1201469109 . PMC 3356636. PMID 22508998 .
- ^ Rabe, Patrick; Klapschinski, Tim A; Brock, Nelson L; Citron, Christian A; D'Alvise, Paul; Gram, Lone; Dickschat, Jeroen S (2014年8月6日). 「海洋抗生物質トロポジチエティック酸の類似体の合成と生物活性」Beilstein Journal of Organic Chemistry . 10 : 1796– 1801. doi : 10.3762/bjoc.10.188 . PMC 4142847. PMID 25161739 .
- ^ Beyersmann, Paul G.; Tomasch, Jürgen; Son, Kwangmin; Stocker, Roman; Göker, Markus; Wagner-Döbler, Irene; Simon, Meinhard; Brinkhoff, Thorsten (2017年12月). 「トロポジチエティック酸の抗生物質およびシグナル伝達分子としての二重機能によるプロバイオティクス細菌Phaeobacter inhibensの遺伝子発現制御」. Scientific Reports . 7 (1): 730. Bibcode :2017NatSR...7..730B. doi : 10.1038/s41598-017-00784-7 . PMC 5429656. PMID 28389641 .
- ^ Keith, Michael P.; Gilliland, William R.; Uhl, Kathleen (2009). 「痛風」.薬理学と治療学: 1039–1046 . doi :10.1016/B978-1-4160-3291-5.50079-2. ISBN 978-1-4160-3291-5。
- ^ Thiel, Verena; Brinkhoff, Thorsten; Dickschat, Jeroen S.; Wickel, Susanne; Grunenberg, Jörg; Wagner-Döbler, Irene; Simon, Meinhard; Schulz, Stefan (2009年12月10日). 「海洋性ロゼオバクター系統の細菌が産生するトロポン誘導体および硫黄揮発性物質の同定と生合成」. Organic & Biomolecular Chemistry . 8 (1): 234– 246. doi :10.1039/B909133E. PMID 20024154.
- ^ Duan, Ying; Petzold, Melanie; Saleem-Batcha, Raspudin; Teufel, Robin (2020年9月). 「細菌性トロポン天然物および誘導体:その生合成、生物活性、生態学的役割、およびバイオテクノロジー的可能性の概要」. ChemBioChem . 21 (17): 2384– 2407. doi : 10.1002/cbic.201900786 . PMC 7497051. PMID 32239689 .
- ^ Randau, KP; Sproll, S.; Lerche, H.; Bracher, F. (2009年5月1日). 「ペルナンブコン、クロトン・アルギログロスム由来の新規トロポン誘導体」. Die Pharmazie . 64 (5): 350– 351. doi :10.1691/ph.2009.7592. PMID 19530449.
- ^ ブラッハー、フランツ;ランダウ、カリーナ P.レルチェ、ホルガー (2008 年 4 月 1 日)。 「クロトン・ゼンネリからの新しいトロポン誘導体であるクロトトロポン」。フィトテラピア。79 (3): 236–237。土井:10.1016/j.fitote.2007.12.001。PMID 18321658。
- ^ フルチエ, アラン; ラスコル, ジャン=ピエール; アンダリー, クロード; プリヴァット, ガイ (1981年1月1日). 「オロバンシュ・ラプム・ジェニスタエ由来のトロポン誘導体」.植物化学. 20 (4): 777– 779. Bibcode :1981PChem..20..777F. doi :10.1016/0031-9422(81)85173-4.