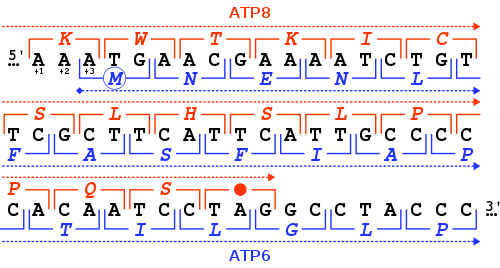
ヒトミトコンドリアゲノムにおけるMT-ATP8 遺伝子の位置。MT -ATP8 は、2つのATP合成酵素ミトコンドリア遺伝子(赤い枠)のうちの1つです。 ヒトミトコンドリア遺伝子MT-ATP8 とMT-ATP6 の読み枠における46ヌクレオチドの重複。各ヌクレオチドトリプレット(角括弧内)には、対応するアミノ酸が1文字コードで示されており、MT-ATP8 の場合は+1フレーム(赤)に、 MT-ATP6 の場合は+3フレーム(青)に示されています。MT-ATP8 ATP8 ミトコンドリア遺伝子 であり、フルネームは「ミトコンドリアによってコードされたATP合成酵素膜サブユニット8」であり、ミトコンドリアATP合成酵素のサブユニットである ATP合成酵素F o サブユニット8 (またはサブユニットA6L )をコードしています。このサブユニットは、大きな膜貫通型F型ATP合成酵素のF o 複合体に属しています。 [ 5 ] 複合体Vとしても知られるこの酵素は、電子伝達系 における酸化的リン酸化 の最終段階を担っています。具体的には、ATP合成酵素の1つのセグメントは、プロトン と呼ばれる正に帯電したイオンがミトコンドリア内の特殊な膜を通過できるようにします。酵素の別のセグメントは、このプロトンの流れによって生成されたエネルギーを使用して、 アデノシン二リン酸 (ADP)分子をATP に変換します。 [ 6 ] 後生動物 、植物 、真菌 の間で配列 が異なる。
構造 ヒトおよび他の哺乳類のATP合成酵素タンパク質8は、ミトコンドリアゲノム中の MT-ATP8 遺伝子 によってコードされている。ヒトミトコンドリアゲノムの完全版が初めて発表された際、MT-ATP8遺伝子は未同定の 読み枠 URF A6L[ 5 ] MT-ATP8 遺伝子の特異な特徴は、 MT-ATP6 -ATP8 の読み枠(+1)に対して、MT-ATP6 遺伝子は+3の読み枠から始まる。
MT-ATP8タンパク質は8 kDaで、68個のアミノ酸 から構成されています。[ 7 ] [ 8 ] 複合体V としても知られるF 1 F o ATPaseのサブユニットです。F型ATPaseは2つの構造ドメインから構成され、F 1 には膜外触媒コアが、F o には膜プロトンチャネルが含まれ、中心茎と周辺茎で結合しています。AサブユニットであるMT-ATP8は、複合体の非触媒膜貫通 F o 部分に含まれ、プロトンチャネル を構成しています。ミトコンドリアATP合成酵素の触媒部分は、5つの異なるサブユニット(α、β、γ、δ、ε)から構成され、αサブユニット3個、βサブユニット3個、および他の3つのサブユニットを代表する1個という化学量論で組み立てられています。プロトンチャネルは3つの主要サブユニット(a、b、c)で構成されています。この遺伝子は、触媒コアのδサブユニットをコードしています。同じアイソフォームをコードする選択的スプライシング転写バリアントが同定されています。[ 9 ] [ 6 ]
関数 MT-ATP8遺伝子は、 チラコイド膜 とミトコンドリア内膜 に位置するミトコンドリアATP合成酵素 のサブユニットをコードしています。ミトコンドリアATP合成酵素は、酸化的リン酸化反応 中に内膜を横切るプロトン の電気化学的勾配 を利用してATP合成を触媒します 。[ 9 ] o 領域は、ATPを加水分解する水溶性成分を持つF 1 の回転を引き起こし、F 1 F o と相まって膜を横切るプロトンの移動経路を形成します。[ 10 ]
このタンパク質サブユニットは、 酵母 ミトコンドリア F-ATPase の固定子柄の不可欠な構成要素であると考えられる。[ 11 ] 膜に固定されており、ATP合成と加水分解が共役している際に、回転子に対するATPaseサブユニットの無駄な回転を防ぐ役割を果たす。このサブユニットは、 後生動物 においても同様の機能を有する可能性がある。
命名法 この酵素の命名法に は長い歴史があります。F 1 画分は「Fraction 1」という用語に由来し、F o (下付き文字「o」で表記され、「ゼロ」ではありません)は、ATP合成酵素のF o ユニットを阻害する天然由来の抗生物質の一種であるオリゴマイシン の結合画分であることに由来します。[ 12 ] [ 13 ] o 領域は、ミトコンドリア膜に埋め込まれたプロトン孔です。A、B、Cの3つの主要サブユニットと、(ヒトでは)d 、e 、f 、g 、MT-ATP6 (またはF6)、MT-ATP8(またはA6L)の6つの追加サブユニットで構成されています。このサブユニットの大腸菌 ホモログの3D構造は、電子顕微鏡 データ(PDB : 1c17
臨床的意義 MT-ATP8 や、ミトコンドリアの酸化リン酸化 に影響を与える他の遺伝子の変異は、ミトコンドリア複合体 V 欠損症、レーバー遺伝性視神経症 (LHON)、脳卒中様発作を伴うミトコンドリア脳筋症 ( MELAS )、リー症候群 、NARP 症候群など、さまざまな 神経変性 疾患や心血管 疾患に関連付けられています。体の細胞のほとんどには、ミトコンドリア DNAのコピーを 1 つ以上持つ、数千個のミトコンドリアが含まれています。一部の ミトコンドリア疾患 の重症度は、各細胞内で特定の遺伝子変化があるミトコンドリアの割合に関連しています。MT -ATP6 遺伝子変異によるリー症候群 の患者は、変異のあるミトコンドリアの割合が非常に高い傾向があります (90% 以上から 95%)。NARP の軽度の症状は、ミトコンドリアにおける変異の割合が低いこと(通常70~90%)に起因します。これら2つの疾患は同じ遺伝子変異に起因し、同一家族内の異なる構成員に発症する可能性があるため、研究者らは、これらが2つの異なる症候群ではなく、重複する症状のスペクトルを表している可能性があると考えています。[ 6 ]
ミトコンドリア複合体V欠損症は、神経障害 、運動失調 、肥大型心筋症 など、多様な臨床症状を呈する。肥大型心筋症は、軽度から重度の肥大 、軽微から広範囲の線維 化および心筋細胞の 乱れ、左室流出路閉塞の有無にかかわらず重篤な心室中隔の輪郭・形態を呈し、臨床経過は極めて多岐にわたる。[ 14 ] [ 15 ]
ミトコンドリア複合体V欠損症は、電子伝達系 の複合体V の不足(欠損)または機能喪失であり、多くの臓器や系、特に神経系 と心臓 に影響を及ぼすさまざまな徴候や症状を 引き起こす可能性があります。この疾患は、乳児期または幼少期に生命を脅かす可能性があります。罹患した個人は、摂食障害、成長の遅れ、筋緊張の低下(低緊張 )、極度の疲労(嗜眠 )、発達の遅れを 示す場合があります。罹患した個人は、血中乳酸値の上昇( 乳酸アシドーシス )を発症する傾向があり、これは、吐き気、嘔吐、脱力感、および頻呼吸を引き起こす可能性があります。罹患した個人は血中アンモニア値の上昇( 高アンモニア血症 )も起こる可能性があり、場合によっては脳機能の異常(脳症 )や他の臓器の損傷につながります。[ 16 ] MT-ATP6のフレームシフト変異を持つ患者では、運動失調 、小頭症 、発達の遅れ、知的障害が観察されています。これにより、位置8612にC挿入が生じ、わずか36アミノ酸長の切断されたタンパク質が生成され、位置8610と8614に2つのT>C一塩基多型が 生じ、ホモポリマーシトシン ストレッチが生成されます。[ 17 ]
肥大型心筋症は 、ミトコンドリア複合体V欠損症の一般的な病態であり、心筋 の肥厚(肥大)を特徴とし、 心不全 につながる可能性があります。[ 16 ] スレオニン に、MT-ATP8の55番目のトリプトファンを アルギニン に変化させます。 [ 18 ] [ 15 ] 眼瞼裂)、突き出た鼻梁、低い位置にある耳、薄い唇、小さな顎(小 顎症 )など、特徴的な顔貌のパターンを示すこともあります。 [ 16 ]
乳児型肥大型心筋症(CMHI)も、 MT-ATP6 およびMT-ATP8を含む異なる遺伝子座の 変異によって引き起こされます。肥大型心筋症 の乳児型は、心室肥大 を特徴とする心疾患で、通常は非対称性で、しばしば心室中隔 が侵されます。症状には、呼吸困難 、失神 、虚脱、動悸 、胸痛 などがあります。運動によって容易に誘発される可能性があります。この疾患は、良性から悪性まで、家族内および家族間で変動があり、心不全 や突然死の リスクが高くなります。[ 14 ] [ 15 ]
参考文献 ^ a b c GRCh38: Ensemblリリース89: ENSG00000228253 – Ensembl 、2017年5月^ a b c GRCm38: Ensemblリリース89: ENSMUSG00000064356 – Ensembl 、2017年5月^ 「ヒトPubMedリファレンス:」 。米国国立医学図書館、国立生物工学情報センター 。^ 「マウスPubMedリファレンス:」 米国 国立医学図書館、国立生物工学情報センター 。 ^ a b Anderson S, Bankier AT, Barrell BG, de Bruijn MH, Coulson AR, Drouin J, Eperon IC, Nierlich DP, Roe BA, Sanger F, Schreier PH, Smith AJ, Staden R, Young IG (1981年4月). 「ヒトミトコンドリアゲノムの配列と構成」. Nature . 290 (5806): 457–65 . Bibcode : 1981Natur.290..457A . doi : 10.1038 / 290457a0 . PMID 7219534. S2CID 4355527 . ^ a b c 「MT-ATP8」 . Genetics Home Reference . NCBI. 2018年8月4日時点の オリジナル よりアーカイブ。 ^ Zong NC, Li H, Li H, Lam MP, Jimenez RC, Kim CS, Deng N, Kim AK, Choi JH, Zelaya I, Liem D, Meyer D, Odeberg J, Fang C, Lu HJ, Xu T, Weiss J, Duan H, Uhlen M, Yates JR, Apweiler R, Ge J, Hermjakob H, Ping P (2013年10月). 「専門的な知識 ベース による心臓プロテオーム生物学と医学の統合」 . Circulation Research . 113 (9): 1043–53 . doi : 10.1161/CIRCRESAHA.113.301151 . PMC 4076475. PMID 23965338 . ^ 「ATP合成酵素タンパク質8」 。 心臓オルガネラタンパク質アトラス知識ベース(COPaKB) 。 ^ a b 「MT-ATP8 ミトコンドリアにコードされたATP合成酵素8 [ホモ・サピエンス (ヒト)]」 Gene NCBI . ^ Velours J, Paumard P, Soubannier V, Spannagel C, Vaillier J, Arselin G, Graves PV (2000年5月). 「酵母ATP合成酵素F(0)の組織化:システイン変異体、チオール修飾、架橋試薬に基づく研究」. Biochimica et Biophysica Acta (BBA) - Bioenergetics . 1458 ( 2–3 ): 443–56 . doi : 10.1016/S0005-2728(00)00093-1 . PMID 10838057 . ^ Stephens AN, Khan MA, Roucou X, Nagley P, Devenish RJ (2003年5月). 「システインスキャン法と化学修飾による酵母ミトコンドリアF1F0-ATP合成酵素サブユニット8の分子近傍領域の解析」 . The Journal of Biological Chemistry . 278 (20): 17867–75 . doi : 10.1074/jbc.M300967200 . PMID 12626501 . ^ Kagawa Y, Racker E (1966年5月). 「酸化的リン酸化を触媒する酵素の部分分解。8. ミトコンドリアアデノシントリホスファターゼにオリゴマイシン感受性を付与する因子の特性」 . The Journal of Biological Chemistry . 241 (10): 2461–6 . doi : 10.1016/S0021-9258(18)96640-8 . PMID 4223640 . ^ Mccarty RE (1992年11月). 「植物生化学者によるH+-ATPaseとATP合成酵素の視点」 . The Journal of Experimental Biology . 172 (Pt 1): 431– 441. doi : 10.1242/jeb.172.1.431 . PMID 9874753 . ^ a b 「MT-ATP8 - ATP合成酵素タンパク質8 - Homo sapiens (ヒト)」 www.uniprot.org . UniProt . 2018年 8月3日 閲覧 。 この記事には、CC BY 4.0 ライセンス に基づいて利用可能なテキストが組み込まれています。^ a b c Ware SM, El-Hassan N, Kahler SG, Zhang Q, Ma YW, Miller E, Wong B, Spicer RL, Craigen WJ, Kozel BA, Grange DK, Wong LJ (2009年5月). 「ミトコンドリアATPase 6遺伝子と8遺伝子の重複領域の変異によって引き起こされる乳児心筋症」. Journal of Medical Genetics . 46 (5): 308–14 . doi : 10.1136 / jmg.2008.063149 . PMID 19188198. S2CID 25354118 . ^ a b c 「ミトコンドリア複合体V欠損症」 Genetics Home Reference . NCBI . 2018年 8月3日 閲覧 。 この記事には、パブリック ドメイン であるこのソースからのテキストが組み込まれています。^ Jackson CB, Hahn D, Schröter B, Richter U, Battersby BJ, Schmitt-Mechelke T, Marttinen P, Nuoffer JM, Schaller A (2017年6月). 「複合体V欠損症、運動失調症、および脳筋症を引き起こす新たなミトコンドリアATP6フレームシフト変異」. European Journal of Medical Genetics . 60 (6): 345– 351. doi : 10.1016/j.ejmg.2017.04.006 . hdl : 10138/237062 . PMID 28412374 . ^ 今井 明、藤田 聡、木下 雄三、幸田 正之、徳澤 勇、平田 剛、水野 雄三、原島 秀、中谷 明、坂田 雄三、武田 明、森 正治、村山 功、大竹 明、岡崎 雄三 (2016年3月). 「ATPase 6および8タンパク質の欠損によるミトコンドリア呼吸鎖複合体V欠損を伴う急速進行性乳児心筋症」. International Journal of Cardiology . 207 : 203–5 . doi : 10.1016/j.ijcard.2016.01.026 . PMID 26803244 .
さらに読む Torroni A, Achilli A, Macaulay V, Richards M, Bandelt HJ (2006年6月). 「ヒトmtDNAツリーの果実を収穫する」. Trends in Genetics . 22 (6): 339–45 . doi : 10.1016/j.tig.2006.04.001 . PMID 16678300 . Bodenteich A, Mitchell LG, Polymeropoulos MH, Merril CR (1992年5月). 「ヒトミトコンドリアDループにおけるジヌクレオチドリピート」. Human Molecular Genetics . 1 (2): 140. doi : 10.1093/hmg/1.2.140-a . PMID 1301157 . Lu X, Walker T, MacManus JP, Seligy VL (1992年7月). 「HT-29ヒト結腸腺癌細胞の分化はミトコンドリアRNAの発現増加と相関する:トレハロースの細胞増殖および成熟への影響」. Cancer Research . 52 (13): 3718–25 . PMID 1377597 . Marzuki S, Noer AS, Lertrit P, Thyagarajan D, Kapsa R, Utthanaphol P, Byrne E (1991年12月). 「ヒトミトコンドリアDNAおよび翻訳産物の正常変異:参照データベースの構築」. Human Genetics . 88 (2): 139–45 . doi : 10.1007/bf00206061 . PMID 1757091. S2CID 28048453 . Moraes CT, Andreetta F, Bonilla E, Shanske S, DiMauro S, Schon EA (1991年3月). 「重鎖プロモーター領域を欠く複製能のあるヒトミトコンドリアDNA」 . Molecular and Cellular Biology . 11 (3): 1631–7 . doi : 10.1128/MCB.11.3.1631 . PMC 369459. PMID 1996112 . Attardi G, Chomyn A, Doolittle RF, Mariottini P, Ragan CI (1987). 「ヒトミトコンドリアDNAの7つの未同定リーディングフレームは呼吸鎖NADH脱水素酵素のサブユニットをコードする」Cold Spring Harbor Symposia on Quantitative Biology . 51 Pt 1 (1): 103–14 . doi : 10.1101/sqb.1986.051.01.013 . PMID 3472707 . Chomyn A, Cleeter MW, Ragan CI, Riley M, Doolittle RF, Attardi G (1986年10月). 「URF6、ヒトmtDNAの最後の未同定リーディングフレームはNADH脱水素酵素サブユニットをコードする」. Science . 234 (4776): 614–8 . Bibcode : 1986Sci...234..614C . doi : 10.1126/science.3764430 . PMID 3764430 . Chomyn A, Mariottini P, Cleeter MW, Ragan CI, Matsuno-Yagi A, Hatefi Y, Doolittle RF, Attardi G (1985). 「ヒトミトコンドリアDNAの6つの未同定リーディングフレームは呼吸鎖NADH脱水素酵素の構成要素をコードする」Nature . 314 ( 6012): 592–7 . Bibcode : 1985Natur.314..592C . doi : 10.1038/314592a0 . PMID 3921850. S2CID 32964006 . Anderson S, Bankier AT, Barrell BG, de Bruijn MH, Coulson AR, Drouin J, Eperon IC, Nierlich DP, Roe BA, Sanger F, Schreier PH, Smith AJ, Staden R, Young IG (1981年4月). 「ヒトミトコンドリアゲノムの配列と構成」. Nature . 290 ( 5806): 457–65 . Bibcode : 1981Natur.290..457A . doi : 10.1038/290457a0 . PMID 7219534. S2CID 4355527 . Montoya J, Ojala D, Attardi G (1981年4月). 「ヒトミトコンドリアmRNAの5'末端配列の特徴」. Nature . 290 ( 5806): 465–70 . Bibcode : 1981Natur.290..465M . doi : 10.1038/290465a0 . PMID 7219535. S2CID 4358928 . 宝来 誠・早坂 功・近藤 亮・津金 功・高畑 暢 (1995年1月). 「ヒト科ミトコンドリアDNAの完全配列によって明らかになった現代人の最近のアフリカ起源」 . 米国科学アカデミー紀要 . 92 (2): 532–6 . Bibcode : 1995PNAS...92..532H . doi : 10.1073/pnas.92.2.532 PMC 42775. PMID 7530363 . Rieder MJ, Taylor SL, Tobe VO, Nickerson DA (1998年2月). 「品質ベースの蛍光再配列法を用いたDNA変異同定の自動化:ヒトミトコンドリアゲノムの解析」 . Nucleic Acids Research . 26 (4): 967–73 . doi : 10.1093 / nar/26.4.967 . PMC 147367. PMID 9461455 . Andrews RM, Kubacka I, Chinnery PF, Lightowlers RN, Turnbull DM, Howell N (1999年10月). 「ヒトミトコンドリアDNAのケンブリッジ参照配列の再解析と改訂」 . Nature Genetics . 23 (2): 147. doi : 10.1038/13779 PMID 10508508. S2CID 32212178 . Ingman M, Kaessmann H, Pääbo S, Gyllensten U (2000年12月). 「ミトコンドリアゲノム変異と現代人の起源」. Nature . 408 ( 6813): 708–13 . Bibcode : 2000Natur.408..708I . doi : 10.1038/35047064 . PMID 11130070. S2CID 52850476 . Finnilä S、Lehtonen MS、Majamaa K (2001 年 6 月)。「ヨーロッパの mtDNA の系統発生ネットワーク」 。アメリカ人類遺伝学ジャーナル 。68 (6): 1475–84 .土井 : 10.1086/320591 。PMC 1226134 PMID 11349229 。 Maca-Meyer N, González AM, Larruga JM, Flores C, Cabrera VM (2003). 「主要なゲノムミトコンドリア系統が初期人類の進化を描写する」 . BMC Genetics . 2 : 13. doi : 10.1186/1471-2156-2-13 PMC 55343. PMID 11553319 . Herrnstadt C, Elson JL, Fahy E, Preston G, Turnbull DM, Anderson C, Ghosh SS, Olefsky JM, Beal MF, Davis RE, Howell N (2002年5月). 「主要なアフリカ、アジア、ヨーロッパのハプログループにおけるミトコンドリアDNAコード領域配列の縮小中央値ネットワーク解析」 . American Journal of Human Genetics . 70 (5): 1152–71 . doi : 10.1086/339933 . PMC 447592. 11938495 . シウバ WA、ボナット SL、ホランダ AJ、リベイロ - ドス - サントス AK、パイシャン BM、ゴールドマン GH、アベ - サンデス K、ロドリゲス - デルフィン L、バルボサ M、パソ - ラーソン ML、ペツル - エルラー ML、バレンテ V、サントス SE、ザーゴ MA (2002 年 7 月)。「アメリカ先住民のミトコンドリアゲノムの多様性は、創始者集団のアメリカへの単一の早期侵入を裏付けています 。 」アメリカ人類遺伝学ジャーナル 。71 (1): 187–92 .土井 : 10.1086/341358 。PMC 384978 PMID 12022039 。 Mishmar D, Ruiz-Pesini E, Golik P, Macaulay V, Clark AG, Hosseini S, Brandon M, Easley K, Chen E, Brown MD, Sukernik RI, Olckers A, Wallace DC (2003年1月). 「自然選択がヒトにおけるmtDNAの地域的変異を形作った」 .米国科学アカデミー紀要 . 100 (1): 171–6 . Bibcode : 2003PNAS..100..171M . doi : 10.1073/pnas.0136972100 PMC 140917. PMID 12509511 . Ingman M, Gyllensten U (2003年7月). 「オーストラリアおよびニューギニア先住民のミトコンドリアゲノム変異と進化史」 .ゲノム研究 . 13 (7): 1600–6 . doi : 10.1101/gr.686603 . PMC 403733. PMID 12840039 . この記事には、パブリック ドメイン である米国国立医学図書館 のテキストが組み込まれています。

 この記事には、CC BY 4.0ライセンス に基づいて利用可能なテキストが組み込まれています。
この記事には、CC BY 4.0ライセンス に基づいて利用可能なテキストが組み込まれています。 この記事には、パブリック ドメインであるこのソースからのテキストが組み込まれています。
この記事には、パブリック ドメインであるこのソースからのテキストが組み込まれています。

