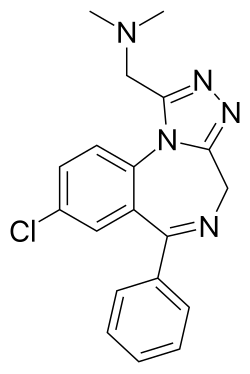
アディナゾラム
 | |
 | |
| 臨床データ | |
|---|---|
| 商号 | デラシン |
| 投与経路 | オーラル |
| ATCコード | |
| 法的地位 | |
| 法的地位 | |
| 薬物動態データ | |
| 代謝 | 肝臓 |
| 代謝物 |
|
| 消失半減期 | 3時間未満 |
| 排泄 | 腎臓 |
| 識別子 | |
| |
| CAS番号 |
|
| PubChem CID | |
| ドラッグバンク |
|
| ケムスパイダー |
|
| ユニイ | |
| ケッグ |
|
| チェビ |
|
| チェムブル |
|
| CompToxダッシュボード(EPA) | |
| 化学および物理データ | |
| 式 | C19H18ClN5 |
| モル質量 | 351.84 g·mol −1 |
| 3Dモデル(JSmol) | |
| 融点 | 171~172.5℃(339.8~342.5℉) |
| 水への溶解度 | LogP: 4.16 ジクロロメタンおよびメタノールに可溶 塩(メシル酸塩)水に溶ける量 mg/mL(20℃) |
| |
| |
| (確認する) | |
アディナゾラム[ 1 ](商品名:デラシン)は、トリアゾール環が縮合したベンゾジアゼピン(BZD)であるトリアゾロベンゾジアゼピン(TBZD)系の精神安定剤です。抗不安作用、[ 2 ]抗けいれん作用、鎮静作用、抗うつ作用[ 3 ] [ 4 ]を有します。アディナゾラムは、自身が開発したアルプラゾラムの抗うつ作用を強化することを目指していたジャクソン・B・ヘスターによって開発されました。 [ 5 ]アディナゾラムはFDAの承認を受けておらず、一般市場に流通したこともありませんが、デザイナードラッグとして販売されています。[ 6 ]
用途と目的
アジナゾラムは主に抗不安作用を目的として使用されます。序論で述べたように、また分子作用機序でさらに詳しく説明するように、アジナゾラムはベンゾジアゼピン誘導体であり、中枢神経系のGABA受容体に作用し、GABAの抑制作用を促進します。その結果、鎮静効果が得られるため、不安障害、パニック障害、抗うつ薬として使用されます。[ 7 ]
Amsterdamら[ 8 ]の論文では、大うつ病の研究診断基準(RDC)を満たす外来患者43名を対象に研究が行われました。患者はアジナゾラムまたはイミプラミンのいずれかに無作為に割り付けられました。薬剤の投与量は忍容性と必要性に基づいて調整され、毎週、様々な尺度を用いて臨床評価と評価が行われました。
アジナゾラムは大うつ病の治療においてイミプラミンと同等の有効性を示し、メランコリー型うつ病においても同様の有効性を示した。アジナゾラムには、眠気/鎮静、口渇、便秘、かすみ目、吐き気/嘔吐/下痢、神経過敏、頭痛などの副作用があった。しかし、眠気/鎮静を除く全ての副作用はイミプラミンよりも少なかった。本研究は、アジナゾラムが治療効果の高い有望な代替薬となる可能性を示唆しているが、その臨床プロファイルと安全性を明らかにするにはさらなる研究が必要である。
可用性
アディナゾラムは1980年代から1990年代にかけて抗うつ薬として開発・試験されましたが、初期の評価期間を過ぎると研究と試験は減少しました。その薬理学的特性に関する更なる研究に関する情報は限られています。1990年代にFDAがアディナゾラムを却下したため、主流の医療用途からは姿を消しました。
この拒絶反応の後、アディナゾラムは2015年頃に再登場し、デザイナードラッグとして市場に流通しました。この地位と機能の変化は、医療用途以外でのアディナゾラムの適用について疑問を投げかけています。デザイナードラッグは、化学組成が改変されていることや乱用されやすいことから、規制当局にとってしばしば課題となっています。
副作用
アジナゾラムを使用すると、短期的にも長期的にも様々な副作用が現れることがあります。初期段階では、短期的な副作用として、眠気、鎮静、軽度認知障害などが挙げられます。[ 8 ] [ 9 ]
過剰摂取では、筋力低下、運動失調、構音障害、特に子供では逆説的な興奮が起こる可能性があり、さらに重篤な場合には反射神経の低下、混乱、昏睡が起こることもあります。 [ 10 ]
アジナゾラム(30mgと50mg)の主観的効果と乱用可能性をジアゼパム、ロラゼパム、プラセボと比較したヒト研究では、アジナゾラムが最も「精神的および肉体的鎮静」と最も大きな「精神的不快感」を引き起こすことが示されました。[ 11 ]
アジナゾラムを長期使用すると、耐性が生じ、同じ治療効果を得るためにより高い用量が必要になる可能性があります。その結果、用量を増やすと副作用や合併症のリスクが高まる可能性があります。また、アジナゾラムを長期使用すると依存症になる可能性があり、不安症状を管理するために精神的にも身体的にも薬剤に依存するようになる可能性があります。[ 12 ] [ 13 ]依存症は重大な問題を引き起こします。急激な減量は、反跳性不安や不眠症から発作などのより重篤な症状に至るまで、離脱症状を引き起こす可能性があります。さらに、アジナゾラムの長期使用は認知障害の一因となり、記憶力、集中力、そして全体的な認知機能に影響を与える可能性があります。[ 14 ] [ 9 ]
薬力学と薬物動態学
アジナゾラムは、ヒトの主な活性代謝物である代謝物N-デメチルアジナゾラム(NDMAD)のプロドラッグである。 [ 15 ]しかし、アジナゾラムとその他の代謝物であるジ-N-デメチルアジナゾラム、⍺-ヒドロキシ-アルプラゾラム、エストラゾラムは、それ自体が活性化合物である。[ 15 ]これらは、GABA A受容体のサブセットである(中枢)ベンゾジアゼピン受容体(BzR)に正のアロステリックに結合することにより、中枢神経系(CNS)に作用する。[ 7 ] [ 16 ] [ 17 ]アジナゾラムは GABA A受容体に対して高い親和性を有するが、その代謝物は [ 3H ]フルニトラゼパム(放射性標識を使用)の結合を 20~40 倍阻害する力が強い。[ 15 ]
(GABA) A受容体は、脳内の主要な抑制性神経伝達物質であり、ニューロンの活動を調整する上で重要な役割を果たしているγ-アミノ酪酸(GABA)の放出に反応します。[ 7 ] GABAA受容体はシナプスに位置するタンパク質複合体です。このタンパク質は、神経細胞膜を介して塩化物イオンを伝導するリガンド依存性イオンチャネル(イオンチャネル型受容体)です。[ 7 ]この複合体は、2つの⍺、2つのβ、および1つのγの5つのサブユニットで構成されています。 GABAは⍺サブユニットとβサブユニットの界面(2つの結合部位)に結合しますが、ベンゾジアゼピンは⍺サブユニットとγサブユニットの界面に結合します。しかし、ベンゾジアゼピンの結合は、ベンゾジアゼピン受容体と呼ばれる⍺ 1、⍺ 2、⍺ 3 、および⍺ 5の⍺の種類にヒスチジン残基がある場合にのみ可能です。 [ 7 ] [ 18 ]アジナゾラムまたは他のベンゾジアゼピンの結合は、ベンゾジアゼピン受容体の構造変化を誘発することでアゴニストとして作用し、GABAへの親和性を高め、今度は神経活動を低下させます。この神経活動の低下が、観察される臨床効果を説明しています。ベンゾジアゼピンの異なる薬理学的特性は、⍺サブユニットの多様性に起因すると考えられます。 ⍺ 1サブユニットは鎮静作用、順行性健忘作用、抗けいれん作用に必要であり、抗不安作用と筋弛緩作用に必要な⍺ 2サブユニットは、⍺ 2、⍺ 3、および⍺ 5サブユニットを含むGABAA受容体によって媒介される。[ 18 ]
ニューロンの発火は、安静時には負である膜電位が閾値(活動電位)に達するまで増加(脱分極)したときに起こります。この電位に達すると、電位依存性ナトリウムチャネルが開き、ナトリウムが細胞内に流入します。GABAがGABA-A受容体に結合すると、塩化物イオンが細胞内に流入し、膜電位を低下(分極)させることで、この流入が抑制されます。[ 19 ] [ 20 ]アジナゾラムなどのベンゾジアゼピン系薬剤の結合は塩化物イオンの流入を増加させ、膜電位の分極を増加させます。[ 7 ] [ 16 ] [ 17 ]
化学情報
反応性
アジナゾラムは、その構造中に複数の反応性部位を有する。第一にジメチルアミンはpKaが6.30と弱塩基性であり、生理的pH下では化合物の5%以上がプロトン化する。第三級アミンは、水素結合を形成する能力を有することからタンパク質結合において重要な役割を果たす可能性があり、脱メチル化による代謝の標的となる可能性も高い。ジメチルアミンは酸化分解に対しても不安定であり、その結果、メチル基が1つ失われてN-デスメチルアジナゾラムが形成される。ジメチルメタナミン全体が酸化分解によって失われ、エスタゾラムが形成される可能性もある。第二の反応性基は4位の窒素である。pKaは5.09であり、生理的pHよりも低いpHレベルでのみプロトン化される。プロトン化後、この基は水和に対して不安定であり、ジアゼピン環が開環する。その後、エチルアミンが開裂するか、環が再び閉じられ、他の構造となる。
合成
アジナゾラムを合成する論理的な方法の一つは、ベンゾジアゼピン前駆体を反応させることです。ヘスターらが採用した経路の一つは、 7-クロロ-2-ヒドラジニル-5-フェニル-3H-ベンゾ[e][1,4]ジアゼピンを出発原料としています。まず、 β-アラニンと無水フタル酸からN-フタルイミドイル-β-アラニンをin situで生成します。この溶液を冷却し、カルボニルジイミダゾールで処理します。次に、7-クロロ-2-ヒドラジニル-5-フェニル-3H-ベンゾ[e][1,4]ジアゼピンをこの溶液に加え、室温で18時間反応させます。この手順の後、酢酸エチル溶媒和物を作り、2-(2-(8-クロロ-6-フェニル-4H-ベンゾ[f][1,2,4]トリアゾロ[4,3-a][1,4]ジアゼピン-1-イル)エチル)イソインドリン-1,3-ジオンを得た。続いて、2-(2-(8-クロロ-6-フェニル-4H-ベンゾ[f][1,2,4]トリアゾロ[4,3-a][1,4]ジアゼピン-1-イル)エチル)イソインドリン-1,3-ジオンを88%ギ酸および37%水酸化ナトリウム水溶液で処理した。ホルムアルデヒド(3.2 mol/mol)を窒素雰囲気下、100 °Cで1時間反応させると、2-(2-(4-(2-ベンゾイル-4-クロロフェニル)-5-(ジメチルアミノ)メチル)-4H-1,2,4-トリアゾール-3-イル)エチル)イソインドリン-1,3-ジオンが生成した。この段階でジアゼピン環が切断され、フタル酸エステルが転移する。最後の段階では、ヒドラジン水和物を用いて窒素雰囲気下、70 °Cで1時間30分反応させることでジアゼピン環が再形成され、アジナゾラムが生成される。[ 21 ]
アジナゾラムを合成する別の方法として、Gallらが行ったエスタゾラムを経由する方法があります。この合成法では、ビス(ジメチルアミノ)メタンをDMFに溶解し、0℃まで冷却します。次に、この溶液をDMF中の塩化アセチルで処理し、ジメチル(メチレン)アンモニウムクロリド塩を形成します。次に、この溶液にK 2 CO 3を加え、続いてエスタゾラムのDMF溶液を加えます。この混合物を60℃で3時間加熱し、後処理を経てアジナゾラムが得られます。[ 22 ]
代謝
アジナゾラムは、1984年8月発行のThe Journal of Pharmacy and Pharmacologyで活性代謝物があると報告された。[ 15 ]主な代謝物はN-デスメチルアジナゾラムである。[ 23 ] NDMADは、その前駆体と比較してベンゾジアゼピン受容体に対する親和性が約25倍高く、経口投与後にベンゾジアゼピン様効果を示す。[ 1 ]複数のN-脱アルキル化によりジメチルアミノメチル側鎖が除去され、その効力に差が生じる。[ 23 ]他の2つの代謝物は、α-ヒドロキシアルプラゾラムとエスタゾラムである。[24] 同誌1986年8月号で、Sethy、Francis、およびDayは、プロアディフェンがN-デスメチルアジナゾラムの形成を阻害することを報告した。[ 25 ]
アディナゾラムは摂取後、主に肝経路および腸管経路によるN-脱アルキル化によって代謝されます。アディナゾラムはCYP3A4の基質であるため、経口摂取後、腸管および肝臓で活性代謝物に変換される可能性があります。ただし、腸管代謝は肝代謝よりも先に重要な役割を果たします。CYP3A4は腸管および肝臓に存在する酵素であり、薬物代謝において重要な役割を果たします。したがって、アディナゾラムの腸管代謝経路の研究は、この物質の薬理学全体を理解する上で重要です。[ 2 ] [ 6 ] [ 24 ] [ 26 ]
いくつかの研究によると、アジナゾラムの主な代謝物は、CYP3A4などのシトクロムP450酵素によって触媒される酸化反応を伴う第1相代謝物としても知られ、モノ- N -デスメチルアジナゾラム(活性代謝物)と(N、N -ジ)デスメチルアジナゾラムです。モノ- N -デスメチルアジナゾラムは、窒素に結合したメチル基がN脱アルキル化によって除去されるアジナゾラムの変換によって生成され、この活性代謝物はさらにデスメチルアジナゾラムに代謝され、別のメチル基が除去されて水素原子に置き換えられます。デスメチルアジナゾラムの脱アミノ化により中間代謝物が生成され、これがα-ヒドロキシ化されてα-ヒドロキシ-アルプラゾラムになるか、または側鎖が切断されてエスタゾラムになりますが、これらは微量代謝物です。[ 2 ] [ 24 ] [ 26 ] [ 27 ] [ 6 ] [ 15 ] [ 28 ]アディナゾラムとその代謝物の代謝。
参照
参考文献
- ^ a b FR 2248050、「4,5-ジヒドロ-4h-s-トリアゾロ(4,3-a)(1,4)ベンゾジアゼピン - 中枢神経抑制剤、抗けいれん剤、抗攻撃剤および体性反射」、1977年1月21日発行、Ciba-Geigy AGおよびNovartis AGに譲渡。
- ^ a b c Venkatakrishnan K, von Moltke LL, Duan SX, Fleishaker JC, Shader RI, Greenblatt DJ (1998年3月). 「ヒトにおけるアジナゾラムおよびN-デスメチルアジナゾラムの肝臓における生体内変換に関与する酵素の速度論的特徴づけと同定」 . The Journal of Pharmacy and Pharmacology . 50 (3 ) : 265– 274. doi : 10.1111/j.2042-7158.1998.tb06859.x . PMID 9600717. S2CID 33656240 .
- ^ Dunner D, Myers J, Khan A, Avery D, Ishiki D, Pyke R (1987年6月). 「アディナゾラム ― 新しい抗うつ薬:大うつ病外来患者を対象としたプラセボ対照二重盲検試験の結果」. Journal of Clinical Psychopharmacology . 7 (3): 170– 172. doi : 10.1097/00004714-198706000-00010 . PMID 3298327 .
- ^ Lahti RA, Sethy VH, Barsuhn C, Hester JB (1983年11月). 「抗うつ薬アジナゾラム(トリアゾロベンゾジアゼピン系薬剤)の薬理学的プロファイル」. Neuropharmacology . 22 (11): 1277– 1282. doi : 10.1016/0028-3908(83)90200-9 . PMID 6320036. S2CID 667962 .
- ^ 「Discovers Award 2004」(PDF) . Special Publications . Pharmaceutical Research and Manufacturers of America. 2004年4月. p. 39. 2006年8月24日時点のオリジナル(PDF)からアーカイブ。 2006年8月18日閲覧。
- ^ a b c Moosmann B, Bisel P, Franz F, Huppertz LM, Auwärter V (2016年11月). 「デザイナーベンゾジアゼピンの特性評価とin vitro第I相ミクロソーム代謝 - アディナゾラム、クロニプラゼパム、フォナゼパム、3-ヒドロキシフェナゼパム、メチゾラム、ニトラゾラムを含む最新情報」. Journal of Mass Spectrometry . 51 (11): 1080– 1089. Bibcode : 2016JMSp...51.1080M . doi : 10.1002/jms.3840 . PMID 27535017 .
- ^ a b c d e f Seeman P (2009年3月). 「統合失調症におけるグルタミン酸とドーパミンの成分」 . Journal of Psychiatry & Neuroscience . 34 (2): 143– 149. doi : 10.4103/0973-1229.58825 (2025年7月16日停止). PMC 3043325 .
{{cite journal}}: CS1 maint: DOIは2025年7月時点で非アクティブです(リンク) - ^ a b Amsterdam JD, Kaplan M, Potter L, Bloom L, Rickels K (1986年4月). 「大うつ病性障害の治療における新規トリアゾロベンゾジアゼピン系薬剤アディナゾラムとイミプラミン」Psychopharmacology . 88 (4): 484– 488. doi : 10.1007/BF00178511 . PMID 3085137 .
- ^ a b Linnoila M, Stapleton JM, Lister R, Moss H, Lane E, Granger A, et al. (1990年4月). 「アディナゾラムとジアゼパム単独およびエタノールとの併用による、健常者における精神運動機能および認知機能、ならびに自律神経系反応性への影響」. European Journal of Clinical Pharmacology . 38 (4): 371– 377. doi : 10.1007/BF00315578 . PMID 2344860 .
- ^ 「アディナゾラム」。DrugBank。
- ^ Bird M, Katz D, Orzack M, Friedman L, Dessain E, Beake B, et al. (1987). 「アディナゾラムの乱用可能性:ジアゼパム、ロラゼパム、プラセボとの比較」(PDF) . NIDA研究モノグラフ No. 81. 2016年12月22日時点のオリジナル(PDF)からアーカイブ。 2015年12月17日閲覧。
- ^ Brunetti P, Giorgetti R, Tagliabracci A, Huestis MA, Busardò FP (2021年6月). 「デザイナーベンゾジアゼピン:毒性学と公衆衛生リスクのレビュー」 . Pharmaceuticals . 14 ( 6): 560. doi : 10.3390/ph14060560 . PMC 8230725. PMID 34208284 .
- ^ Owen RT, Tyrer P (1983年4月). 「ベンゾジアゼピン依存症。エビデンスのレビュー」. Drugs . 25 (4): 385– 398. doi : 10.2165/00003495-198325040-00003 . PMID 6133736 .
- ^ Stewart SA (2005). 「ベンゾジアゼピンの認知機能への影響」.臨床精神医学ジャーナル. 66 (Suppl 2): 9– 13. PMID 15762814 .
- ^ a b c d e Sethy VH, Collins RJ, Daniels EG (1984年8月). 「アディナゾラムとその代謝物の生物学的活性の測定」. The Journal of Pharmacy and Pharmacology . 36 (8): 546– 548. doi : 10.1111/j.2042-7158.1984.tb04449.x . PMID 6148400. S2CID 21094654 .
- ^ a b Tamama K, Lynch MJ (2019). 「新たに出現した乱用薬物」. Nader MA, Hurd YL (編).物質使用障害. 実験薬理学ハンドブック. 第258巻. 出版社: Springer International Publishing. pp. 463– 502. doi : 10.1007/164_2019_260 . ISBN 978-3-030-33678-3. PMID 31595417 .
- ^ a b Hayhoe B, Lee-Davey J (2018年7月). 「ベンゾジアゼピン乱用への取り組み」 . BMJ . 362 k3208. doi : 10.1136/bmj.k3208 . PMC 6065205. PMID 30054270 .
- ^ a b Tan KR, Rudolph U, Lüscher C (2011年4月). 「ベンゾジアゼピン中毒:GABAA受容体サブタイプと依存症」 . Trends in Neurosciences . 34 (4): 188– 197. doi : 10.1016 / j.tins.2011.01.004 . PMC 4020178. PMID 21353710 .
- ^ベン・アリ Y、カジポフ R、ライネクーゲル X、カイヤール O、ガイアルサ JL (1997 年 11 月)。 「GABAA、NMDA、AMPA 受容体:発達的に調節される「トロワの精神」「神経科学の動向. 20 (11): 523– 529. doi : 10.1016/S0166-2236(97)01147-8 . PMID 9364667 .
- ^武藤 正之、吉岡 毅(2000年3月). 「ラット海馬におけるGABA(A)受容体を介した電流の発達的変化」.神経科学. 96 (3): 507– 514. doi : 10.1016/s0306-4522(99)00574-6 . PMID 10717431 .
- ^ Hester JB, Rudzik AD, VonVoigtlander PF (1980年4月). 「抗不安作用および抗うつ作用を有する1-(アミノアルキル)-6-アリール-4-Hs-トリアゾロ[4,3-a][1,4]ベンゾジアゼピン」. Journal of Medicinal Chemistry . 23 (4): 392– 402. doi : 10.1021/jm00178a009 . PMID 6103958 .
- ^ Gall M, Kamdar BV, Lipton MF, Chidester CG, Duchamp DJ (1988年11月). 「ジメチル(メチレン)アンモニウムクロリドによる複素環化合物のマンニッヒ反応:エスタゾラムからアジナゾラムへの高収率ワンステップ変換」 . Journal of Heterocyclic Chemistry . 25 (6): 1649– 1661. doi : 10.1002/jhet.5570250610 . ISSN 0022-152X .
- ^ a b Peng GW (1984年8月). 「液体クロマトグラフィーによる血漿中アディナゾラムの測定」. Journal of Pharmaceutical Sciences . 73 (8): 1173– 1175. Bibcode : 1984JPhmS..73.1173P . doi : 10.1002/jps.2600730840 . PMID 6491930 .
- ^ a b c Fraser AD, Isner AF, Bryan W (1993年11月~12月). 「Emit dau法およびFPIAベンゾジアゼピン法による尿中アジナゾラムおよびその主要代謝物のスクリーニングとHPLCによる確認」Journal of Analytical Toxicology . 17 (7): 427– 431. doi : 10.1093/jat/17.7.427 . PMID 8309217 .
- ^ Sethy VH, Francis JW, Day JS (1986年8月). 「プロアディフェンのアディナゾラム代謝への影響」. The Journal of Pharmacy and Pharmacology . 38 (8): 631– 632. doi : 10.1111 / j.2042-7158.1986.tb03099.x . PMID 2876087. S2CID 9394686 .
- ^ a b Fleishaker JC, Phillips JP, Smith TC, Smith RB (1989年5月). 「高齢者におけるアディナゾラムの多回投与における薬物動態および薬力学」.製薬研究. 6 (5): 379– 386. doi : 10.1023/A:1015975214070 . PMID 2748528 .
- ^ Ajir K, Smith M, Lin KM, Fleishaker JC, Chambers JH, Anderson D, et al. (1997年2月). 「アディナゾラムの薬物動態と薬力学:多民族比較」. Psychopharmacology . 129 (3): 265– 270. doi : 10.1007/s002130050189 . PMID 9084065 .
- ^ Wu D, Fu L (2023年12月). 「デザイナーベンゾジアゼピンの検出における最近の知見と進歩:簡潔なレビュー」 . Arhiv Za Higijenu Rada I Toksikologiju . 74 (4): 224– 231. doi : 10.2478/aiht-2023-74-3771 . PMC 10750316. PMID 38146763 .

