クロロファシノン
 | |
| 名前 | |
|---|---|
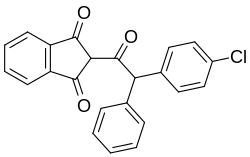
| 推奨IUPAC名 2-[(4-クロロフェニル)フェニルアセチル]-1H-インデン-1,3(2H ) -ジオン | |
| 識別子 | |
| |
3Dモデル(JSmol) | |
| ケムスパイダー |
|
| ECHA 情報カード | 100.020.912 |
| ケッグ |
|
PubChem CID | |
| ユニイ |
|
CompToxダッシュボード(EPA) | |
| |
| |
| プロパティ | |
| C 23 H 15 Cl O 3 | |
| モル質量 | 374.82 g·mol −1 |
特に記載がない限り、データは標準状態(25 °C [77 °F]、100 kPa)における材料のものです。 | |
クロロファシノンは第一世代の抗凝固性殺鼠剤である。[ 1 ]作用機序は、機能不全の凝固因子による内出血である。齧歯類の個体数を制御するための毒素として使用されていた。米国では、緊急事態計画および地域社会の知る権利法(42 USC 11002)第302条で定義されている極めて危険な物質に分類されており、大量に製造、保管、または使用する施設には厳格な報告義務が課せられている。[ 2 ]
歴史
心臓病患者の治療のための抗凝固剤の製造経験があったフランスの会社、Liphatech(旧称Lipha)は、1961年にクロロファシノンを開発し、「Rozol」というブランド名で販売した。クロロファシノンは第一世代の抗凝固性殺鼠剤グループに属し、1940年代から1960年代に陸上環境に生息するげっ歯類を駆除するために初めて開発された。[ 3 ] [ 4 ] [ 5 ]クロロファシノンの使用は、1970年代に同グループの他の殺鼠剤とともに、より強力な第二世代の抗凝固性殺鼠剤に置き換えられ始めたが、そのきっかけとなったのは、北欧とアメリカ合衆国でげっ歯類がワルファリン(別の第一世代の抗凝固性殺鼠剤)に対して耐性を発現し、さらにすべての第一世代の抗凝固性殺鼠剤に対する交差耐性が発見されたという複数の研究結果であった。これは、単一の優性常染色体遺伝子によって引き起こされ、げっ歯類のビタミンK(主に抗凝固剤が生成を阻害するビタミン)の食事必要量を通常の20倍にまで増加させることがわかった。[ 6 ]使用量は減少しているものの、従来の殺鼠剤の餌が使用できない状況では、クロロファシノンは今でも殺鼠剤として購入することができる。[ 7 ]
構造と物理的特性
クロロファシノンは、次の体系名を持つ有機化合物です:(2-[2-(4-クロロフェニル)-2-フェニルアセチル]インダン-1,3-ジオン。構造は、片側がインダンジオン環に結合したアセチル基で構成されています。もう片側には2つのフェニル基が結合しており、1つには塩化物が含まれています。クロロファシノンには1つの光学活性炭素が含まれているため、2つのエナンチオマーとして存在します。
ヘンリー定数は5.12 x 10 −7 atm-m3/molであり、水や土壌から大気中に揮発する可能性が低いことを示唆しています。ヘキサン(25℃で854 mg/L)やメタノール(25℃で786 mg/L)などの有機溶媒への溶解性は、水(25℃で3.43 mg/L)と比較して比較的良好です。[ 5 ] [ 8 ]
| 外観 | 淡黄色の粉末 |
| 融点 | 143.0℃ |
| 危険有害性情報 | H360D: 胎児に悪影響を与える可能性がある H300: 飲み込むと致命的 H310: 皮膚に接触すると致命的 H330: 吸入すると致命的 H372: 長期または長期間にわたる暴露により血液に障害を引き起こす 度重なる露出 H410: 水生生物に対して非常に有毒であり、長期的影響を伴う |
| 相対密度 | 1.4301 g/mL |
| 蒸気圧 | 23℃で 4.76 x 10 −4 Pa |
| ヘンリーの法則定数 | 5.12 x 10 −7 atm-m3/モル |
| UV/Vis吸収 | 約260 nmおよび315 nm |
合成

クロロファシノンは様々なメカニズムで合成できます。以下では、最近研究されたメカニズム(図1)について説明します。この合成法では、従来のメカニズムに比べて副産物の生成量が少なく、クロロファシノンが合成されます。
この合成では、安価で市販されているマンデル酸1 を出発物質として用いる。マンデル酸は塩化スズ4存在下でクロロベンゼン2と反応し、フェニル酢酸3の85%を得る。その後、フェニル酢酸を室温で塩化オキサリルで処理し、6-クロロ-2,2-ジフェニルアセチルクロリド4を得る。最終段階である、先に得られた化合物4と1,3-インダンジオン5とのフリーデル・クラフツ反応は、精製を必要とせず、合成の最終段階に進む。この反応では、ジファシノンやその他の副産物はほとんど生成せず、最終生成物であるクロロファシノン6が得られる。 [ 9 ]
作用機序

クロロファシノンは第一世代の抗凝固性殺鼠剤である。この化合物はインダンジオン誘導体であり、ビタミンK拮抗薬として作用し、肝臓でのビタミンK依存性凝固因子の合成を阻害することで抗凝固作用を発揮する。[ 5 ]凝固因子II、VII、IX、Xの合成には、 γ-グルタミルカルボキシラーゼ(GGCX)によるグルタミン酸のγ-カルボキシグルタミン酸への翻訳後カルボキシル化が関与する。γ-カルボキシグルタミン酸残基は、血管のリン脂質への凝固因子の結合を促進し、それによって凝固を促進する。しかし、カルボキシル化反応を起こすにはビタミンKヒドロキノン(KH 2)補因子が必要である。カルボキシル化反応中にKH 2はビタミンK 2,3エポキシド(KO)に変換される。 KH 2補因子はビタミンKの酸化還元サイクルで生成される。クロロファシノンは、小胞体(ER)に存在する膜貫通タンパク質であるビタミンKエポキシド還元酵素(VKOR)を阻害することで、ビタミンKの酸化還元サイクルを阻害する。この酵素は、このサイクルにおいて重要な役割を果たしている。VKORの触媒活性は、KOからビタミンK、そしてKH 2への還元に必要である。クロロファシノンによるVKORの阻害は、KOからKH 2へのビタミンKのリサイクルを阻害する(図2)。したがって、組織におけるKH 2の供給が減少し、γ-グルタミルカルボキシラーゼのカルボキシル化活性が低下する。 [ 10 ] [ 11 ]その結果、凝固因子のカルボキシル化が低下し、血管の内皮表面に結合できなくなり、生物学的に不活性となる。 [ 12 ]
代謝
クロロファシノンは消化管から吸収されるが、皮膚や呼吸器系からも吸収される可能性がある。[ 13 ]経口摂取した場合、クロロファシノンの吸収は初回摂取後4~6時間でピークとなる。この化合物の半減期は約10時間である。クロロファシノンの最高濃度は肝臓と腎臓で認められる。ラットに経口で繰り返し投与した場合、肝臓への生体蓄積が示唆される。 [ 5 ] 1~4日間の反復暴露の後、定常状態に達する。定常状態に達するまでの時間から、クロロファシノンは体内から急速に排出されることが示唆される。[ 8 ]抗凝固剤は主に腸で速やかに吸収される。この殺鼠剤は肝臓で代謝されることがわかった。代謝はシトクロムP450アイソザイムによって行われ、環水酸化も重要な生体内変換段階であると考えられる。フェニル環とインダンジオニル環で水酸化が起こり、[ 14 ]これらの代謝物は、体循環に入る前にグルクロン酸との抱合をさらに受け、腸肝再循環を起こす可能性があります。肝代謝は一般的に二相性で、初期相は急速で、終末相はより長くなります。[ 10 ]しかし、クロロファシノンの代謝物排泄経路はまだ十分に解明されていません。クロロファシノンの主な排泄経路は糞便(約95%)ですが、尿や呼吸による排泄も少量(<1%)あります。クロロファシノンの26%は、曝露後8時間以内に胆汁を介して排泄されます。[ 5 ]
有効性
クロロファシノンは、陸上環境におけるげっ歯類の個体群制御のための抗凝固性殺鼠剤として使用されています。ラット、マウス、ビーバーを用いた有効性試験において、非常に効果的であることが証明されています。[ 15 ] [ 16 ]ストリキニーネ、リン化亜鉛、クロロファシノン、ジファシノンの4つの毒物の中で、クロロファシノンはマウンテンビーバーの個体群制御において最も高い有効性を示しています。少量を長期間にわたって慢性的に摂取した場合、同量の急性摂取よりも毒性が強くなることが証明されており、これは抗凝固性殺鼠剤に共通する特徴です。[ 17 ]
動物への影響
第一世代抗凝固性殺鼠剤に属するクロロファシノンは、同カテゴリーの他の化学物質と同様に、動物に対して同様の症状を示します。具体的には、標的動物(多くの場合、げっ歯類)が数回摂取すると、血液凝固を阻害し、内出血を引き起こし、最終的には5~7日以内に死に至ります。この作用は、ビタミンK(1)-2,3エポキシド還元酵素(VKOR)を殺鼠剤が阻害することによるものです。VKORはビタミンKの合成を担い、血液凝固に不可欠な凝固因子II、VII、IX、Xを合成します。これらの因子が欠乏すると、最終的に動物の体内で大量出血を引き起こします。このカテゴリーの殺鼠剤における通常の死因は内出血ですが、クロロファシノンは実験ラットにおいて心肺機能や神経症状も引き起こすことが示されており、多くの場合、有意な出血が起こる前に死に至ることがあります。[ 6 ] [ 18 ]
毒性
クロロファシノンは、哺乳動物に経口、経皮、吸入で投与された場合、毒性が極めて強い物質として分類され、毒性区分 I に該当します。皮膚や眼を刺激せず、経皮感作性もありません (毒性区分 IV)。[ 5 ]子羊の暴露事故では、鼻血、呼吸困難、顔面および頸部の腫れなどの症状が見られました。影響を受けた子羊 2 匹の剖検では、すべての臓器 (特に肝臓) が青白く、肺が通常より重く、わずかに茶色がかっていました。[ 19 ] 2.13 ± 0.4 mg/kg のクロロファシノンに暴露された 4 匹のビーバーでは、口からの出血、息苦しさ、痙攣が見られ、暴露後 15 日以内に死亡しました。[ 17 ]鳥類は哺乳類ほどクロロファシノンに敏感ではありませんが、外出血、内血腫、血液凝固時間の延長といった亜致死的影響を経験する可能性があります。一般的な中毒症状としては、呼吸困難、無気力、鼻出血、尿道出血などがあります。[ 5 ]
各種の LD 50値:
| 種 | LD 50値(mg/kg) |
| 雄のネズミ | 3.15 |
| メスのネズミ | 10.95 |
| うさぎ | 0.329 |
| オグロプレーリードッグ | 1.94 |
| キジバト | 258 |
| レッドワーム | >300 |
SENSOR農薬データベースには、1998年から2011年の間にクロロファシノンに関連する12件のヒト曝露事例が記録されています。そのうち1件は中等度の事例で、断熱材作業員がクロロファシノンの粉塵に触れたり吸入したりすることで曝露しました。作業員は震え、発熱、嘔吐に加え、呼吸器系、神経系、胃腸系、腎臓系、心血管系の症状を経験しました。もう1件は、住宅所有者が誤ってクロロファシノンを吸入した後に息切れと咳を経験した事例です。慢性曝露の可能性は低いため、クロロファシノンの発がん性評価は行われていません。[ 5 ]
環境リスク
プレーリードッグ、ホリネズミ、マウンテンビーバー、ジリスなどの動物の個体数を管理するために、巣穴の入り口や巣穴のすぐ外側の地面にクロロファシノンの餌が撒かれる。各撒布は非標的生物への曝露を避けるために草や小石で覆われており、クロロファシノンが土壌に流れ込む可能性は低いが、それでも非標的生物が餌を食べることでクロロファシノンに曝露する可能性は残る。捕食動物もクロロファシノンで中毒した動物を食べる可能性があり、これは二次曝露に分類されるが、致死量を摂取するには複数の中毒動物を摂取する必要がある。抗凝固剤の濃度は二次曝露で10倍に希釈され、捕食動物が中毒でない獲物も食べる場合はさらに薄められる。[ 17 ]標的動物と巣穴を共有する小型の穀類食動物が主に曝露のリスクがある。米国環境保護庁(USEPA)(2004)がまとめた研究では、放牧地におけるカリフォルニアジリスの駆除にクロロファシノンを餌として用いたところ、非標的のシカネズミとサンホアキンポケットマウスが死亡し、その少なくとも86%は餌への曝露によるものと考えられました。鳥類へのクロロファシノン曝露のリスクは最小限であり、水生植物および陸生植物への曝露は無視できる程度と考えられています。[ 5 ]
参照
参考文献
- ^ Buckle, Alan (2000). 「殺鼠剤」. Ullmann's Encyclopedia of Industrial Chemistry . doi : 10.1002/14356007.a23_211 . ISBN 3-527-30673-0。
- ^ 「40 CFR: Part 355の付録A - 極めて危険な物質とその閾値計画量リスト」(PDF)(2008年7月1日版)。政府印刷局。 2011年10月29日閲覧。
{{cite journal}}:ジャーナルを引用するには|journal=(ヘルプ)が必要です - ^ 「殺鼠剤:背景と危険性|安全な齧歯動物駆除」 。 2024年3月14日閲覧。
- ^ "History" . liphatech.com . 2024年3月14日閲覧。
- ^ a b c d e f g h i Lemay A, McCaskill M, Warren J, Hall, TC, Paz L, Deliberto S, Ruell E, Wimberly (2023年3月).野生動物被害管理におけるクロロファシノンの使用(PDF) (報告書).
- ^ a b Hadler, Malcolm R.; Buckle, Alan P. (1992年3月). 「抗凝固剤殺鼠剤の45年間 ― 過去、現在、そして未来の動向」 .第15回脊椎動物害虫会議議事録. CORE出力ID 17234624 .
- ^ 「Rozol Tracking Powder」 liphatech.com . 2024年3月14日閲覧。
- ^ a b「有効成分の評価;承認の更新;評価報告書;クロロファシノン」 2016年7月。
- ^チュク、ルネ;バーセル、アレクサンダー。シュトロール、ディーター (2011-01-01)。「クロロファシノンに代わる効率的なルート」。Zeitschrift für Naturforschung B . 66 (1): 95–97。土井: 10.1515/znb-2011-0116。ISSN 1865-7117。
- ^ a b Horak, Katherine E.; Fisher, Penny M.; Hopkins, Brian (2018). 「標的生物および非標的生物における抗凝固剤の薬物動態」.抗凝固剤と野生生物. 生態毒性学の新たなトピックス. 第5巻. pp. 87– 108. doi : 10.1007/978-3-319-64377-9_4 . ISBN 978-3-319-64375-5。
- ^ Tie, Jian-Ke; Stafford, Darrel W. (2008). 「ビタミンKエポキシド還元酵素の構造と機能」.ビタミンK.ビタミン&ホルモン. 第78巻. pp. 103– 130. doi : 10.1016/s0083-6729(07)00006-4 . ISBN 978-0-12-374113-4. PMID 18374192 .
- ^ Furie, Bruce; Bouchard, Beth A.; Furie, Barbara C. (1999). 「ビタミンK依存性γ-カルボキシグルタミン酸生合成」. Blood . 93 (6): 1798– 1808. doi : 10.1182/blood.v93.6.1798.406k22_1798_1808 . PMID 10068650 .
- ^ Tasheva M. (1995). 「抗凝固性殺鼠剤、環境保健基準175」(PDF) . 世界保健機関.
- ^ Yu, CC; Atallah, YH; Whitacre, DM (1982). 「ラットおよびマウスにおけるジファシノンの代謝と体内動態」. Drug Metabolism and Disposition . 10 (6): 645– 648. doi : 10.1016/S0090-9556(25)07949-8 .
- ^ Whisson, Desley A.; Quinn, Jessica H.; Collins, Kellie; Engilis, Andrew (2004). 「カリフォルニア沿岸林におけるクマネズミ(Rattus rattus)によるオープンカップ巣の鳴鳥への影響を軽減するための管理戦略の開発」脊椎動物害虫会議議事録. 21 (21) . ISSN 0507-6773 .
- ^ピット, ウィリアム C.; ドリスコル, ローラ C.; 杉原, ロバート T. (2011年4月). 「ハワイにおける3種の侵略的げっ歯類の駆除における殺鼠剤ベイトの有効性」.環境汚染・毒性学アーカイブ. 60 (3): 533– 542. Bibcode : 2011ArECT..60..533P . doi : 10.1007/s00244-010-9554-x . ISSN 1432-0703 . PMID 20552335 .
- ^ a b c Arjo, Wendy M.; Nolte, Dale L. (2004). 「マウンテンビーバー(Aplodontia rufa)防除における登録地下餌製品の有効性評価」. Crop Protection . 23 (5): 425– 430. Bibcode : 2004CrPro..23..425A . doi : 10.1016/j.cropro.2003.09.011 .
- ^ペルフレン, アラン・F. (2001). 「殺鼠剤」.農薬毒性学ハンドブック. pp. 1793– 1836. doi : 10.1016/B978-012426260-7.50086-0 . ISBN 978-0-12-426260-7クロロファシノンは、
肝臓におけるプロトロンビンおよび凝固因子VII、IX、Xの合成を抑制する抗凝固剤です。同時に毛細血管透過性への直接的な損傷も生じます。これらの作用の最終的な影響は、広範囲にわたる内出血を誘発することです。さらに、クロロファシノンは酸化的リン酸化の脱共役剤でもあります。クマリン誘導体とは異なり、クロロファシノンは実験ラットにおいて神経障害および心肺障害の症状および徴候を引き起こす可能性があり、出血が起こる前に死亡に至る場合が多いです。クロロファシノンは、長時間持続する凝固抑制作用を特徴としています。
- ^ Piero, Fabio Del; Poppenga, Robert H. (2006年9月). 「クロロファシノン曝露による子羊の急性致死性出血の流行」. Journal of Veterinary Diagnostic Investigation . 18 (5): 483– 485. doi : 10.1177/104063870601800512 . PMID 17037620 .

