| コルチウイルス | |
|---|---|

| |
| コルチウイルス粒子[1] | |
| ウイルスの分類 | |
| (ランク外): | ウイルス |
| レルム: | リボビリア |
| 王国: | オルタナウイルス科 |
| 門: | デュプロルナビリコタ |
| クラス: | レセントビリセテス |
| 注文: | レオウイルス科 |
| 家族: | スピナレオウイルス科 |
| 属: | コルチウイルス |
コルチウイルスは、スピナレオウイルス科に属するウイルス属で、脊椎動物および無脊椎動物に感染します。コロラドダニ熱の原因ウイルスもこのウイルスに含まれます。[2]コロラドダニ熱ウイルスは、発熱、悪寒、頭痛、羞明、筋肉痛、関節痛、倦怠感などを引き起こします。特に小児では出血性疾患を発症する可能性があります。コロラドダニ熱ウイルスでは、リンパ球と好中球の両方が減少する白血球減少症が非常によく見られます。いずれの場合も、感染は脳炎または髄膜炎につながる可能性があります。[3]
ウイルス学
コルチウイルスはウイルス属の一種です。ウイルスは細胞内寄生虫であり、自力で増殖する手段を持たないため、宿主細胞の機能を乗っ取る必要があります。そうすることで初めて、ウイルスタンパク質を合成し、子孫を作り出すことができます。ウイルスには遺伝物質の種類によって2つの種類があります。
DNAウイルスはデオキシリボ核酸(DNA)からなるゲノムを持ち、一方、コルチウイルスなどのRNAウイルスは分節化された(多分節の) RNA(リボ核酸)ゲノムを持ちます。[4] [1]
概要
「コルティウイルス」という名称は、コロラドダニ熱ウイルス(Col orado ti ck)という属の標準種に由来しています。コルティウイルスはスピナレオウイルス科に属します。[5] コルティウイルスと近縁のオルビウイルス属には合わせて約109の血清型があり、そのうちヒトに疾患を引き起こすのは4つだけです。[5]ダニはコルティウイルスの主な媒介動物です。[6]コロラドダニ熱は19世紀に初めて記録され、現在では米国で最も一般的なダニ媒介性疾患の一つとなっています。[3]
ヨーロッパアイヤックウイルスとコロラドダニ熱ウイルスは、同族遺伝子、55%~88%のアミノ酸類似性、および区別できない顕微鏡レベルでの類似性により、親戚関係にあることが知られています。[6]これらの類似性を見つけるために、ゲノム配列解析が実施されました。[7]ヨーロッパアイヤックウイルスがヨーロッパに出現した方法の一つとして、5000万年以上前に北アメリカからウサギ目動物が移住したことが提唱されています。 [6]それ以来、このウイルスはいくつかの違いを帯び、現在では独自のウイルス種であると考えられています。ヨーロッパアイヤックウイルスは、1976年にヨーロッパのIxodes ricinusから分離され、1981年にはIxodes ventalloiと共に同種から分離されました。
分類学
この属には学名順に以下の種が含まれる: [8]
- コルチウイルス・デルマセントリス、コロラドダニ熱ウイルス
- コルチウイルス イクソディス、エイハ ウイルス
- コルチウイルス クンダレンセ、クンダル ウイルス
- コルチウイルス タイエンセ、タイ フォレスト コルチウイルス
- コルチウイルス タルミズエンセ、垂水ウイルス
その他の特徴
形態学と生理学

コルチウイルス のビリオンは直径約60~80ナノメートルで、エンベロープを持たず、一般的に正20面体対称の球形をしています。各ビリオンは、直径約50ナノメートルの核を囲む2つの同心円状のカプシド殻で構成されています。粒子の表面は比較的滑らかです。[7]ウイルスは、周囲の液体が酸性(pH約3)になると感染力を失いますが、pHが7~8の間であれば安定します。また、温度が約55℃になると脅威ではなくなります。[7]
| 属 | 構造 | 対称 | カプシド | ゲノム配列 | ゲノムセグメンテーション |
|---|---|---|---|---|---|
| コルチウイルス | 正二十面体 | T=13、T=2 | 非封筒 | リニア | セグメント化された |
ゲノムとゲノム構成

コルチウイルスは、直鎖状の二本鎖RNAの12のセグメントを有しています。ゲノムをゲル電気泳動で処理すると、セグメントは3つのクラスサイズ(3つのバンド)として移動します。各セグメントは複製され、最大のセグメントはRNAポリメラーゼをコードしています。[7]ゲノム上の他のタンパク質の位置はまだ特定されていません。
病因とウイルスの増殖
コルチウイルスは節足動物と脊椎動物の両方の細胞質内で複製しますが、感染は節足動物によってのみ行われます。[5]ウイルスが複製される際には、RNAポリメラーゼが活性化され、ウイルス粒子のRNA複製を継続するために、ウイルス粒子の外殻が除去される必要があります。子孫におけるRNAセグメントの再集合は一般的であり、これが血清型間の遺伝的多様性の一部に関与しています。場合によっては、これがウイルスの特性の急速な変化につながることがあります。[5]
コルチウイルス属の主要種であるコロラドダニ熱ウイルス(CTF)は、ロッキーマウンテンマダニ(Dermacentor andersoni)に感染します。この種のダニは、低木地帯、薄い森林地帯、草原、ハイキングコースやサイクリングコースで見られます。このダニのすべてのライフステージ(幼虫、若虫、成虫)は、コロラドダニ熱ウイルスを脊椎動物に感染させる可能性があります。残念ながら、成熟したD. andersoniは、膝の高さの植物の周りを歩き回る中型または大型の哺乳類を好んで食べます。[9]多くの場合、この感染はダニの幼虫が、すでにウイルスに感染しているリスなどのげっ歯類を吸血することで発生します。ダニの唾液にはウイルスが含まれており、終生感染力を持ちます。その後、成虫は咬傷を通じてウイルスを人間に感染させ、骨髄細胞に感染します。[5]
ウイルスはこれらの骨髄細胞内で複製され、白血球、好酸球、好塩基球の発達と複製を阻害します。このため、血小板減少症も起こり得ます。核のない赤血球である赤血球は、核のある前駆段階である赤芽球の段階で感染するようです。[5]ウイルスはこれらの赤血球内に最大4か月間、害を与えることなく留まります。[7]ここで、ウイルスは免疫系の攻撃から保護されます。[3]ウイルスに対する抗体は症状が現れ始めてから約2週間後にのみ検出されますが、ウイルスは血液細胞内に約6週間存在し続けます。[5]
| 属 | ホストの詳細 | 組織向性 | エントリー詳細 | リリースの詳細 | 複製部位 | 組立場所 | 伝染 ; 感染 |
|---|---|---|---|---|---|---|---|
| コルチウイルス | 人間、げっ歯類、ダニ、蚊 | 赤血球 | 細胞受容体のエンドサイトーシス | 細胞死 | 細胞質 | 細胞質 | 節足動物の咬傷 |
コロラドダニ熱ウイルス(CTFV)の症状と診断
コロラドダニ熱ウイルスは、発熱、悪寒、頭痛、羞明、筋肉痛、関節痛、倦怠感などを引き起こします。特に小児では出血性疾患を発症する可能性があります。コロラドダニ熱ウイルスによる白血球減少症は、リンパ球と好中球の両方が減少する症状として非常によく見られます。いずれの場合も、感染は脳炎または髄膜炎につながる可能性があります。[3]
診断のためには、赤血球を組織培養に注入し、感染の有無を確認することで赤血球を分離することができます。また、コロラドダニ熱ウイルスの抗原は、免疫蛍光顕微鏡法を用いて同定することができます。この方法では、赤血球表面の抗原を蛍光標識し、蛍光顕微鏡で観察します。[5]
疫学と制御


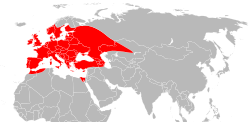
コロラドダニ熱ウイルスの分布は、アメリカ合衆国ロッキー山脈地域の標高4,000フィートから10,000フィートの範囲です。[7]当然のことながら、コロラドダニ熱ウイルスは、カリフォルニア州、コロラド州、アイダホ州、モンタナ州、ネバダ州、オレゴン州、ユタ州、ワシントン州、ワイオミング州、ブリティッシュコロンビア州、アルバータ州などの地域でも見られます。これは、隣の図に示されているウイルスを媒介するダニの分布とほぼ同じです。[5]
このウイルスはダニとげっ歯類の間で循環し、ヒトが二次宿主となります。[5]感染リスクが高いのは、危険地域をハイキングやキャンプをする人です。また、4月、5月、6月は成虫のダニが環境中に蔓延する時期であるため、感染が主に発生します。残念ながら、この時期はハイキングやキャンプに適した気候でもあります。ダニに刺されて感染するのを防ぐ最善の方法は、長袖や長ズボンを着用し、ダニの多い場所を避け、ダニ忌避剤を使用することです。[5]
処理

コロラドダニ熱ウイルスは、逆転写ポリメラーゼ連鎖反応(RT-PCR)によって患者から検出することができ、この方法では単一のウイルス粒子とその遺伝物質を検出することができます。 [7]ウイルスに対する抗原は、免疫蛍光法を使用して検出することもできます。[5]現在、これらのコロラドダニ熱ウイルスを治療するためのワクチンや治療法は知られていませんが、ヌクレオシド類似体である3'-フルオロ-3'-デオキシアデノシンは、コロラドダニ熱ウイルスの複製を試験管内で停止させます。[5]
参考文献
- ^ abc SIB: Viralzone: コルチウイルス
- ^ Attoui H, Charrel RN, Billoir F, Cantaloube JF, de Micco P, de Lamballerie X (1998). 「コルティウイルス属ウイルスのアメリカ、ヨーロッパ、アジアの分離株の比較配列解析」J. Gen. Virol . 79 (10): 2481–9 . doi : 10.1099/0022-1317-79-10-2481 . PMID 9780055.
- ^ abcd Murray, PR; Rosenthal, KS & Pfaller, MA (2013). 「コルチウイルスとオルビウイルス:第59章」. Medical Microbiology (第7版).
- ^ Lodish; Berk; Kaiser; Krieger; Bretscher; Ploegh; Amon & Scott (2013).分子生物学. WH Freeman and Company. p. 160.
- ^ abcdefghijklm アリゾナ州カピキアン、ショップ RE (1996)。 「ロタウイルス、レオウイルス、コルチウイルス、オルビウイルス: 第 63 章」。カピキアン アリゾナ州、ショップ RE、バロン S (編著)。医学微生物学(第 4 版)。ISBN 978-0-9631172-1-2. PMID 21413350。
- ^ abc Attoui H, Mohd Jaafar F, Biagini P, Cantaloube JF, de Micco P, Murphy FA, de Lamballerie X (2002年3月). 「コルティウイルス属(レオウイルス科):旧世界および新世界ウイルスのゲノムおよび形態学的特徴」. Arch. Virol . 147 (3): 533–61 . doi :10.1007/s007050200005. PMC 7098428. PMID 11958454 .
- ^ abcdefg Attoui H、Mohd Jaafar F、de Micco P、de Lamballerie X (2005 年 11 月)。 「北米、ヨーロッパ、アジアにおけるコルチウイルスとシードルナウイルス」。Emerg Infect Dis . 11 (11): 1673 ~ 1679 年。土井:10.3201/eid1111.050868。PMC 3367365。PMID 16318717。
- ^ 「ウイルス分類:2024年版」国際ウイルス分類委員会. 2025年4月22日閲覧。
- ^ ロードアイランド大学TickEncounterリソースセンター (2014). 「Dermacentor andersoni, ロッキーマウンテンマダニ」
外部リンク
- ウイルスゾーン:コルチウイルス
- ロードアイランド大学TickEncounterリソースセンター
- ICTV