 | |
| 名前 | |
|---|---|
| 推奨IUPAC名
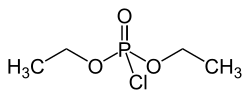
ジエチルホスホロクロリデート | |
その他の名前
| |
| 識別子 | |
3Dモデル(JSmol)
|
|
| ケムスパイダー |
|
| ECHA 情報カード | 100.011.270 |
PubChem CID
|
|
| ユニイ | |
CompToxダッシュボード (EPA)
|
|
| |
| |
| プロパティ | |
| (C 2 H 5 O) 2 P(O)Cl | |
| モル質量 | 172.54 g·mol −1 |
| 外観 | 無色の液体 |
| 密度 | 1.1915 g/cm 3 |
| 沸点 | 60℃(140°F; 333 K)(2 mm Hg) |
特に記載がない限り、データは標準状態(25 °C [77 °F]、100 kPa)における材料のものです。
| |
ジエチルクロロホスフェートは、化学式(C 2 H 5 O) 2 P(O)Clで表される有機リン化合物です。有機合成試薬として、アルコールを対応するジエチルリン酸エステルに変換するために用いられます。フルーティーな香りを持つ無色の液体です。腐食性があり、コリンエステラーゼ阻害剤として経皮吸収により強い毒性を示します。[1]分子は四面体です。
合成と反応
この化合物は、ジエチルホスファイトと四塩化炭素の塩素化(アサートン・トッド反応)によって製造される。[2]
この化合物は求電子性である。制御された加水分解によりテトラエチルピロリン酸が得られる。アルコールと反応するとリン酸エステルが得られる: [3]
- (C 2 H 5 O) 2 P(O)Cl + ROH → (C 2 H 5 O) 2 P(O)OR + HCl
この試薬は、カルボン酸塩[4]、アルコール[5]、アミン[6]のリン酸化のための有機合成において日常的に使用されています。
参照
- ジエチルクロロホスフェートは www.chemicalbook.com にあります。
参考文献
- ^ 「Haz-Mapカテゴリー詳細」hazmap.nlm.nih.gov . 2016年7月30日閲覧。
- ^ Steinberg, Geo. M. (1950). 「ジアルキルホスファイトの反応.ジアルキルクロロホスフェート,テトラアルキルピロホスフェート,および混合オルトリン酸エステルの合成」. Journal of Organic Chemistry . 15 (3): 637–47 . doi :10.1021/jo01149a031.
- ^ Young, Jonathan R. (2001). 「ジエチルホスホロクロリデート」. E-EROS有機合成試薬百科事典. pp. 1– 3.
- ^ Michael A. Insalaco; D. Stanley Tarbell (1970). 「tert-ブチルアジドホルメート」. Org. Synth . 50 :9. doi :10.15227/orgsyn.050.0009.
- ^ DC Muchmore (1972). 「エノールリン酸の調製と還元的開裂:5-メチルコプロスト-3-エン」. Org. Synth . 52 : 109. doi :10.15227/orgsyn.052.0109.
- ^ Nick Nikolaides、Ioanna Schipor、Bruce Ganem (1995). 「アミンからリン酸エステルへの変換:デシルジエチルリン酸」. Org. Synth . 72 : 246. doi :10.15227/orgsyn.072.0246.
