| 赤痢アメーバ | |
|---|---|

| |
| 赤痢アメーバ 栄養体 | |
| 科学的分類 | |
| ドメイン: | 真核生物 |
| 門: | アメーボゾア |
| 家族: | エントアメーバ科 |
| 属: | 赤痢アメーバ |
| 種: | E. histolytica
|
| 二名法名 | |
| 赤痢アメーバ シャウディン、1903年
| |


赤痢アメーバは、嫌気性寄生性アメーバで、赤痢アメーバ属 に属します。 [1]主にヒトやその他の霊長類に感染して赤痢アメーバ症を引き起こし、世界中で約3,500万~5,000万人が赤痢アメーバに感染していると推定されています。 [1]赤痢アメーバ感染症によって、毎年55,000人以上が死亡していると推定されています。 [2]以前は、世界人口の10%が感染していると考えられていましたが、この数字は、これらの感染症の少なくとも90%が2番目の種である赤痢アメーバによるものであるという認識以前のものです。 [3]犬や猫などの哺乳類は一時的に感染する可能性がありますが、伝染に大きく寄与するとは考えられていません。
組織溶解という言葉は文字通り、有機組織の崩壊と溶解を意味します。
伝染 ; 感染
活動期(栄養体)は宿主と新鮮な軟便にのみ存在する。嚢子は宿主の体外で水、土壌、食物上、特に食物の湿潤条件下で生存する。赤痢アメーバに感染した人の便に触れたものを口に入れたり、赤痢アメーバに汚染された水や食物を飲み込んだり、汚染された表面や指についた赤痢アメーバの嚢子(卵)を飲み込んだりすると、感染が起こる可能性がある。 [4]嚢子は熱や凍結温度で容易に死滅し、宿主の体外では数ヶ月しか生存しない。[5] 嚢子が飲み込まれると、消化管で脱嚢(栄養体を放出)して感染を引き起こす。赤痢アメーバの病原性は1875年にFedor A. Löschによって初めて報告されたが[1]、ラテン語名が与えられたのは1903年にFritz Schaudinnによって記載されたときだった。赤痢アメーバは、その名前( histo – lytic = 組織を破壊する)が示すとおり病原性があり、感染しても無症状のこともあれば、アメーバ性赤痢やアメーバ性肝膿瘍を引き起こすこともある[6] [7]。症状には、劇症赤痢、血性下痢、体重減少、疲労、腹痛、アメーバ腫などがある。アメーバは腸壁に穴を開けて病変や腸の症状を引き起こし、血流や腹腔に到達することもある[8] 。 そこから人体の重要な臓器、通常は肝臓、ときには肺、脳、脾臓に到達する。[9] この組織侵入の一般的な結果は肝膿瘍であり、治療しないと致命的となる可能性があります。[8]摂取された赤血球がアメーバ細胞の細胞質内に見られることがあります。[10]
リスク要因
衛生状態の悪さは、赤痢アメーバ症(E. histolytica)にかかるリスクを高めることが知られています。[11]アメリカ合衆国では、カリフォルニア州とテキサス州(これらの州が赤痢アメーバの流行地域(メキシコなど)に近いことが原因である可能性があります)、ラテンアメリカの一部、およびアジアで、赤痢アメーバ症関連の死亡率が非常に高くなっています。[12] 赤痢アメーバは、特に男性同性愛関係において、新興の性感染性病原体としても認識されており、非流行地域での発生を引き起こしています。[13]そのため、リスクの高い性行為も潜在的な感染源となります。[14]因果関係があるかどうかは不明ですが、研究によると、ヒト免疫不全ウイルス(HIV)に感染している人は、赤痢アメーバに感染する可能性が高いことが示されています。[15] [16]
ゲノム
赤痢アメーバの ゲノム は2005年に配列決定、アセンブル、自動アノテーションが行われた。[17] ゲノムは2010年に再アセンブルおよび再アノテーションされた。[18] 2,000万塩基対のゲノムアセンブリには8,160個の予測遺伝子が含まれており、既知および新規の転移因子がマッピングおよび特徴付けられ、機能割り当てが改訂・更新され、代謝経路、遺伝子オントロジー割り当て、トランスポーターのキュレーション、遺伝子ファミリーの生成などの追加情報が組み込まれている。[19]赤痢アメーバ における転移因子の主要なグループは、非LTRレトロトランスポゾンである。これらは、EhLINEおよびEhSINE(EhLINE1,2,3およびEhSINE1,2,3)と呼ばれる3つのファミリーに分類されている。[20] EhLINE1は、逆転写酵素とヌクレオチド結合ORF1に加えて、細菌の制限エンドヌクレアーゼ(EN)タンパク質をコードしており、これは細菌の制限エンドヌクレアーゼと類似性がある。細菌タンパク質とのこの類似性は、この原生動物寄生虫において、転移因子が原核生物から水平遺伝子伝播によって獲得されたことを示唆している。[21]
E. histolyticaのゲノムには、 opisthokontのような特徴を持つsnoRNAがあることがわかっています。[22] E. histolytica U3 snoRNA(Eh_U3 snoRNA)は、Homo sapiens U3 snoRNAと類似した配列と構造的特徴を示しています。[23]
病原体相互作用
赤痢アメーバは特定のヒトウイルスの毒性を調節する可能性があり、またそれ自体が自身のウイルスの宿主となる。[要出典]
例えば、後天性免疫不全症候群(AIDS)は赤痢アメーバの損傷と病原性を増強します。[16]一方、HIVに感染した細胞は赤痢アメーバによってしばしば消費されます。感染性HIVはアメーバ内で生存しますが、このウイルスを保有するアメーバからヒトへの再感染の証拠はありません。[24]
赤痢アメーバ(Entamoeba histolytica)のウイルスに関する研究の爆発的な進展は、1972年から1979年にかけてDiamondらが発表した一連の論文に端を発する。1972年、彼らは赤痢アメーバ(Entamoeba histolytica )の中に、細胞溶解を引き起こす2種類の多角体型ウイルス株と糸状型ウイルス株が存在するという仮説を立てた。おそらく最も斬新な発見は、2種類のウイルス株が存在し、ある種類のアメーバ(HB-301株)では多角体型株は有害な影響を与えないが、別の種類のアメーバ(HK-9株)では細胞溶解を引き起こすという点であった。Matternらはこれらの原生動物ウイルスがバクテリオファージのように機能する可能性を探ろうとしたが、ウイルス感染による赤痢アメーバの毒性に有意な変化は見られなかった。 [25]
免疫病理学
赤痢アメーバは組織破壊を引き起こし、臨床疾患につながります。赤痢アメーバは、宿主細胞の直接的な死、炎症、そして寄生虫の侵入という3つの主要な過程によって組織損傷を引き起こします。栄養体は回腸末端部で脱嚢すると、大腸に定着し、粘液層の表面に留まり、細菌や食物粒子を餌とします。時折、未知の刺激に反応して栄養体は粘液層を通過し、上皮細胞層と接触して病理学的プロセスを開始します。赤痢アメーバは、上皮細胞表面のガラクトースおよびN-アセチルガラクトサミン糖に結合するレクチンを有しています。このレクチンは通常、細菌を結合させて摂取するために用いられます。この寄生虫は、孔形成タンパク質、リパーゼ、システインプロテアーゼといった酵素を複数有しており、これらは通常、食胞内の細菌を消化するために使用されるが、栄養体が上皮細胞と接触し、レクチンを介して結合すると、細胞壊死やアポトーシスを誘導し、上皮細胞の溶解を引き起こす可能性がある。放出された酵素は腸壁や血管への侵入を可能にし、時には肝臓や他の臓器にまで浸透する。栄養体はこれらの死んだ細胞を摂取する。上皮細胞層へのこの損傷はヒトの免疫細胞を引き寄せ、これらの免疫細胞は栄養体によって溶解される。そして、免疫細胞の溶解酵素が周囲の組織に放出され、一種の連鎖反応が起こり、組織破壊につながる。この破壊は組織に「潰瘍」という形で現れ、横断面での外観からフラスコ型と表現されることが多い。この組織破壊は血管にも波及し、血性下痢やアメーバ性赤痢を引き起こす可能性があります。栄養体が血流に入り、門脈系を介して肝臓に運ばれることもあります。肝臓では同様の病理学的連鎖が起こり、アメーバ性肝膿瘍を引き起こします。栄養体は他の臓器に侵入することもあり、血流を介して侵入する場合もあれば、肝膿瘍の破裂や瘻孔を介して侵入する場合もあります。同様に、栄養体が脳に侵入すると、アメーバ性脳膿瘍を引き起こす可能性があります。[26]
診断
診断は、新鮮または適切に保存された糞便検体、直腸鏡検査で得られた吸引物または掻爬物の塗抹標本、膿瘍の吸引物またはその他の組織検体における栄養体または嚢子の顕微鏡検査によって確定されます。血液検査も利用可能ですが、医療提供者が感染が腸管を越えて肝臓などの他の臓器に広がっている可能性があると判断した場合にのみ推奨されます。ただし、この血液検査は、検査時に感染していなくても、過去にアメーバ症に罹患したことがある場合は陽性となる可能性があるため、現在の病気の診断には役立たない可能性があります。[27] 便抗原検出とPCRは診断に利用可能であり、顕微鏡検査よりも感度と特異度が高いです。[2]
-
赤痢アメーバ 栄養体
-
赤痢アメーバによる腸潰瘍
-
赤痢アメーバ 嚢胞
-
未熟な赤痢アメーバ嚢胞(成熟した嚢胞は4つの核を持つ)
-
赤痢アメーバの染色体小体を含む四核囊胞。
-
二分裂による増殖
-
E. histolytica の図
-
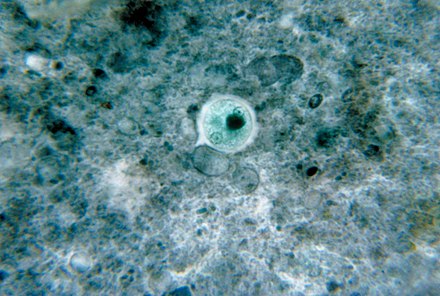
アメーバ性大腸炎患者における特異的抗赤痢アメーバマクロファージ遊走阻止因子抗体を用いた栄養体(茶色)の免疫組織化学染色
処理
赤痢アメーバの治療には、いくつかの抗生物質が利用可能です。赤痢アメーバ感染症による症状がない場合は、1種類の抗生物質のみで治療されますが、症状が悪化している場合は、2種類の抗生物質が処方される可能性が高くなります。 [28]それ以外の場合は、以下の治療法があります。
腸の感染症
通常、ニトロイミダゾール誘導体(メトロニダゾールなど)が使用されます。これは、アメーバの栄養体に対して非常に有効であるためです。アメーバシストにはほとんど効果がないため、通常はこの治療に続いて、腔内の微生物に作用する薬剤(パロモマイシンやジロキサニドフラン酸塩など)が投与されます。[2]
肝膿瘍
肝膿瘍の治療には、主にメトロニダゾールやクロロキンなどの薬剤を用いて固形組織内の微生物を標的とすることに加え、再浸潤を防ぐために腸管腔内に作用する薬剤(前段落参照)も含める必要があります。破裂が差し迫っている場合を除き、外科的ドレナージは通常必要ありません。[29]
症状のない人
非流行地域に居住する無症状の人(いわゆる無症候性キャリア)は、パロモマイシンで治療する必要があります。その他の治療薬としては、ジロキサニドフランカルボン酸エステルやヨードキノールなどがあります。[要出典] ヨードキノールとヨードクロルヒドロキシキンの使用には問題があるため、推奨されません。ジロキサニドフランカルボン酸エステルは、嚢胞を排出しているだけの軽度の症状のある人にも使用できます。[要出典]
| 属と種 | 赤痢アメーバ |
| 病因物質: | アメーバ症、アメーバ赤痢、腸管外アメーバ症(通常はアメーバ性肝膿瘍)、"アンチョビソース"、皮膚アメーバ、アメーバ性肺膿瘍("肝臓色の痰") |
| 感染期 | 四核囊胞(2~4個の核を持つ) |
| 終宿主 | 人間 |
| 入国ポータル | 口 |
| 感染経路 | 汚染された食物や水を介して成熟嚢胞を摂取する |
| 生息地 | 結腸と盲腸 |
| 病原性段階 | 栄養体 |
| 機関車装置 | 偽足(「偽の足」) |
| 運動性 | 能動的、進歩的、方向性のある |
| 核 | 「リングとドット」の外観:周辺クロマチンと中心核小体 |
| 繁殖方法 | 二分裂 |
| 病因 | 溶解性壊死(消化管切片(GIT)では「フラスコ型」の穴のように見える) |
| 嚢胞の種類 | 保護と生殖 |
| 臨床検査による診断 | 最も一般的な検査法は、直接糞便塗抹標本(DFS)と染色(ただし、種レベルの同定は不可能)、酵素免疫測定(EIA)、間接赤血球凝集反応(IHA)、抗原検出(モノクローナル抗体)、種同定のためのPCRです。嚢子の検出には、固定液(ホルマリン)の使用のみが有効な場合もあります。培養:糞便サンプルから:ロビンソン培地、ジョーンズ培地 |
| 処理 | 侵襲性栄養体にはメトロニダゾールを、腸管内に留まっている栄養体には内腔アメーバ駆除薬を併用する。ジロキサニドフランカルボン酸エステル(フラミド)は米国およびカナダでは市販されていないため(米国疾病予防管理センター(CDC)からのみ入手可能)、パロモマイシン(ヒューマチン)が内腔アメーバ駆除薬として最適である。有効性を直接比較した結果、パロモマイシンの方が治癒率が高いことが示された。 [30] パロモマイシン(ヒューマチン)は腎毒性と聴毒性の両方を有するため、大腸炎患者には慎重に使用する必要がある。損傷した腸管壁からの吸収は、永続的な難聴や腎障害を引き起こす可能性がある。推奨用量:メトロニダゾール750mgを1日3回経口投与し、5~10日間投与した後、パロモマイシン30mg/kg/日を3回に分けて経口投与し、5~10日間投与するか、ジロキサニドフロエート500mgを1日3回経口投与し、10日間投与することで、内腔アメーバを根絶し、再発を予防する。[31] [32] |
| 栄養体段階 | |
| 病理学的/診断的特徴 | 摂取した赤血球;特徴的な核 |
| 嚢胞期 | |
| 染色体小体 | 「葉巻」型の体(結晶リボソームで構成されている) |
| 核の数 | 初期段階では1、成熟段階では4 |
| 病理学的/診断的特徴 | 「リングとドット」核と染色体小体 |
減数分裂
有性生殖を行う真核生物では、相同組換え(HR)は通常、減数分裂中に起こる。減数分裂特異的組換え酵素Dmc1は効率的な減数分裂HRに必要であり、Dmc1は赤痢アメーバ(E. histolytica)で発現している。[33]赤痢アメーバ から精製されたDmc1はシナプス前フィラメントを形成し、少なくとも数千塩基対に及ぶATP依存性の相同DNA対合およびDNA鎖交換を触媒する。[33] DNA対合および鎖交換反応は、真核生物の減数分裂特異的組換え補助因子(ヘテロ二量体)Hop2-Mnd1によって促進される。[33] これらのプロセスは減数分裂組換えの中心的過程であり、赤痢アメーバが減数分裂を起こすことを示唆している。[33]
赤痢アメーバには、有糸分裂および減数分裂HRに関与する他のいくつかの遺伝子も存在する。[34] HRは、ストレスのかかる成長条件(血清飢餓)下で増強され、同時にHR関連遺伝子の上方制御も起こる。[35] また、紫外線照射は赤痢 アメーバの栄養体においてDNA損傷を誘発し、組換えDNA修復経路を活性化する。[34] 特に、Rad51タンパク質(リコンビナーゼ)の発現は紫外線処理によって約15倍に増加する。[34]
参照
参考文献
- ^ abc Rawat A, Singh P, Jyoti A, Kaushik S, Srivastava VK (2020年8月). 「伝播の回避:アメーバ症管理における重要なターゲット」. Chemical Biology & Drug Design . 96 (2): 731– 744. doi :10.1111/cbdd.13699. PMID 32356312. S2CID 218475533.
- ^ abc Shirley DT, Farr L, Watanabe K, Moonah S (2018年7月). 「アメーバ症の世界的負担、新たな診断法、そして現在の治療法のレビュー」. Open Forum Infectious Diseases . 5 (7) ofy161. doi :10.1093/ofid/ofy161. PMC 6055529. PMID 30046644 .
- ^ 「アメーバ症」(PDF) . Relevé Épidémiologique Hebdomadaire。72 (14): 97–99。1997年 4 月。PMID 9100475 。
- ^ 「赤痢アメーバ」. 米国疾病予防管理センター. 2017年10月24日閲覧。
- ^ アメリカ水道協会(2006年6月)「水系病原体」アメリカ水道協会ISBN 978-1-58321-403-9。
- ^ Ryan KJ, Ray CG編 (2004). Sherris Medical Microbiology (第4版). McGraw Hill. pp. 733–8 . ISBN 978-0-8385-8529-0。
- ^ Nespola B, Betz V, Brunet J, Gagnard JC, Krummel Y, Hansmann Y, et al. (2015). 「初発から22年後に初めてアメーバ性肝膿瘍が発見された症例」. Parasite . 22 : 20. doi :10.1051/parasite/2015020. PMC 4472968. PMID 26088504.

- ^ ab Jackson-Akers JY, Prakash V, Oliver TI (2023年8月8日). 「アメーバ性肝膿瘍」. StatPearls . フロリダ州トレジャーアイランド: StatPearls Publishing. PMID 28613582. 2024年1月11日閲覧– 国立医学図書館経由.
- ^ ドス・サントス・ザネッティA、マレイロスAF、デ・マトスTA、ドス・サントスC、バッタリーニPF、モレイラLM、レモスLM、カトリヨンSK、ダ・コスタ・ボアモルテ・コルテーラD、イニョッティE、エスピノーサOA (2021)。 「ブラジルにおけるエンタメーバ属の多様性、地理的分布、蔓延:体系的レビューとメタ分析」。パラサイト。28 : 17.土井: 10.1051/parasite/2021028。PMC 8019558。PMID 33812449。
- ^ 「アメーバ症の臨床検査:赤痢アメーバと赤痢アメーバ・ディスパー」(PDF) DPDx :公衆衛生上の懸念のある寄生虫の臨床検査による同定。米国疾病管理予防センター。 2024年1月11日閲覧。
- ^ 「一般情報:アメーバ症」。寄生虫。米国疾病予防管理センター。 2018年3月1日閲覧。
- ^ Gunther J, Shafir S, Bristow B, Sorvillo F (2011年12月). 「短報:米国居住者におけるアメーバ症関連死亡率、1990~2007年」.アメリカ熱帯医学衛生誌. 85 (6): 1038–40 . doi :10.4269/ajtmh.2011.11-0288. PMC 3225148. PMID 22144440 .
- ^ Escolà-Vergé L、Arando M、Vall M、Rovira R、Espasa M、Sulleiro E、他。 (2017年7月)。 「男性と性行為をする男性の間で腸内アメーバ症が発生、バルセロナ(スペイン)、2016年10月と2017年1月」。ユーロ監視。22 (30)。土井:10.2807/1560-7917.ES.2017.22.30.30581。PMC 5553055。PMID 28797327。
- ^ Stark D, van Hal SJ, Matthews G, Harkness J, Marriott D (2008年7月). 「男性同性愛者における侵襲性アメーバ症、オーストラリア」. Emerging Infectious Diseases . 14 (7): 1141–3 . doi :10.3201/eid1407.080017. PMC 2600324. PMID 18598643 .
- ^ James R, Barratt J, Marriott D, Harkness J, Stark D (2010年10月). 「オーストラリア、シドニーにおける男性同性愛者における赤痢アメーバ感染症の血清有病率」.アメリカ熱帯医学衛生学誌. 83 (4): 914–6 . doi :10.4269/ajtmh.2010.10-0231. PMC 2946768. PMID 20889891 .
- ^ ab Hung CC, Deng HY, Hsiao WH, Hsieh SM, Hsiao CF, Chen MY, et al. (2005年2月). 「台湾におけるヒト免疫不全ウイルス1型感染症患者における新興寄生虫疾患としての侵襲性アメーバ症」.内科アーカイブ. 165 (4): 409– 415. doi : 10.1001/archinte.165.4.409 . PMID 15738369.
- ^ Loftus B, Anderson I, Davies R, Alsmark UC, Samuelson J, Amedeo P, et al. (2005年2月). 「原生生物寄生虫Entamoeba histolyticaのゲノム」. Nature . 433 (7028): 865–8 . Bibcode :2005Natur.433..865L. doi : 10.1038/nature03291 . PMID 15729342.
- ^ Lorenzi HA, Puiu D, Miller JR, Brinkac LM, Amedeo P, Hall N, Caler EV (2010年6月). 「赤痢アメーバゲノムの新たなアセンブリ、再アノテーション、解析により、新たなゲノム特性とタンパク質含有量の情報が明らかになった」. PLOS Neglected Tropical Diseases . 4 (6) e716. doi : 10.1371 /journal.pntd.0000716 . PMC 2886108. PMID 20559563.
- ^ Caler, E & Lorenzi, H (2010). 「赤痢アメーバ:ゲノムの現状とウェブリソース」.嫌気性寄生性原生動物:ゲノミクスと分子生物学. Caister Academic Press . ISBN 978-1-904455-61-5。
- ^ Bakre AA, Rawal K, Ramaswamy R, Bhattacharya A, Bhattacharya S (2005年7月). 「赤痢アメーバのLINEとSINE:比較分析とゲノム分布」.実験寄生虫学. 110 (3): 207– 213. doi :10.1016/j.exppara.2005.02.009. PMID 15955314.
- ^ Yadav VP, Mandal PK, Rao DN, Bhattacharya S (2009年12月). 「赤痢アメーバの非長末端反復配列レトロトランスポゾンEhLINE1がコードする制限酵素様エンドヌクレアーゼの特性解析」. The FEBS Journal . 276 (23): 7070–82 . doi :10.1111/j.1742-4658.2009.07419.x. PMID 19878305. S2CID 30791213.
- ^ Kaur D, Gupta AK, Kumari V, Sharma R, Bhattacharya A, Bhattacharya S (2012年8月). 「赤痢アメーバ(Entamoeba histolytica)のC/D、H/ACA、Eh_U3 snoRNAの計算予測と検証」BMC Genomics . 13 390. doi : 10.1186/1471-2164-13-390 . PMC 3542256 . PMID 22892049.
- ^ Srivastava A, Ahamad J, Ray AK, Kaur D, Bhattacharya A, Bhattacharya S (2014年2月). 「寄生性原生生物Entamoeba histolyticaにおけるU3 snoRNAと小サブユニットプロセソーム構成因子の解析」Mol Biochem Parasitol . 193 (2): 82– 92. doi :10.1016/j.molbiopara.2014.03.001. PMID 24631428.
- ^ Brown M, Reed S, Levy JA, Busch M, McKerrow JH (1991年1月). 「ヒト細胞への伝播の証拠なしに赤痢アメーバからHIV-1を検出」. AIDS . 5 (1): 93– 96. doi :10.1097/00002030-199101000-00014. PMID 2059366.
- ^ Diamond LS, Mattern CF, Bartgis IL (1972年2月). 「赤痢アメーバウイルス. I. 伝染性ウイルス様因子の同定」. Journal of Virology . 9 (2): 326– 341. doi :10.1128/JVI.9.2.326-341.1972. PMC 356300. PMID 4335522 .
- ^ Kantor M, Abrantes A, Estevez A, Schiller A, Torrent J, Gascon J, et al. (2018). 「赤痢アメーバ:臨床症状、病因、ワクチン開発の最新情報」. Canadian Journal of Gastroenterology & Hepatology . 2018 4601420. doi : 10.1155/2018/4601420 . PMC 6304615. PMID 30631758 .
- ^ 「赤痢アメーバ」. 米国疾病予防管理センター. 2017年10月24日閲覧。
- ^ 「赤痢アメーバ」. 米国疾病予防管理センター. 2017年10月24日閲覧。
- ^ Kucik CJ, Martin GL, Sortor BV (2004年3月). 「一般的な腸管寄生虫」. American Family Physician . 69 (5): 1161–8 . PMID 15023017.
- ^ Blessmann J, Tannich E (2002年10月). 「無症候性腸管赤痢アメーバ感染症の治療」. The New England Journal of Medicine . 347 (17): 1384. doi : 10.1056/NEJM200210243471722 . PMID 12397207.
- ^ Stanley SL (2003年3月). 「アメーバ症」. Lancet . 361 (9362): 1025–34 . Bibcode :2003Lanc..361.1025S. doi :10.1016/S0140-6736(03)12830-9. PMID 12660071. S2CID 208792864.
- ^ “Diloxanide (Systemic)”. 2016年11月10日時点のオリジナルよりアーカイブ。2011年11月17日閲覧。
- ^ abcd Kelso AA, Say AF, Sharma D, Ledford LL, Turchick A, Saski CA, et al. (2015). 「Entamoeba histolytica Dmc1はカルシウムとHop2-Mnd1によって刺激される相同DNA対合および鎖交換を触媒する」. PLOS ONE . 10 (9) e0139399. Bibcode :2015PLoSO..1039399K. doi : 10.1371/journal.pone.0139399 . PMC 4589404. PMID 26422142 .
- ^ abc López-Casamichana M, Orozco E, Marchat LA, López-Camarillo C (2008年4月). 「赤痢アメーバにおけるDNA損傷に対する相同組換え機構の転写プロファイルとEhRAD51リコンビナーゼの特性解析」BMC Molecular Biology 9-35 . doi : 10.1186 /1471-2199-9-35 . PMC 2324109. PMID 18402694 .
- ^ Singh N, Bhattacharya A, Bhattacharya S (2013). 「エントアメーバにおける相同組換えは成長ストレスとステージ転換中に促進される」. PLOS ONE . 8 (9) e74465. Bibcode :2013PLoSO...874465S. doi : 10.1371/journal.pone.0074465 . PMC 3787063. PMID 24098652 .
外部リンク
- 赤痢アメーバ画像ライブラリ 2013年10月20日アーカイブ - Wayback Machine
- 赤痢アメーバ –疾病管理予防センター
- CDC DPDx寄生虫学診断ウェブサイト(2013年7月10日アーカイブ)
- LSHTM Entamoeba ホームページ
- アメーバゲノムリソース – AmoebaDB
- 米国食品医薬品局のBad Bug Bookに掲載されている赤痢アメーバに関する記事







_using_specific_anti–Entamoeba_histolytica_macrophage_migration_inhibitory_factor_antibodies_in_a_patient_with_amebic_colitis.jpg/440px-thumbnail.jpg)


