| |
| 名前 | |
|---|---|
| IUPAC名
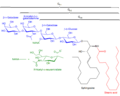
(2 S ,4 S ,5 R ,6 R )-5-アセトアミド-2-[(2 S ,3 R ,4 R ,5 S ,6 R )-5-[(2 S ,3 R ,4 R ,5 R ,6 R )-3-アセトアミド-5-ヒドロキシ-6-(ヒドロキシメチル)-4-[(2 R ,3 R , 4 S ,5 R ,6 R )-3,4,5-トリヒドロキシ-6-(ヒドロキシメチル)オキサン-2-イル]オキシオキサン-2-イル]オキシ-2-[(2 R ,3 S ,4 R ,5 R ,6 R )-4,5-ジヒドロキシ-6-[( E ,2 R ,3 S )-3-ヒドロキシ-2-(イコサノイルアミノ)イコス-4-エノキシ]-2-(ヒドロキシメチル)オキサン-3-イル]オキシ-3-ヒドロキシ-6-(ヒドロキシメチル)オキサン-4-イル]オキシ-4-ヒドロキシ-6-[(1 R ,2 R )-1,2,3-トリヒドロキシプロピル]オキサン-2-カルボン酸
| |
| その他の名前
モノシアロテトラヘキソシルガングリオシド
| |
| 識別子 | |
3Dモデル(JSmol)
|
|
| ケムスパイダー | |
| メッシュ | G(M1)+ガングリオシド |
PubChem CID
|
|
| ユニイ | |
| |
| |
| プロパティ | |
| C 77 H 139 N 3 O 31 | |
| モル質量 | 1 602 .949 g·mol −1 |
特に記載がない限り、データは標準状態(25 °C [77 °F]、100 kPa)における材料のものです。
| |
GM1(モノシアロテトラヘキソシルガングリオシド)は、「プロトタイプ」ガングリオシドであり、1つのシアリン酸残基を含むガングリオシド群の一種です。GM1は重要な生理学的特性を有し、神経可塑性と修復機構、そして脳における神経栄養因子の放出に影響を与えます。脳生理における機能に加え、GM1はコレラ毒素と大腸菌の易熱性腸毒素(旅行者下痢症)の結合部位としても機能します。 [1] [2]
GM1と遺伝性疾患
ガラクトシダーゼはGM1を分解する酵素であり、GM1の除去がうまくいかないとGM1ガングリオシドーシスを発症します。[3] GM1ガングリオシドーシスは、GM1の蓄積に伴い脳と脊髄のニューロンが徐々に破壊される遺伝性疾患です。治療を行わない場合、発達障害や筋力低下をきたし、最終的には重度の知的障害や死に至ります。
GM1と後天性疾患
GM1に対する抗体はギラン・バレー症候群、認知症、狼瘡において増加しているが、その機能は明らかではない。[4] GM1に対する抗体がギラン・バレー症候群における下痢 と関連していることを示唆する証拠もいくつかある。[5]
GM1 抗体は、まれな抗体媒介性炎症性神経障害 である多巣性運動神経障害(MMN) でも見られます。
GM1とコレラ毒素
コレラ菌はコレラ毒素と呼ばれる多量体毒素を産生する。分泌された毒素はGM1ガングリオシドに結合して宿主粘膜細胞の表面に付着する。GM1は、セラミド脂質に共有結合したシアリン酸含有オリゴ糖からなる。この毒素のA1サブユニットは、GM1ガングリオシド受容体を介してBサブユニットの助けを借りて腸管上皮細胞に侵入する。侵入後、A1サブユニットはGsαサブユニットをADPリボシル化し、 GTPase活性を阻害する。これにより活性状態が維持され、アデニル酸シクラーゼが持続的に刺激される。持続的なアデニル酸シクラーゼ活性はcAMPの持続的な増加につながり、電解質と水分の喪失を引き起こし、下痢を引き起こす。[要出典]
SGLT1受容体は小腸に存在します。コレラ患者に水、ナトリウム、ブドウ糖を含む溶液を投与すると、SGLT1受容体はナトリウムとブドウ糖を再吸収し、同時に水はナトリウムとともに受動的に吸収されます。これにより、コレラ誘発性下痢で失われた 水分と電解質が補充されます。
治療への応用
GM1はニューロン修復機構において重要な役割を果たすことから、様々な神経変性疾患の進行を遅らせ、あるいは逆転させる可能性のある薬剤として研究されてきました。対照試験である第II相試験では、GM1がパーキンソン病の症状を緩和することが示されており、これはおそらく黒質の変性を抑制することによってもたらされると考えられます。[6]また、同様の手法を用いて、急性脊髄損傷後に生じる壊死やアポトーシスによる細胞損傷を抑制することが試みられています。[7]
追加画像
-
スフィンゴリピドーシス
参考文献
- ^ Mocchetti I (2005). 「外因性ガングリオシド、神経可塑性と修復、そして神経栄養因子」. Cell. Mol. Life Sci . 62 ( 19–20 ): 2283–94 . doi :10.1007/s00018-005-5188-y. PMC 11139125. PMID 16158191 .
- ^ Chen JC, Chang YS, Wu SL, et al. (2007年9月). 「Chaenomeles speciosaによる大腸菌の易熱性腸毒素誘発性下痢の抑制」J Ethnopharmacol . 113 (2): 233–9 . doi :10.1016/j.jep.2007.05.031. PMID 17624704.
- ^ 米国国立医学図書館. 「GM1ガングリオシドーシス」. Genetic Home Reference . 2013年10月26日閲覧。
- ^ Bansal AS, Abdul-Karim B, Malik RA, et al. (1994). 「自己免疫疾患または神経障害患者および対照群におけるIgMガングリオシドGM1抗体」J. Clin. Pathol . 47 (4): 300–2 . doi :10.1136/jcp.47.4.300. PMC 501930. PMID 8027366 .
- ^ 入江 誠・斎藤 剛・金澤 暢・他 (1997). 「抗ガングリオシド抗体とギラン・バレー症候群の臨床的特徴との関連」.内科医学. 36 (9): 607–12 . doi : 10.2169/internalmedicine.36.607 . PMID 9313102.
- ^ トーマス・ジェファーソン大学(2012年12月)「パーキンソン病に対するGM1ガングリオシドの効果」Clinical Trials.gov。
- ^ マクドナルド、ジョン(1999年9月)「損傷した脊髄の修復」サイエンティフィック・アメリカン:69ページ。