プルシアンブルー
 | |
| 名前 | |
|---|---|
| IUPAC名 鉄(II,III)ヘキサシアニド鉄(II,III)酸塩 | |
その他の名前
| |
| 識別子 | |
| |
3Dモデル(JSmol) | |
| チェビ |
|
| チェムブル | |
| ケムスパイダー |
|
| ECHA 情報カード | 100.034.418 |
| EC番号 |
|
| 1093743 | |
PubChem CID | |
| ユニイ |
|
CompToxダッシュボード(EPA) | |
| |
| |
| プロパティ | |
| C 18 Fe 7 N 18 | |
| モル質量 | 859.239 g·mol −1 |
| 外観 | 青い不透明な結晶 |
| 不溶性 | |
| 構造 | |
| 面心立方格子、cF43 | |
| Fm 3 m、No. 225 [ 1 ] | |
| 薬理学 | |
| V03AB31 ( WHO ) | |
| オーラル | |
| 危険 | |
| 安全データシート(SDS) | MSDS プルシアンブルー |
| 関連化合物 | |
その他の陽イオン | |
特に記載がない限り、データは標準状態(25 °C [77 °F]、100 kPa)における材料のものです。 | |
プルシアンブルー(ベルリンブルー、ブランデンブルクブルー、パリジャンブルー、パリブルーとも呼ばれる)は、フェロシアン化第一鉄塩の酸化によって生成される濃い青色の顔料です。化学式はFe 4 [Fe( CN ) 6 ] 3です。鉄の酸化状態が+3であるFe 3+陽イオンと、鉄の酸化状態が+2である[Fe(CN) 6 ] 4−陰イオンで構成されているため、この塩の別名はヘキサシアノ鉄(II)酸鉄(III)です。ターンブルブルーは化学的には基本的に同一ですが、異なる試薬から作られるため、不純物と粒子サイズが異なり、色がわずかに異なります。
プルシアンブルーは18世紀初頭に作られ、近代初の合成顔料です。水に溶けないため、非常に微細なコロイド分散液として調製されます。プルシアンブルーには様々な量の他のイオンが含まれており[ 2 ]、その外観はコロイド粒子のサイズに大きく依存します。この顔料は絵具に使用され、19世紀の日本の木版画「藍摺り絵」で顕著に見られ、製図図面における伝統的な「青」となっています。
医学においては、経口投与されるプルシアンブルーは、タリウム(I)やセシウムの放射性同位元素などによる特定の重金属中毒の解毒剤として用いられています。この治療法は、プルシアンブルーのイオン交換特性と特定の「ソフト」金属陽イオンに対する高い親和性を利用しています。プルシアンブルーは、世界保健機関(WHO)の必須医薬品リストに掲載されており、基本的な保健システムにおいて最も重要な医薬品です。[ 3 ]
プルシアンブルーは、そこから得られる青酸(シアン化水素)にその名を冠しています。ドイツ語では、シアン化水素は「Blausäure(青い酸)」と呼ばれます。
歴史

プルシアンブルー顔料は、エジプト青の合成に関する知識が失われて以来、初めて広く使用された、安定性と比較的耐光性に優れた青色顔料であるという点で重要です。ヨーロッパの画家たちは、それ以前にも藍染料、スマルト、ティリアンパープル、そしてラピスラズリから作られた非常に高価なウルトラマリンなど、様々な顔料を使用していました。同様に、日本の画家や木版画家たちも、ヨーロッパからプルシアンブルーを輸入し始めるまで、耐久性のある青色顔料を利用することができませんでした。[ 4 ]
プルシアンブルーFe 7 ( CN ) 18(Fe 4 [Fe(CN) 6 ] 3 ·xH 2 Oとも呼ばれる)は、おそらく1706年頃にベルリンで絵の具製造業者ヨハン・ヤコブ・ディースバッハによって初めて合成されました。[ 5 ] [ 6 ]この顔料は、ディースバッハが赤いコチニール染料を作るために血液で汚染されたカリを使用したときに偶然に作られたと考えられています。元の染料には、カリ、硫酸鉄、乾燥したコチニールが必要でした。代わりに、血液、カリ、硫酸鉄が反応して鉄フェロシアン化物と呼ばれる化合物が生成され、これは目的の赤色顔料とは異なり、非常に独特な青色をしています。[ 7 ]これは1709年に最初の貿易業者によってPreußisch blauおよびBerlinisch Blauと命名されました。 [ 8 ] [ 9 ] [ 10
この顔料はすぐに高価なラピスラズリ由来のウルトラマリンに取って代わり、1708年から1716年にかけてヨハン・レオンハルト・フリッシュとプロイセン科学アカデミー会長ゴットフリート・ヴィルヘルム・ライプニッツの間で交わされた書簡の中でも重要な話題となった。 [ 8 ]フリッシュがライプニッツに1708年3月31日に書いた書簡の中で初めて言及されている。1708年には、フリッシュはこの顔料をヨーロッパ中で宣伝し、販売し始めた。1709年8月までに、この顔料はPreussisch blauと名付けられ、1709年11月にはドイツ語名のBerlinisch Blau がフリッシュによって初めて使用された。フリッシュ自身が、1710年の論文Notitia Coerulei Berolinensis nuper inventiでプルシアンブルーについて初めて公表した人物であることが、彼の書簡から推測できる。ディースバッハは1701年頃からフリッシュのために働いていた。

現在までに、ピーテル・ファン・デル・ヴェルフ(ポツダム、サンスーシ絵画館)による1709年の「キリストの埋葬」が、プルシアンブルーが使用された最古の絵画として知られています。1710年頃、プロイセン宮廷の画家たちはすでにこの顔料を使用していました。ほぼ同時期にプルシアンブルーはパリに伝わり、アントワーヌ・ヴァトー、そして後に後継者のニコラ・ランクレとジャン=バティスト・パテールが絵画に使用しました。[ 5 ] [ 11 ]フランソワ・ブーシェは、青と緑の両方にこの顔料を広く使用しました。[ 12 ]
1731年、ゲオルク・エルンスト・シュタールはプルシアンブルーの最初の合成に関する論文を発表しました。[ 13 ]この話にはディースバッハだけでなく、ヨハン・コンラート・ディッペルも関わっています。ディースバッハはコチニール色素から赤色のレーキ顔料を作ろうとしていましたが、使用していたカリが汚染されていたために青色になってしまいました。彼はディッペルからカリを借用し、ディッペルはそれを使って動物油を製造していました。この文脈でディッペルについて言及している史料は他に知られていません。そのため、今日この話の信憑性を判断することは困難です。1724年、ジョン・ウッドワードによってようやくレシピが発表されました。[ 14 ] [ 15 ] [ 16 ]
1752年、フランスの化学者ピエール・J・マッケールは、プルシアンブルーを還元して鉄塩と新しい酸を得、それを使って染料を再構成できることを示す重要な一歩を踏み出しました。[ 17 ]この新しい酸であるシアン化水素は、純粋なプルシアンブルーから初めて単離され、1782年にスウェーデンの化学者カール・ヴィルヘルム・シェーレによって特徴付けられました。[ 18 ]プルシアンブルーに由来するため、最終的にBlausäure (文字通り「青い酸」)と名付けられ、英語では一般に青酸として知られるようになりました。プルシアンブルーの製造過程で形成される無色の陰イオンであるシアン化物は、ギリシャ語で濃い青を意味する言葉に由来する名前です。
1800年代後半、ラジンのハシディズムの指導者であるゲルション・ヘノック・ライナー師は 、セピアを混ぜたプルシアンブルーでツィツィヨットを染め、これが真のテケイル染料であると信じていました。人工的に作られたものであるため、それがテケイル染料であるかどうか疑問視する声もあり、ライナー師がこの事実を知っていたならば、自分の染料がテケイルであるという主張を撤回しただろうと主張する者もいます。[ 19 ]一方、これに異議を唱え、ライナー師は撤回しなかっただろうと主張する者もいます。[ 20 ]
軍事シンボル

18世紀初頭から、プロイセン軍の歩兵連隊と砲兵連隊では、プルシアンブルーが制服のコートの主な色として使われていました。[ 21 ]この色合いはドゥンケルブラウ(濃い青)として象徴的な重要性を獲得し、第一次世界大戦の勃発まで、ほとんどのドイツ兵が儀式や非番の際に着用し続け、その後、緑がかった灰色のフィールドグレー(フェルトグラウ)に取って代わられました。[ 22 ]
合成
プルシアンブルーは、フェロシアン化第一鉄塩の酸化によって生成される。この白色固体は、化学式Mで表される。2Fe[Fe(CN)6]ここでM+=ナ+またはK+この物質に含まれる鉄はすべて第一鉄であるため、混合原子価に伴う濃い色は見られません。この白色固体を過酸化水素または塩素酸ナトリウムで酸化すると、フェリシアン化物が生成され、プルシアンブルーが得られます。[ 23 ]
実際にはコロイド状の「可溶性」形態であるKFe 3+ [Fe 2+ (CN) 6 ]は、フェロシアン化カリウムと鉄(III) から作ることができます。
K + + Fe 3+ + [Fe 2+ (CN) 6 ] 4− → KFe 3+ [Fe 2+ (CN) 6 ]
フェリシアン化カリウムと鉄(II)の同様の反応では、 [Fe 3+ (CN) 6 ] 3−がフェロシアン化物に変換される ため、同じコロイド溶液が生成されます。
上記の反応に過剰の Fe(III) を加えると、「不溶性」のプルシアンブルーが得られます。
4Fe 3+ + 3[Fe 2+ (CN) 6 ] 4− → Fe 3+ [Fe 3+ Fe 2+ (CN) 6 ] 3 [ 24 ]
プルシアンブルーはシアン化物塩から作られるにもかかわらず、シアン化物基が鉄に強く結合しているため毒性はありません。[ 25 ]フェロシアン化物(( Fe2 + (CN) 6 ) 4−)とフェリシアン化物(( Fe3 + (CN) 6 ) 3−)はどちらも、シアン化物イオンへの強い鉄配位により、特に安定しており毒性のない高分子シアノメタレートです。シアン化物は一般にクロムなどの遷移金属とよく結合しますが、これらの非鉄配位化合物は鉄シアン化物ほど安定していないため、CN−イオンの放出リスクが高まり、その結果、比較的毒性が高くなります。[ 26 ]
ターンブルの青

かつて、フェリシアン化物溶液に鉄(II)塩を加えると、プルシアンブルーとは異なる物質が得られると考えられていました。この生成物は伝統的にターンブルブルー(TB)と呼ばれていました。しかし、 X線回折法と電子回折法によって、PBとTBの構造は同一であることが示されました。[ 27 ] [ 28 ] TBとPBの色の違いは、沈殿方法の微妙な違いを反映しており、粒子サイズと不純物含有量に大きく影響します。
プルシアンホワイト
プルシアンホワイト(ベルリンホワイト、エベレット塩とも呼ばれる)は、プルシアンブルーの完全還元型のナトリウム端成分であり、鉄はすべてFe(II)として存在する。これは、式Na 2 Fe[Fe(CN) 6 ]で表されるFe(II)のヘキサシアノ鉄酸ナトリウムである。 [ 29 ]分子量は314 g/molである。[ 29 ]
Na +陽イオンをK +陽イオンに置換することを可能にするより一般的な式は、 A (2−x) B x Fe 2 (CN) 6(AまたはB = Na +またはK +)です。
プルシアンホワイトはプルシアンブルーと近縁ですが、結晶構造、分子骨格の細孔サイズ、および色が著しく異なります。立方晶ナトリウムプルシアンホワイトNa (2−x) K x Fe 2 (CN) 6 ·yH 2 OとカリウムプルシアンホワイトK (2−x) Na x Fe 2 (CN) 6 · yH 2 Oは、 Naイオン電池の正極材料の候補です。[ 30 ]カリウムプルシアンホワイトのフレームワークにNa +およびK +カチオンを挿入すると、好ましい相乗効果が得られ、長期電池安定性が向上し、再充電サイクルの数が増え、耐用年数が長くなります。 [30] Na +およびK +カチオンを容易に収容できるプルシアンホワイトの大きなフレームワークは、充放電サイクル中にそれらの挿入とそれに続く抽出を促進します。広くて剛性の高いホスト結晶構造は、多くのサイクルを経てナトリウム電池に発生する内部膨張応力と歪みに対する体積安定性に貢献します。 [ 29 ]この材料はまた、低温でも高い再充電率を提供しながら、高いエネルギー密度(Ah/kg)の見通しを提供します。 [ 29 ]
プロパティ
プルシアンブルーは微結晶性の青い粉末です。不溶性ですが、結晶子はコロイドを形成する傾向があります。このようなコロイドは微細なフィルターを通過することができます。[ 2 ]プルシアンブルーは最も古い合成化合物の一つであるにもかかわらず、その組成は長年不明のままでした。その正確な同定は、以下の3つの要因によって困難を極めていました。
- プルシアンブルーは非常に不溶性であるが、コロイドを形成する傾向がある。
- 従来の合成法では不純な化合物が得られる傾向がある
- 純粋なプルシアンブルーでさえ構造が複雑で、通常の結晶構造解析では分析できない。
結晶構造



不溶性プルシアンブルーの化学式はFe 7 (CN) 18 · x H 2 O(x = 14–16)である。構造はIR分光法、メスバウアー分光法、 X 線結晶構造解析、中性子結晶構造解析によって決定された。X線回折では鉄などの重い元素が存在すると炭素と窒素を容易に区別できないため、これらの軽い元素の位置は分光学的手段と鉄原子中心からの距離の観察によって推定される。中性子回折はN原子とC原子を容易に区別できるため、プルシアンブルーとその類似体の詳細な構造を決定するために使用されている。[ 31 ] [ 32 ] [ 33 ] [ 34 ] [ 35 ] [ 36 ] [ 37 ] [ 38 ] [ 39 ] [ 40 ] [ 41 ]
PBは面心立方格子構造を持ち、単位格子あたり4つの鉄(III)イオンを有する。「可溶性」PB結晶は格子間K +イオンを含むが、不溶性PBは格子間水を含む。理想的な不溶性PB結晶では、立方骨格はFe(II)-C-N-Fe(III)配列から構成され、Fe(II)-炭素間距離は1.92Å 、 Fe(III)-窒素間距離は2.03Åである。Fe (CN) 6サブユニットの4分の1のサイト(おそらくランダム)は空であり、単位格子あたり平均3つのグループが残る。[ 42 ]空の窒素サイトは、代わりにFe(III)に配位した水分子で満たされる。

低スピンのFe(II)中心は、八面体構造で6つの炭素配位子に囲まれている。高スピンのFe(III)中心は、平均4.5個の窒素原子と1.5個の酸素原子(6つの配位水分子の酸素)に囲まれた八面体構造となっている。単位格子内には、約8個の(格子間)水分子が、孤立した分子として、あるいは配位水に水素結合した状態で存在する。可溶性のヘキサシアノ鉄酸塩では、Fe(IIまたはIII)は常にシアン化物の炭素原子に配位しているが、結晶性のプルシアンブルーでは、FeイオンはCとNの両方に配位していることは注目に値する。[ 43 ]
格子欠陥の存在により、組成は非常に変動しやすいことで知られています。水分子が構造内に取り込まれ、陽イオン空孔を占有することで、様々な程度に水和します。プルシアンブルーの組成の変動性は、その低い溶解度に起因しており、固体と液体の完全な平衡に達する前に急速に沈殿します。 [ 42 ] [ 44 ]
色
プルシアンブルーは強い色をしており、油絵の具に混ぜると黒や濃紺になる傾向があります。正確な色調は、粒子の大きさを決定する製造方法に依存します。プルシアンブルーの鮮やかな青色は、Fe(II)からFe(III)への電子移動のエネルギーに関連しています。 [ 45 ]このような混合原子価化合物の多くは、電子間電荷移動の結果として特定の波長の可視光を吸収します。この場合、波長680ナノメートル付近の赤色光が吸収され、その結果、反射光は青色に見えます。[ 46 ]
他の高彩度顔料と同様に、プルシアンブルーはコンピュータのディスプレイ上で正確に表示できません。プルシアンブルーはエレクトロクロミック性を有し、還元されると青色から無色に変化します。この変化はFe(III)からFe(II)への還元によって起こり、プルシアンブルーの色の原因となる電子間電荷移動が消失します。
使用
顔料

プルシアンブルーは、製造が容易で、安価で、毒性がなく、鮮やかな色をしているため、多くの用途に用いられてきました。発明後すぐに顔料として採用され、油絵の具、水彩絵の具、染色に広く利用されました。[ 48 ]主な用途は顔料で、黒や青みがかったインクに使用するために、年間約12,000トンのプルシアンブルーが生産されています。他の様々な顔料にもプルシアンブルーが含まれています。[ 23 ]エンジニアーズブルーとシアンタイプで形成された顔料は、ブループリントという一般名が付けられています。かつてはプルシアンブルー(後にミッドナイトブルーと改名)で着色されたクレヨンもありました。同様に、プルシアンブルーは洗濯物のブルーイングにも使われています。
欧州連合ナノマテリアル観測所によると、プルシアンブルーのナノ粒子は一部の化粧品原料の顔料として使用されている。
| プルシアンブルー | |
|---|---|
| 六角形のトリプレット | #003153 |
| sRGB B ( r , g , b ) | (0、49、83) |
| HSV ( h , s , v ) | (205°、100%、33%) |
| CIELCh uv ( L , C , h ) | (19、30、247°) |
| ソース | swiss.csail.mit.edu [ 49 ] |
| B : [0–255] (バイト) に正規化H : [0–100] (百) に正規化 | |
薬
プルシアンブルーは一価金属陽イオン(Me + )を取り込む能力があるため、特定の毒性重金属の金属イオン封鎖剤として有用です。特に医薬品グレードのプルシアンブルーは、タリウム(Tl +)または放射性セシウム(134 Cs +、137 Cs + )を摂取した人に使用されます。国際原子力機関(IAEA)によると、成人男性は1日に少なくとも10gのプルシアンブルーを摂取しても深刻な害はありません。米国食品医薬品局(FDA)は、「承認された新薬申請の条件下で製造された500mgのプルシアンブルーカプセルは、特定の中毒症例において安全かつ効果的な治療法となる可能性がある」と判定しています。[ 50 ] [ 51 ]ラジオガルダーゼ(プルシアンブルー不溶性カプセル[ 52 ] )は、セシウム137を腸管から除去するための市販製品であり、セシウム137の腸肝循環に介入することで間接的に血流から除去し、[ 53 ]体内滞留時間(および被曝量)を約3分の2に短縮します。特に、ブラジルのゴイアニア事故で被ばくした人々からセシウム137 +を吸着・除去するために使用されました。 [ 2 ]
鉄の汚れ
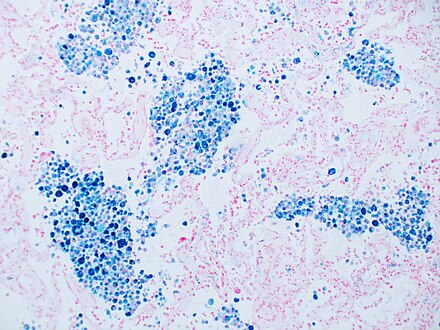
プルシアンブルーは、病理学者が骨髄サンプルなどの生検標本中の鉄の存在を検出するために用いる一般的な組織病理学的染色法です。歴史的には(1867年)、発明者であるドイツ人病理学者マックス・パールズ(1843~1881年)にちなんで「パールズ・プルシアンブルー」と呼ばれていた最初の染色法は、組織を染色するためにフェロシアン化カリウムと酸の別々の溶液を使用していました(現在では、染色直前にこれらを混合して使用します)。組織に沈着した鉄は、その場で紫色のプルシアンブルー染料を形成し、青色または紫色の沈着物として観察されます。[ 54 ]
- プルシアンブルー染色。ヘモシデリン色素を青色に強調表示します。
- プルシアンブルー染色
機械工と工具製作者によって
エンジニアズブルー(油性顔料のプルシアンブルー)は、定盤やベアリングなどの金属表面に手作業でスクレーピングを行う際に、従来から使用されている塗料です。乾燥しないペースト状の薄い層を基準面に塗布し、ワークピースの凹凸に転写します。その後、工具製作者は、マーキングした凹凸を削ったり、石で研磨したり、その他の方法で除去します。プルシアンブルーは、多くの研磨顔料のように非常に精密な基準面を摩耗させないため、好まれています。その他の用途としては、組み立て時に歯車の歯にマーキングして、その接合面の特性を確認することなどがあります。
プルシアンブルーは、乾燥状態でも使用され、原材料上に部品の形状をレイアウトします。機械工はプルシアンブルーを塗布し、ノギスや高さゲージなどの工具を用いて加工する形状を刻みます。プルシアンブルーはこの用途で重宝されます。なぜなら、塗膜に刻まれた線によって、機械工はプリックパンチなどのマーキングツールを用いて形状を正確に把握できるからです。
分析化学では
プルシアンブルーは、総フェノールのプルシアンブルー分析で生成される。試料とフェノール標準物質に酸性塩化第二鉄(III)とフェリシアン化物を加えると、フェノールによってフェロシアン化物に還元される。塩化第二鉄とフェロシアン化物は反応してプルシアンブルーを生成する。試料の700 nmにおける吸光度を標準物質と比較することで、総フェノールまたはポリフェノールを定量することができる。[ 55 ] [ 56 ]
家庭用
プルシアンブルーは、ミセス・スチュワートのブルーイングなどの洗濯用ブルーイング剤に含まれています。[ 57 ]
研究
電池材料

プルシアンブルー(PB)は、1978年以来、電気化学的エネルギー貯蔵への応用について研究されてきました。[ 58 ]プルシアンブルー本体(Fe-Fe固体)は、K +溶液中で2つの明確に定義された可逆的な酸化還元遷移を示します。弱く溶媒和したカリウムイオン(図示されていないRb +とCs +も同様)は、溶媒和半径を持ち、プルシアンブルーの骨格に適合します。一方、溶媒和したNa +とLi +のサイズはPBキャビティには大きすぎるため、これらのイオンのインターカレーションは妨げられ、非常に遅くなります。サイクリックボルタンメトリーにおける低電圧と高電圧のピークのセットは、1と2/3それぞれFe原子1個あたりの電子数である。[ 59 ]高い電圧セットは、 C原子に配位した低スピンFeイオンにおけるFe 3+ /Fe 2+遷移によるものである。低い電圧セットは、N原子に配位した高スピンFeイオンによるものである。[ 60 ] [ 61 ] [ 62 ]
PB中のFe金属中心をMn、Co、Ni、Znなどの他の金属イオンに置換することで、電気化学的に活性なプルシアンブルー類似体(PBA)を形成できます。PB/PBAおよびその誘導体は、リチウムイオン電池、ナトリウムイオン電池、カリウムイオン電池における可逆的なアルカリイオン挿入・抽出のための電極材料としても評価されています。
参照
- ブルービリー - 化学産業の排水によって汚染された土壌に形成されたプルシアンブルーの堆積物
- 青色顔料
- コバルトブルー – 青色顔料
- クリスタルバイオレット – トリアリールメタン染料
- フルオレセイン – 染料や蛍光トレーサーとして使用される合成有機化合物
- 漢紫と漢青 – 古代中国で開発された顔料
- 無機顔料の一覧
- ミッドナイトブルー – 濃い青
- フタロシアニンブルーBN – フタロシアニン染料のグループに属する合成青色顔料リダイレクト先の簡単な説明を表示するページ
大衆文化において
「Wear Your Love Like Heaven」は、イギリスのシンガーソングライター、ドノヴァンが1967年にリリースした曲であり、アメリカのシングルです。最初の歌詞は「Color in sky, Prussian blue」です。
参考文献
- ^ Fuess, H. (2010年7月20日).国際結晶学表A巻(2016年版). Wiley. ISBN 978-0-470-68575-4。
- ^ a b c Dunbar, KR & Heintz, RA (1997).遷移金属シアン化物化合物の化学:現代の展望. 無機化学の進歩. 第45巻. pp. 283– 391. doi : 10.1002/9780470166468.ch4 . ISBN 9780470166468。
- ^ 「WHO必須医薬品モデルリスト」(PDF)世界保健機関2013年10月2014年4月22日閲覧。
- ^セントクレア、カシア(2016年)『色彩の秘密の生活』ロンドン:ジョン・マレー、pp. 189– 191. ISBN 9781473630819. OCLC 936144129 .
- ^ a b Bartoll, Jens. 「絵画におけるプルシアンブルーの初期の使用」(PDF) .第9回国際美術非破壊検査会議、イスラエル、エルサレム、2008年5月25~30日. 2010年1月22日閲覧。
- ^ベルガー、JE (c.1730) Kern aller Fridrichs=Städtschen Begebenheiten。ベルリン国立図書館 - プロイッシャー文化センター、ハンドシュリフテンアブテイルング、ボルス女史。クォート。 124.
- ^フィンレイ、ヴィクトリア(2014年)『美術における色彩の華麗なる歴史』J・ポール・ゲティ美術館、pp. 86– 87. ISBN 978-1606064290。
- ^ a b Frisch, JL (1896) Briefwechsel mit Gottfried Wilhelm Leibniz LH Fischer (編)、ベルリン、Stankiewicz Buchdruck、再版ヒルデスハイム/ニューヨーク: Georg Olms Verlag、1976
- ^ JL フリッシュ (1710)。「Serius Exhibitiona. Notitia Coerulei Berolinensis nuper inventi」 [追記。最近発見されたベルリンブルーに関する情報。Miscellanea Berolinensia Ad Incrementum Scientiarum (ラテン語)。1 : 377–378。
- ^クラフト、アレクサンダー(2011年)。「プルシアンブルーに関する最初の論文発表300周年を記念した『Notitia Coerulei Berolinensis nuper inventi』」(PDF) .化学史紀要. 36 (1): 3– 9. doi : 10.70359/bhc2011v036p003 . PMID 21612121 .
- ^ Bartoll, J.; Jackisch, B.; Most, M.; Wenders de Calisse, E.; Vogtherr, CM (2007). 「初期のプルシアンブルー:プロイセン王フリードリヒ2世所蔵のヴァトー、ランクレ、ペイターの絵画における青と緑の顔料」Techné . 25 : 39–46 .
- ^ムルヘロン、ジェイミー (2001). 「プルシアンブルー、ブーシェ、ニュートン:ロココ絵画の素材、実践、理論」『オブジェクト(3): 68–93』
- ^シュタール、ゲオルク・エルンスト (1731)。Georgii Ernesti Stahlii、Experimenta、Observationes、Animadversiones、CCC Numero、Chymicae Et Physicae: Qualium alibi vel nulla、vel rara、nusquam autem satis ampla、ad debitos nexus、および veros usus、deducta mentio、commemeratio、aut explicatio、invenitur。 Qualium Partim、別名 Autoris scriptis、variamentio fata habetur; Partim Autem nova commemoratio hoc Tractatu exhibetur: utrimque vero, universa res uberius explicatur atqueconfirmatur (ラテン語)。ハウデ。
- ^ Woodward, J. (1724–1725). "Praeparatio coerulei Prussiaci es Germanica missa ad Johannem Woodward." [ドイツからジョン・ウッドワードに送られたプルシアンブルーの調製…]. Philosophical Transactions of the Royal Society of London . 33 (381): 15– 17. doi : 10.1098/rstl.1724.0005 .
- ^ブラウン、ジョン (1724–1725). 「前述の準備に関する観察と実験」 .哲学論文集. 33 (381): 17– 24. Bibcode : 1724RSPT...33...17B . doi : 10.1098/rstl.1724.0006 . JSTOR 103734 . 。このレシピはその後、Geoffroy, Étienne-François (1727) "Observations sur la Preparation de Bleu de Prusse ou Bleu de Berlin" Mémoires de l'Académie Royale des Sciences année 1725に出版されました。パリ。 153–172ページ。
- ^ 「18世紀ヨーロッパにおける色の創造:プルシアンブルー」 www.gutenberg-e.org . 2022年7月28日閲覧。
- ^ Macquer, Pierre-Joseph (1752) "Éxamen chymique de bleu de Prusse"、Mémoires de l'Académie Royale des Sciences année 1752 ... (パリ、1756)、60–77 ページ。この記事は、「Sur le bleu de Prusse」、Histoire de l'Académie Royale des Sciences ... (1752)、(Paris、1756)、79 ~ 85 ページでレビューされました。
- ^カール W. シェーレ (1782)「Försök, beträffande det färgande ämnet uti Berlinerblå」 (ベルリン ブルーの着色物質に関する実験)、 Kungliga Svenska VetenskapsakademiensHandlingar (スウェーデン王立科学アカデミー論文集)、 3 : 264–275 (スウェーデン語)。ラテン語で「De materia tingente caerulei berolinensis」として転載:Carl Wilhelm Scheele with Ernst Benjamin Gottlieb Hebenstreit (ed.) and Gottfried Heinrich Schäfer (trans.)、 Opuscula Chemica et Physica (Leipzig ("Lipsiae")、(ドイツ): Johann Godfriedミュラー、1789)、vol. 2、148~174ページ。
- ^テクヘレット#セピア・オフィシナリスを参照
- ^ “聖書に登場する青いテケイル染料の原料、長い間失われていたチラゾンが再発見されたのか?” 2008年4月8日。 2008年4月8日時点のオリジナルよりアーカイブ。 2020年5月12日閲覧。
- ^ヘイソーンスウェイト、フィリップ(1991)『フリードリヒ大王の軍隊―歩兵』ブルームズベリーUSA、p.14、 ISBN 1855321602
- ^ブル、スティーブン(2000年)『第一次世界大戦:ドイツ軍』ブラッシー社、pp.8-10、 ISBN 1-85753-271-6
- ^ a bフェルツ、ハンス G.他。 (2006) ウルマン工業化学百科事典の「顔料、無機」。ワイリー-VCH、ワインハイム。土井: 10.1002/14356007.a20_243.pub2。
- ^エゴン・ウィバーグ、ニルス・ウィバーグ、アーノルド・フレデリック・ホレマン著『無機化学』p.1444. アカデミック・プレス、2001年; Googleブックス
- ^毒物学ジャーナル、フェリシアン化カリウムの摂取による自殺未遂
- ^ Jonathan R. Thurston、Scott E. Waters、Brian H. Robb、Michael P. Marshak (2022年3月). 「有機および金属有機RFB」.エネルギー貯蔵百科事典. 第2巻. pp. 423– 435. doi : 10.1016/B978-0-12-819723-3.00082-2 . ISBN 9780128197301. S2CID 236672995 .
{{cite book}}: CS1 maint: 複数の名前: 著者リスト (リンク) - ^尾関 徹; 松本 幸一; 引目 誠一郎. (1984). 「プルシアンブルーの光音響スペクトルとフェリシアン化鉄(III)の光化学反応」.分析化学. 56 (14): 2819. doi : 10.1021/ac00278a041 .
- ^ Izatt, Reed M. ; Watt, Gerald D. ; Bartholomew, Calvin H. ; Christensen, James J. (1970). 「プルシアンブルーとターンブルブルー生成の熱量測定による研究」 .無機化学(投稿原稿). 9 (9): 2019. doi : 10.1021/ic50091a012 .
- ^ a b c d「Prussian White」 . Macsen Labs . 2023年10月28日. 2024年3月16日閲覧。
- ^ a bピエルナス=ムニョス、マリア・ホセ;カスティージョ・マルティネス、エリザベス。ボンダルチュク、オレクサンドル。アルマン、ミシェル。ロホ、テオフィロ (2016)。 「Naイオン電池用の高電圧プラトーキュービックプルシアンホワイト」。電源ジャーナル。324 .エルゼビア: 766– 773。Bibcode : 2016JPS...324..766P。土井: 10.1016/j.jpowsour.2016.05.050。ISSN 0378-7753。
- ^多核遷移金属シアン化物の電気化学 - プルシアンブルーとその類似体。1986年。化学研究報告。19/162-168。doi: 10.1021 /ar00126a001。
- ^高性能リチウムイオン電池の安定ホスト材料としての低欠陥FeFe(CN) 6フレームワーク。2016年ACS Applied Materials and Interfaces誌、8/23706-23712号。doi : 10.1021/acsami.6b06880。
- ^電気化学的エネルギー貯蔵のためのプルシアンブルー類似体とその派生材料:期待と課題。2024年。材料研究速報。170/ doi : 10.1016/j.materresbull.2023.112593。
- ^プルシアンブルー電池のいくつかの性能特性。1985年電気化学協会誌。132/1382-1384。doi: 10.1149/1.2114121。
- ^プルシアンブルー、Fe 4 [Fe 4 (CN) 6 ] 3の中性子回折研究。 14D 2 O. 1974。ツァイシュリフト毛皮物理化学。 92/354-357。土井: 10.1524/zpch.1974.92.4-6.354。
- ^プルシアンブルーFe(III) 4 [Fe( II )(CN) 6 ] 3 ·xD 2 Oの原子価非局在化、偏光中性子回折法による。1980年。Helvetica Chimica Acta。63/148-153。doi: 10.1002/hlca.19800630115。
- ^プルシアンブルーFe 4 [Fe(CN) 6 ] 3 ·xH 2 Oの中性子回折研究。水分子の位置と長距離磁気秩序。1980年。無機化学。19/956-959。doi: 10.1021/ic50206a032。
- ^プルシアンブルーと構造的に関連する化合物の粉末および単結晶の中性子およびX線回折研究。1999年。Zeitschrift fur Naturforschung – Section B Journal of Chemical Sciences。54/870-876。doi: 10.1515/znb-1999-0708。
- ^プルシアンブルーの結晶性混合原子価マンガン類似体:磁気、分光学、X線および中性子回折研究。2004年アメリカ化学会誌。126/16472-16477. doi : 10.1021/ja0465451。
- ^中性子回折および中性子振動分光法によるプルシアンブルー類似体Cu 3 [Co(CN) 6 ] 2 の水素吸着の研究。2006年。材料化学。18/3221-3224。doi: 10.1021/cm0608600。
- ^分子磁性化合物Ni 1.125 Co 0.375 [Fe(CN) 6 ]·6.4H 2 Oの中性子回折研究。 2006年。Physica B:凝縮物質。385-386 I / 444-446。doi: 10.1016 / j.physb.2006.05.147。
- ^ a b c Herren, F.; Fischer, P.; Ludi, A.; Haelg, W. (1980). 「プルシアンブルー Fe 4 [Fe(CN) 6 ] 3 ·xH 2 O の中性子回折研究:水分子の位置と長距離磁気秩序」.無機化学. 19 (4): 956. doi : 10.1021/ic50206a032 .
- ^プルシアンブルー類似体とその派生材料を用いた電気化学的エネルギー貯蔵:期待と課題。2024年。Materials Research Bulletin。170/。M. Fayaz、W. Lai、J. Li、W. Chen、X. Luo、Z. Wang、他。doi: 10.1016 /j.materresbull.2023.112593
- ^ Lundgren, CA; Murray, Royce W. (1988). 「プルシアンブルー膜の組成とその電気化学に関する観察」.無機化学. 27 (5): 933. doi : 10.1021/ic00278a036 .
- ^ Robin, Melvin B. (1961年11月20日). 「プルシアンブルーの色と電子配置」 .無機化学. 1 (2): 337– 342. doi : 10.1021/ic50002a028 – acs.org経由.
- ^ Cheng, Ming; Peng, Wei; Hua, Peng; Chen, Zhengrong; Sheng, Jia; Yang, Juan; Wu, Yongyou (2017-03-24). 「光音響イメージングおよび癌の光熱療法のためのpH応答性プルシアンブルーのin situ形成」 . RSC Advances . 7 (30): 18270– 18276. Bibcode : 2017RSCAd...718270C . doi : 10.1039/C7RA01879G . ISSN 2046-2069 .
- ^ 「ビッグベンの時計の文字盤が青に変わる」英国議会。 2023年10月21日閲覧。
- ^ベリー、バーバラ・H. (1997). 「プルシアンブルー」.EW・フィッツヒュー編『アーティストの顔料:その歴史と特性ハンドブック』. ワシントンD.C.: ナショナル・ギャラリー. ISBN 0894682563。
- ^ 「Project MAC Home Page」(PDF) 。2007年2月26日時点のオリジナル(PDF)からのアーカイブ。
- ^ 「プルシアンブルーに関する質問と回答」食品医薬品局. 2009年7月10日時点のオリジナルよりアーカイブ。2020年3月20日閲覧。
- ^ 「カルシウムDTPAと亜鉛DTPAに関する質問と回答(更新)」米国食品医薬品局(FDA)2018年11月3日。 2020年3月21日閲覧。
- ^ Radiogardase:処方箋付きパッケージ添付文書Archived 2011-03-20 at the Wayback Machine
- ^ Heyltex Corporation – Toxicologyアーカイブ2007-11-12 at the Wayback Machine
- ^パールズ・プルシアンブルー染色の処方。2009年4月2日にアクセス。
- ^ Hagerman, Ann E. (2011年3月18日). 「タンニンの化学」(PDF) . 2013年8月26日時点のオリジナル(PDF)からアーカイブ。 2009年12月19日閲覧。 (1.41MB)
- ^ Graham, Horace D. (1992). 「ポリフェノールの測定におけるプルシアンブルー色の安定化」. Journal of Agricultural and Food Chemistry . 40 (5): 801– 805. Bibcode : 1992JAFC...40..801G . doi : 10.1021/jf00017a018 . ISSN 0021-8561 .
- ^シュワルツ、ジョー(2016年1月22日)「正しい化学反応:刑事コロンボ、あなたの洗濯物、そして液体ブルーイング」モントリオール・ガゼット。 2017年2月28日閲覧。
- ^ Neff, Vernon D. (1978-06-01). 「プルシアンブルー薄膜の電気化学的酸化および還元」 . Journal of the Electrochemical Society . 125 (6): 886– 887. Bibcode : 1978JElS..125..886N . doi : 10.1149/1.2131575 . ISSN 1945-7111 .
- ^ Neff, Vernon D. (1985-06-01). 「プルシアンブルー電池の性能特性」. Journal of the Electrochemical Society . 132 (6): 1382– 1384. Bibcode : 1985JElS..132.1382N . doi : 10.1149/1.2114121 . ISSN 0013-4651 .
- ^板谷 金吾; 内田 勇; ネフ, ヴァーノン D. (1986-06-01). 「多核遷移金属シアン化物の電気化学:プルシアンブルーとその類似体」. Accounts of Chemical Research . 19 (6): 162– 168. doi : 10.1021/ar00126a001 . ISSN 0001-4842 .
- ^呉、咸永;シャオ、ミャオミャオ。ウー、チェンハオ。銭、江峰。曹操、玉梁。アイ、シンピン。楊、韓西 (2016-09-14)。 「高性能リチウムイオン電池の安定したホスト材料としての低欠陥 FeFe(CN) 6フレームワーク」。 ACS アプライド マテリアルズとインターフェイス。8 (36): 23706–23712。ビブコード: 2016AAMI....823706W。土井:10.1021/acsami.6b06880。ISSN 1944-8244。PMID 27556906。
- ^ Fayaz, Muhammad; Lai, Wende; Li, Jie; Chen, Wen; Luo, Xianyou; Wang, Zhen; Chen, Yingyu; Li, De; Abbas, Syed Mustansar; Chen, Yong (2024). 「電気化学的エネルギー貯蔵のためのプルシアンブルー類似体とその派生材料:期待と課題」. Materials Research Bulletin . 170 112593. Elsevier. doi : 10.1016/j.materresbull.2023.112593 . ISSN 0025-5408 .
外部リンク
- FDAのプルシアンブルーに関するページ
- CDCのプルシアンブルーに関するページ
- 国家汚染物質目録 – シアン化合物ファクトシート
- ラジオガルダーゼ(プルシアンブルー不溶性カプセル)の販売業者であるHeyltex Corporation。 2020年2月21日にWayback Machineでアーカイブ。
- サラ・ローエンガード「プルシアンブルー」『18世紀ヨーロッパにおける色の創造』コロンビア大学出版、2006年
- プルシアンブルー、ColourLex
- クラフト、アレクサンダー (2008). 「プルシアンブルーの発見と歴史について」(PDF) . Bull. Hist. Chem. 33 (2): 61– 67. doi : 10.70359/bhc2008v033p061 .