医療における金属は、診断および治療の目的で有機系に使用されます。[1]無機元素は、金属タンパク質と呼ばれる酵素の補因子として有機生命体にとって不可欠です。体内の金属が不足または過剰になった場合、介入療法や自然療法によって平衡を自然な状態に戻す必要があります。
有毒金属
金属は大量に摂取すると有毒となる可能性があります。摂取または代謝経路の異常によって金属毒性(金属中毒)を引き起こす可能性があります。有毒金属の発生源としては、タバコ由来のカドミウム、農業由来のヒ素、火山や森林火災由来の水銀などが挙げられます。自然界では、樹木や植物といった形で多くの毒素を捕捉し、異常に高い濃度を正常な状態に戻すことができます。有毒金属中毒は通常、何らかのキレート剤を用いて治療されます。[2] [3] 水銀、カドミウム、鉛などの 重金属中毒は特に有害です。
有毒金属の具体的な例としては次のようなものがあります。
- 銅:銅中毒は通常、銅の蓄積に関与するタンパク質であるセルロプラスミンの低レベルによる副作用として現れます。これはウィルソン病と呼ばれます。ウィルソン病は常染色体劣性遺伝疾患であり、その変異により、銅を胆汁中に輸送し、最終的にセルロプラスミンに取り込むATPaseの機能不全を引き起こします。
- プルトニウム:核時代以降、プルトニウム中毒は特に原子炉作業員にとって潜在的な危険であり、プルトニウムの粉塵を吸入すると、強いアルファ粒子放出のため特に危険です。プルトニウム中毒の症例はごくわずかです。
- 水銀:水銀は通常、農業やその他の環境源から摂取されます。水銀中毒は、治療せずに放置すると神経疾患や腎不全を引き起こす可能性があります。
- 鉄:鉄毒性、鉄中毒、鉄過剰症はよく知られています。鉄はがんのエームス試験ではごく弱陽性反応を示すものの、強力な触媒であり、ATPの生成、ひいてはDNAの生成に不可欠なため、過剰な可溶性鉄は特に経時的に毒性を示します。組織への過剰な鉄の沈着や血流中の鉄濃度の上昇は、アルツハイマー病からマラリアに至るまで、多くのヒト疾患と関連していることが証明されています。植物学では、サハラ以南のアフリカでは、地下水に過剰な鉄分が含まれ、それが作物を中毒させるため、鉄は米、トウモロコシ、小麦などの灌漑において深刻な問題となっています。
- 鉛とカドミウム:鉛中毒とカドミウム中毒は、胃腸障害、腎臓障害、神経障害を引き起こす可能性があります。無鉛塗料と無鉛ガソリンの使用により、鉛重金属中毒の症例数は減少しました。
- ニッケル、クロム、カドミウム:金属とDNAの相互作用により、これらの金属は発がん性を持つ可能性があります。[3]
- ニッケル: 特にジュエリーを介した皮膚と金属の接触により、ニッケルアレルギーがよく起こります。
- 亜鉛、カドミウム、マグネシウム、クロム:金属ヒューム熱はこれらの金属のヒュームを摂取することで引き起こされ、インフルエンザのような症状を引き起こします。
- ベリリウム:ベリリウム中毒のリスクは、微量を超えるベリリウムを含む合金または鉱石を扱う金属加工業者や製鉱業者にとって、労働安全衛生上重要な問題です。合金の場合、これはベリリウムが意図的に含まれている合金を指し、鉱石の場合、これはベリリウムの採取を目的とした鉱石、またはベリリウムが無視できないほど多く含まれる鉱石を指します。
バイオメタル
恒常性
体液と電解質のバランスは、恒常的に絡み合っており、すべての生物の健康に不可欠です。これには、生体金属の陽イオン濃度の基準範囲が含まれており、人間の医学と獣医学に関しては、主に人間、家畜、ペットの血清イオン濃度の基準範囲が含まれます。このような体液と電解質のバランスの乱れは、脱水、過労、下痢の状況で最も頻繁に発生しますが、癌(特に腫瘍随伴症候群)、寄生虫症、先天性代謝異常、およびその他のさまざまな状況でも発生します。内科や内分泌学(特に慢性疾患)や集中治療医学(重篤な急性疾患) など、一部の医療専門分野では、電解質異常が特に頻繁に扱われます。
金属貧血
人間は正常に機能するために、特定の金属を一定量必要とします。ほとんどの金属は酵素の補酵素または補綴物として使用され、特定の反応を触媒し、重要な役割を果たします。人間にとって必須の金属は、ナトリウム、カリウム、マグネシウム、銅、バナジウム、クロム、マンガン、鉄、コバルト、ニッケル、亜鉛、モリブデン、カドミウムです。貧血の症状は、特定の必須金属の欠乏によって引き起こされます。貧血は、栄養失調や代謝異常と関連している可能性があり、通常は遺伝子欠陥によって引き起こされます。[3]
金属貧血の具体的な例としては、以下のものがあります。
- 鉄:一般的な単純性貧血(鉄欠乏症)は、酸素の運搬や利用を担う機能的なヘムタンパク質(ヘモグロビン、ミオグロビンなど)の喪失を引き起こします。悪性貧血は、ビタミンB12(コバルト錯体であるコバラミンを含む)の欠乏によって引き起こされ、赤血球の機能を阻害します。
- 亜鉛:亜鉛貧血は主に食事が原因で、成長遅延を引き起こす可能性があります。
- 銅:乳児の銅貧血は食生活の乱れから起こり、心臓病を引き起こす可能性があります。[3]
診断における金属
核イメージングにおける金属錯体
金属イオンは診断用画像診断によく用いられます。金属錯体は、放射性同位元素イメージング(放出される放射線を利用する)や、磁気共鳴画像(MRI)などの造影剤として用いられます。このような画像診断は、錯体中の配位子を操作して特異性を作り出し、特定の細胞や臓器に取り込まれるようにすることで、より鮮明にすることができます。[3] [4]
診断に使用される金属の例は次のとおりです。
- テクネチウム99mTcは、イメージング目的で最も一般的に使用される放射性同位元素です。半減期が短く、ガンマ線光子のみを放出し、ベータ線やアルファ線(周囲の細胞にダメージを与える)を放出しないため、イメージング用の放射性同位元素として特に適しています。
- ガドリニウム(III)、鉄(III)、マンガン(II):MRI検査では、造影画像を得るために常磁性金属が必要です。ガドリニウム(III)、鉄(III)、マンガン(II)はいずれも常磁性金属であり、組織の緩和時間を変化させ、造影画像を生成することができます。
- ガリウム 68 は、陽電子放出断層撮影の陽電子源として有用です。
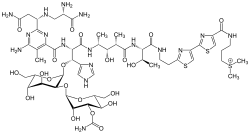
- コバルト(III): 57コバルト(III)は、抗生物質であるブレオマイシン(BLM)(図1)と併用することで、腫瘍細胞に選択的に取り込まれる。コバルトの使用により、血液と腫瘍の分布比は最も良好となるが、半減期が長すぎるため、画像診断には適さない。ブレオマイシンの末端チアゾール環にEDTA基を結合させ、放射性標識することで複合体全体の追跡を可能にするという解決策が提案されている。このシステムは腫瘍の位置を正確に特定することができ、将来的には早期発見とより非侵襲的な手技につながる可能性がある。[3]
MRI画像における金属物体
MRI(磁気共鳴画像法)検査における重要な禁忌は、MRIスキャナーの近く、特にMRIスキャナーの視野内に金属物を置くことです。これは、インプラントの金属プレート、骨ネジ(内固定)、または靱帯結合ネジを装着している人はMRI検査を受けられないことを意味するだけでなく、宝石、ベルトのバックル、財布、ハンドバッグ、警備員の武器など、多くの日常的な物品をMRI検査エリアから遠ざける必要があることを意味します。
治療中の金属
金属は古代から治療に使用されてきました。紀元前1500年のエーベルス・パピルスは、治療における金属の使用に関する最初の記録であり、銅による炎症の軽減や鉄による貧血の治療について記述されています。バナジン酸ナトリウムは20世紀初頭から関節リウマチの治療に使用されてきました。近年、金属はがん細胞を特異的に攻撃し、DNAと直接相互作用することで、がん治療にも利用されています。ほとんどの金属の正電荷は、DNAのリン酸骨格の負電荷と相互作用します。金属を含む薬剤の中には、タンパク質の活性部位に既に存在する他の金属と直接相互作用するものもあれば、還元電位が最も高いアミノ酸と相互作用するために金属を使用する薬剤もあります。[4]

治療に使用される金属の例は次のとおりです。
- 白金:白金系化合物は頭頸部腫瘍に特異的に作用することが示されています。これらの配位錯体は、腫瘍細胞内のDNAを架橋する作用を持つと考えられています(図2)。
- 金:金塩複合体は関節リウマチの治療に用いられてきました(図3)。金塩はアルブミンと相互作用し、最終的には免疫細胞に取り込まれ、抗ミトコンドリア作用を誘発し、最終的には細胞のアポトーシスを誘導すると考えられています。これは関節リウマチの間接的な治療であり、免疫反応を緩和します。
- リチウム:Li 2 CO 3 は躁うつ病の予防治療に使用できます。
- 亜鉛:亜鉛は局所的に傷を治すために使用できます。Zn2 +はヘルペスウイルスの治療に使用できます。
- 銀:銀は火傷患者の火傷部位の感染を防ぐために使用されてきました。
- プラチナ、チタン、バナジウム、鉄: シス DDP (シス-ジアミンジクロロプラチナ)、チタン、バナジウム、鉄は、がん患者の治療において、腫瘍細胞内の DNA と特異的に反応することが示されています。
- 金、銀、銅:金、銀、銅を含むホスフィン配位子化合物には抗癌作用がある。[3]
- ランタン:炭酸ランタンは、フォスレノールという商標名でよく使用され、慢性腎臓病の患者のリン酸結合剤として使用されます。
- ビスマス:次サリチル酸ビスマスは制酸剤として使用されます。
- ジルコニウム:ジルコニウムシクロケイ酸ナトリウムは、慢性腎臓病患者に使用されるカリウム結合剤です。
- ヒ素:三酸化ヒ素は急性前骨髄球性白血病の治療に使用される化学療法薬です。


参照
参考文献
- ^ Gumienna-Kontecka, Elzbieta; Carver, Peggy L. (2019-01-14). 「7. トロイの木馬の構築:感染症治療のためのシデロフォア-薬物複合体」.医学における必須金属:臨床における金属イオンの治療的使用と毒性. 第19巻. De Gruyter. pp. 181– 202. doi :10.1515/9783110527872-007. ISBN 978-3-11-052787-2. PMID 30855102。
{{cite book}}:|journal=無視されました (ヘルプ) - ^ ナッシュ、ロバートA.「医療における金属」代替療法II.4(2005):18-25。
- ^ abcdefg Lippard, Stephen J.「医療における金属」生体無機化学、ミルシティ:University Science Books、1994年、505-583。
- ^ ab Dabrowiak, James C. “Metals in Medicine.” Inorganic Chemica Acta. (2012). 序文.