 | |
| 名前 | |
|---|---|
| IUPAC名
塩化ウラン(V)
| |
| その他の名前
五塩化ウラン
塩化ウラン | |
| 識別子 | |
| |
3Dモデル(JSmol)
|
|
| ケムスパイダー |
|
PubChem CID
|
|
| |
| |
| プロパティ | |
| UCl 5 | |
| モル質量 | 415.29グラム/モル |
特に記載がない限り、データは標準状態(25 °C [77 °F]、100 kPa)における材料のものです。
| |
五塩化ウランは、+5 の酸化状態のウランと 5 つの塩素原子から構成される無機 化合物です。
準備
五塩化ウランは、三酸化ウランと四塩化炭素を反応させることで製造することができ、その際、予め調製した量の化合物が触媒として働く。[1]
- 4 UO 3 + 10 CCl 4 → 4 UCl 5 + 10 COCl 2 + O 2
また、流動床反応器内で550℃の四塩化ウランと塩素を反応させることによっても製造できる。 [1]
プロパティ
五塩化ウランは、赤褐色の微結晶粉末、または金属光沢のある赤黒色の結晶として入手可能です。四塩化ウランとは異なり、液体塩素に溶解します。吸湿性が非常に高く、水中または加熱すると六塩化ウランと四塩化ウランに分解します。また、アルコール、アセトン、ジエチルエーテル、ジオキサンなどの有機溶媒とは反応しますが、四塩化炭素、二硫化炭素、塩化チオニルには安定な溶液を形成します。
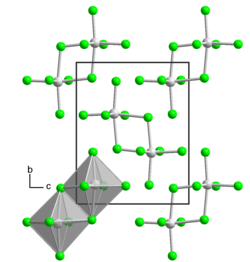
ウランには2つの結晶形態があり、いずれもウラン原子が6つの塩素原子の間に八面体状に存在します。通常はα型で、空間群 P 2 1 / nの単斜晶系結晶構造を持ちます。また、空間群P 1 [2]を持ち、五臭化ウランと同様にU 2 Cl 10二量体で構成される三斜晶系β型も存在します。[3]
気体形態は強いf軌道の寄与によりC 4v 対称性を持ち、電子親和力は4.76 ± 0.03 eV . [4]
参考文献
- ^ ab Brauer、Georg (1975). Handbuch der präparativen anorganischen Chemie、vol. 1 (第 3 版)。シュトゥットガルト:エンケ。 p. 1208.ISBN 3-432-02328-6. OCLC 310719485。
- ^ レスター・R・モース、ノーマン・M・エデルスタイン、J・フーガー(編)『アクチノイド元素と超アクチノイド元素の化学』 pp. 522– 523.
- ^ Levy, JH; Taylor, JC; Wilson, PW (1978-01-01). 「粉末中性子回折による五臭化ウランの結晶構造」 . Journal of Inorganic and Nuclear Chemistry . 40 (6): 1055– 1057. doi :10.1016/0022-1902(78)80507-7. ISSN 0022-1902 . 2021年5月29日閲覧。
- ^ Su, J; Dau, PD; Xu, CF; Huang, DL; Liu, HT; Wei, F; Wang, LS; Li, J (2013). 「UCl5-およびUCl5の電子構造に関する光電子分光法と理論的研究の共同研究」. Chemistry: An Asian Journal . 8 (10): 2489–96 . doi :10.1002/asia.201300627. PMID 23853153.