B細胞成熟抗原
| TNFRSF17 | |||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| 識別子 | |||||||||||||||||||||||||||||||||||||||||||||||||||
| エイリアス | TNFRSF17、BCM、BCMA、CD269、TNFRSF13A、腫瘍壊死因子受容体スーパーファミリーメンバー17、TNF受容体スーパーファミリーメンバー17 | ||||||||||||||||||||||||||||||||||||||||||||||||||
| 外部ID | オミム: 109545 ; MGI : 1343050 ;ホモロジーン: 920 ;ジーンカード:TNFRSF17 ; OMA : TNFRSF17 - オルソログ | ||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| ウィキデータ | |||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||
| BCMA TALL-1結合ドメイン | |||||||
|---|---|---|---|---|---|---|---|
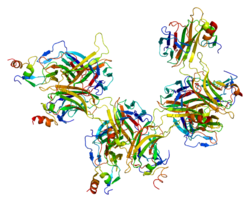
 ストール-1とbcmaの結晶構造 | |||||||
| 識別子 | |||||||
| シンボル | BCMA-Tall_bind | ||||||
| ファム | PF09257 | ||||||
| インタープロ | IPR015337 | ||||||
| SCOP2 | 1oqd /スコープ/ SUPFAM | ||||||
| |||||||
B 細胞成熟抗原( BCMAまたはBCM ) は、腫瘍壊死因子受容体スーパーファミリーメンバー 17 ( TNFRSF17 )としても知られ、ヒトではTNFRSF17遺伝子によってコードされるタンパク質です。
TNFRSF17は、B細胞活性化因子(BAFF)を認識するTNF受容体スーパーファミリーの細胞表面受容体である。[ 5 ] [ 6 ] [ 7 ]
血清B細胞成熟抗原(sBCMA)はBCMAの切断型であり、正常患者の血清中では低レベルで検出され、多発性骨髄腫(MM)患者では一般的に高値を示します。 [ 8 ]
関数
この遺伝子によってコードされるタンパク質は、TNF受容体スーパーファミリーのメンバーです。この受容体は成熟Bリンパ球で優先的に発現し、B細胞の発達と自己免疫応答に重要である可能性があります。この受容体は、腫瘍壊死因子(リガンド)スーパーファミリーのメンバー13b(TNFSF13B/TALL-1/BAFF)に特異的に結合し、NF-κBおよびMAPK8/JNKの活性化につながることが示されています。この受容体は、様々なTRAFファミリーのメンバーにも結合するため、細胞の生存と増殖のためのシグナルを伝達する可能性があります。[ 7 ]
相互作用
TNFRSF17はB細胞活性化因子TNFSF13Bと相互作用することが示されている。[ 9 ] [ 10 ] N末端の保存されたドメイン、BCMA TALL-1結合ドメインはTNFSF13Bへの結合に必要である。 [ 9 ]
臨床的意義
TNFRSF17は白血病、リンパ腫、多発性骨髄腫に関与していることが示唆されている[ 11 ](「Mitelmanデータベース」[ 12 ]および腫瘍学と血液学における遺伝学と細胞遺伝学のアトラス[ 13 ]を参照)。
薬剤ターゲットとして
抗体薬物複合体であるベランタマブマフォドチン(GSK2857916)は、再発性・難治性多発性骨髄腫患者を対象に評価されています。[ 14 ]ベランタマブマフォドチンは、2020年8月に米国で、少なくとも4種類の治療を受けた再発性または難治性多発性骨髄腫患者の治療薬として承認されました。[ 15 ]
キメラ抗原受容体(CAR)T細胞は、前臨床および第I相臨床試験での最初の報告以来、多発性骨髄腫の重要な治療法として浮上している。[ 16 ] [ 17 ]プロテアソーム阻害剤または免疫調節薬に抵抗性で、抗CD38抗体の投与を受けた骨髄腫患者におけるBCMAを標的としたCAR-T細胞療法であるJNJ-4528の第Ib/2相試験が完了している。[ 18 ]
ALLO-715は、Allogene Therapeutics社によるB細胞成熟抗原(BCMA)を標的としたCAR-T療法である。 [ 19 ] 2021年6月現在、多発性骨髄腫の治療薬として臨床試験が行われている。[ 20 ] 2021年4月21日、FDAはALLO-715に再生医療先進療法のステータスを付与した。 [ 21 ] ALLO-715は、メモリアルスローンケタリングがんセンターとメイヨークリニックで[ 22 ]多発性骨髄腫のUNIVERSAL試験の一環として、単独または選択的ガンマセクレターゼ阻害剤ニロガセスタットとの併用で研究されている。[ 20 ] [ 23 ]
参考文献
- ^ a b c GRCh38: Ensemblリリース89: ENSG00000048462 – Ensembl、2017年5月
- ^ a b c GRCm38: Ensemblリリース89: ENSMUSG00000022496 – Ensembl、2017年5月
- ^ 「ヒトPubMedリファレンス:」。米国国立医学図書館、国立生物工学情報センター。
- ^ 「マウスPubMedリファレンス:」米国国立医学図書館、国立生物工学情報センター。
- ^ Laâbi Y, Gras MP, Carbonnel F, Brouet JC, Berger R, Larsen CJ, Tsapis A (1992年11月). 「悪性T細胞リンパ腫において、染色体16上の新規遺伝子BCMがat(4;16)(q26;p13)転座によってインターロイキン2遺伝子と融合する」 . The EMBO Journal . 11 (11): 3897– 3904. doi : 10.1002 / j.1460-2075.1992.tb05482.x . PMC 556899. PMID 1396583 .
- ^ Laabi Y, Gras MP, Brouet JC, Berger R, Larsen CJ, Tsapis A (1994年4月). 「Bリンパ球成熟期に優先的に発現するBCMA遺伝子は双方向転写される」. Nucleic Acids Research . 22 (7): 1147–1154 . doi : 10.1093/nar/22.7.1147 . PMC 523635. PMID 8165126 .
- ^ a b「Entrez遺伝子:TNFRSF17腫瘍壊死因子受容体スーパーファミリー、メンバー17」。
- ^ Maglione PJ, Ko HM, Tokuyama M, Gyimesi G, Soof C, Li M, et al. (2020年1月). 「血清B細胞成熟抗原(BCMA)レベルは一次抗体欠損症を区別する」 . The Journal of Allergy and Clinical Immunology. In Practice . 8 (1): 283–291.e1. doi : 10.1016 / j.jaip.2019.08.012 . PMC 6980522. PMID 31430592 .
- ^ a b Liu Y, Hong X, Kappler J, Jiang L, Zhang R, Xu L, et al. (2003年5月). 「TNFファミリーメンバーTALL-1によるリガンド-受容体結合の解明」 . Nature . 423 (6935): 49– 56. Bibcode : 2003Natur.423...49L . doi : 10.1038/nature01543 . PMID 12721620. S2CID 4373708 .
- ^ Shu HB, Johnson H (2000年8月). 「B細胞成熟タンパク質は腫瘍壊死因子ファミリーメンバーTALL-1の受容体である」 . Proceedings of the National Academy of Sciences of the United States of America . 97 (16): 9156– 9161. Bibcode : 2000PNAS...97.9156S . doi : 10.1073/pnas.160213497 . PMC 16838. PMID 10908663 .
- ^ 「TNFRSF17(腫瘍壊死因子受容体スーパーファミリー、メンバー17)」。atlasgeneticsoncology.org。
- ^ 「Mitelmanデータベース:がんにおける染色体異常と遺伝子融合」。2016年5月25日時点のオリジナルよりアーカイブ。2015年1月29日閲覧。
- ^ 「腫瘍学と血液学における遺伝学と細胞遺伝学のアトラス」atlasgeneticsoncology.org。
- ^ Lonial S, Lee HC, Badros A, Trudel S, Nooka AK, Chari A, et al. (2020年2月). 「再発性または難治性多発性骨髄腫に対するベランタマブ・マフォドチン(DREAMM-2):2群間ランダム化オープンラベル第2相試験」. The Lancet. Oncology . 21 (2): 207– 221. doi : 10.1016 / s1470-2045(19)30788-0 . PMID 31859245. S2CID 209425201 .
- ^ Baines AC, Ershler R, Kanapuru B, Xu Q, Shen G, Li L, 他 (2022年11月). 「FDA承認概要:再発性または難治性多発性骨髄腫患者に対するベランタマブ・マフォドチン」 . Clinical Cancer Research . 28 (21): 4629– 4633. doi : 10.1158/1078-0432.CCR-22-0618 . PMC 9633344. PMID 35736811 .
- ^ Carpenter RO, Evbuomwan MO, Pittaluga S, Rose JJ, Raffeld M, Yang S, et al. (2013年4月). 「B細胞成熟抗原は多発性骨髄腫の養子T細胞療法における有望な標的である」 . Clinical Cancer Research . 19 (8): 2048– 2060. doi : 10.1158/ 1078-0432.CCR -12-2422 . PMC 3630268. PMID 23344265 .
- ^ Ali SA, Shi V, Maric I, Wang M, Stroncek DF, Rose JJ, 他 (2016年9月). 「抗B細胞成熟抗原キメラ抗原受容体を発現するT細胞は多発性骨髄腫の寛解を引き起こす」 . Blood . 128 ( 13): 1688–1700 . doi : 10.1182/blood-2016-04-711903 . PMC 5043125. PMID 27412889 .
- ^ Madduri D, Usmani SZ, Jagannath S, Singh I, Zudaire E, Yeh TM, et al. (2019-11-13). 「再発性および/または難治性多発性骨髄腫(R/R MM)患者を対象とした、B細胞成熟抗原(BCMA)を標的としたCAR-T細胞療法であるJNJ-4528の第1b/2相試験CARTITUDE-1の結果」 Blood . 134 ( Supplement_1): 577. doi : 10.1182/blood-2019-121731 . ISSN 0006-4971 . S2CID 209265279 .
- ^ Sommer C, Boldajipour B, Valton J, Galetto R, Bentley T, Sutton J, Ni Y, Leonard M, Van Blarcom T, Smith J, Chaparro-Riggers J (2018年11月29日). 「ALLO-715:多発性骨髄腫治療におけるオフスイッチ機能を有する同種BCMA CAR-T療法」 Blood . 132 ( Supplement 1): 591. doi : 10.1182/blood-2018-99-119227 . ISSN 0006-4971 .
- ^ a b ClinicalTrials.govにおける「Allogene Therapeutics」の臨床試験番号NCT04093596
- ^ 「FDA、再発性/難治性多発性骨髄腫に対するALLO-715にRMAT指定を付与」 OncLive 、 2021年4月21日。 2022年5月10日閲覧。
- ^ 「再発性または難治性多発性骨髄腫の成人患者におけるALLO-715およびALLO-647 BCMA同種CAR T細胞の安全性と有効性(UNIVERSAL)」メイヨークリニック。2022年5月10日閲覧。
- ^ Taylor NP (2020年12月7日). 「ASH: Allogeneの既製CAR-T、競争の激しいBCMA分野で60%の奏効率を達成」 . Fierce Biotech . 2022年5月10日閲覧。
外部リンク
- UCSC ゲノム ブラウザのヒトTNFRSF17ゲノムの位置とTNFRSF17遺伝子の詳細ページ。
さらに読む
- Treml LS, Crowley JE, Cancro MP (2006年10月). 「BLyS受容体シグネチャーは、ナイーブB細胞と抗原経験B細胞間の恒常性的に独立したコンパートメントを解明する」Seminars in Immunology . 18 (5): 297– 304. doi : 10.1016/j.smim.2006.07.001 . PMID 16919470 .
- Mackay F, Leung H (2006年10月). 「BAFF/APRILシステムのT細胞機能における役割」. Seminars in Immunology . 18 (5): 284– 289. doi : 10.1016/j.smim.2006.04.005 . PMID 16931039 .
- Gras MP, Laâbi Y, Linares-Cruz G, Blondel MO, Rigaut JP, Brouet JC, et al. (1995年7月). 「BCMAp:ヒト成熟Bリンパ球のゴルジ体における膜貫通タンパク質」. International Immunology . 7 (7): 1093– 1106. doi : 10.1093/intimm/7.7.1093 . PMID 8527407 .
- Loftus BJ, Kim UJ, Sneddon VP, Kalush F, Brandon R, Fuhrmann J, 他 (1999年9月). 「ヒト染色体16番染色体長腕部および16番染色体長腕部由来の12 MbのDNA配列におけるゲノム重複およびその他の特徴」. Genomics . 60 (3): 295–308 . doi : 10.1006/geno.1999.5927 . PMID 10493829 .
- Gross JA, Johnston J, Mudri S, Enselman R, Dillon SR, Madden K, et al. (2000年4月). 「TACIとBCMAはB細胞自己免疫疾患に関与するTNFホモログの受容体である」. Nature . 404 ( 6781): 995–999 . Bibcode : 2000Natur.404..995G . doi : 10.1038/35010115 . PMID 10801128. S2CID 4323357 .
- Hatzoglou A, Roussel J, Bourgeade MF, Rogier E, Madry C, Inoue J, et al. (2000年8月). 「TNF受容体ファミリーメンバーであるBCMA(B細胞成熟因子)は、TNF受容体関連因子(TRAF)1、TRAF2、およびTRAF3と会合し、NF-κB、elk-1、c-Jun N末端キナーゼ、およびp38ミトゲン活性化プロテインキナーゼを活性化する」 . Journal of Immunology . 165 (3): 1322– 1330. doi : 10.4049/jimmunol.165.3.1322 . PMID 10903733 .
- Shu HB, Johnson H (2000年8月). 「B細胞成熟タンパク質は腫瘍壊死因子ファミリーメンバーTALL-1の受容体である」 .米国科学アカデミー紀要. 97 (16): 9156–9161 . Bibcode : 2000PNAS...97.9156S . doi : 10.1073/ pnas.160213497 . PMC 16838. PMID 10908663 .
- Yu G, Boone T, Delaney J, Hawkins N, Kelley M, Ramakrishnan M, et al. (2000年9月). 「APRILとTALL-I、そして受容体BCMAとTACI:体液性免疫の制御システム」. Nature Immunology . 1 (3): 252– 256. doi : 10.1038/79802 . PMID 10973284. S2CID 6799584 .
- 川崎 明、土屋 暢、深澤 剛、橋本 秀、徳永 憲(2001年8月). 「ヒトBCMA遺伝子における4つの主要ハプロタイプの存在:全身性エリテマトーデスおよび関節リウマチとの関連性の欠如」. Genes and Immunity . 2 (5): 276– 279. doi : 10.1038/sj.gene.6363770 . PMID 11528522. S2CID 12315457 .
- Novak AJ, Darce JR, Arendt BK, Harder B, Henderson K, Kindsvogel W, 他 (2004年1月). 「多発性骨髄腫におけるBCMA、TACI、およびBAFF-Rの発現:増殖と生存のメカニズム」 . Blood . 103 (2): 689– 694. doi : 10.1182/blood-2003-06-2043 . PMID 14512299 .
- Hymowitz SG, Patel DR, Wallweber HJ, Runyon S, Yan M, Yin J, et al. (2005年2月). 「APRIL受容体複合体の構造:BCMAと同様に、TACIは高親和性リガンド結合にシステインリッチドメインを1つだけ用いる」 . The Journal of Biological Chemistry . 280 (8): 7218– 7227. doi : 10.1074/jbc.M411714200 . PMID 15542592 .
- Bellucci R, Alyea EP, Chiaretti S, Wu CJ, Zorn E, Weller E, 他 (2005年5月). 「多発性骨髄腫患者における移植片対腫瘍反応は、形質細胞膜受容体であるBCMAに対する抗体反応と関連する」 . Blood . 105 ( 10): 3945– 3950. doi : 10.1182/blood-2004-11-4463 . PMC 1895080. PMID 15692072 .
- Hendriks J, Planelles L, de Jong-Odding J, Hardenberg G, Pals ST, Hahne M, et al. (2005年6月). 「ヘパラン硫酸プロテオグリカン結合はAPRIL誘導性腫瘍細胞増殖を促進する」 . Cell Death and Differentiation . 12 (6): 637– 648. doi : 10.1038/sj.cdd.4401647 . PMID 15846369 .
- Chiu A, Xu W, He B, Dillon SR, Gross JA, Sievers E, et al. (2007年1月). 「ホジキンリンパ腫細胞はTACI受容体およびBCMA受容体を発現し、BAFFおよびAPRILに反応して生存および増殖シグナルを産生する」 . Blood . 109 (2): 729– 739. doi : 10.1182 / blood-2006-04-015958 . PMC 1785096. PMID 16960154 .
- Smirnova AS, Andrade-Oliveira V, Gerbase-DeLima M (2008年2月). 「BAFF遺伝子およびBCMA遺伝子の新たなスプライスバリアントの同定」. Molecular Immunology . 45 (4): 1179– 1183. doi : 10.1016/j.molimm.2007.07.028 . PMID 17825416 .
この記事には、パブリック ドメインである米国国立医学図書館のテキストが組み込まれています。






