21-水酸化酵素
| ステロイド21-水酸化酵素 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
 | |||||||||
| 識別子 | |||||||||
| EC番号 | 1.14.14.16 | ||||||||
| CAS番号 | 9029-68-9 | ||||||||
| 別名 | 「シトクロムP450、ファミリー21、サブファミリーA、ポリペプチド2」、CYP21A2、CYP21、CYP21B、[ 1 ] P45021A2、シトクロムP450c21、[ 2 ] [ 3 ] [ 4 ]ステロイド21-モノオキシゲナーゼ、[ 5 ] 21-ヒドロキシラーゼ、21α-ヒドロキシラーゼ、[ 6 ] [ 7 ] 21β-ヒドロキシラーゼ[ 8 ] [ 9 ] | ||||||||
| データベース | |||||||||
| IntEnz | IntEnzビュー | ||||||||
| ブレンダ | ブレンダエントリ | ||||||||
| エクスパスィ | ナイスザイムビュー | ||||||||
| ケッグ | ケッグエントリー | ||||||||
| メタサイクル | 代謝経路 | ||||||||
| プリアム | プロファイル | ||||||||
| PDB構造 | RCSB PDB PDBe PDBsum | ||||||||
| 遺伝子オントロジー | AmiGO / QuickGO | ||||||||
| |||||||||
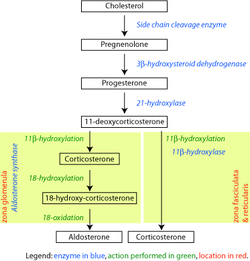
ステロイド 21-水酸化酵素は、ヒトではCYP21A2遺伝子によってコードされているタンパク質です。このタンパク質は分子の C21 位でステロイドを水酸化する酵素です。 [ 10 ] [ 11 ]酵素の命名規則は、作用する基質と実行される化学プロセスに基づいています。生化学的には、この酵素は、血圧調節、ナトリウム恒常性、血糖コントロールに重要な副腎ホルモンであるアルドステロンとコルチゾールの生合成に関与しています。この酵素は、プロゲステロンと17α-ヒドロキシプロゲステロンをそれぞれ11-デオキシコルチコステロンと11-デオキシコルチゾールに変換します[ 12 ] [ 13 ]ヒトでは最終的にアルドステロンとコルチゾールの生成につながる代謝経路内で、この酵素の欠損は先天性副腎過形成を引き起こす可能性があります。
ステロイド 21-ヒドロキシラーゼは、鉄含有ヘム補因子を使用して基質を酸化するモノオキシゲナーゼ酵素のシトクロム P450ファミリーのメンバーです。
ヒトでは、この酵素は副腎皮質細胞の小胞体膜に局在し[ 14 ] [ 15 ] 、 CYP21A2遺伝子によってコードされています。この遺伝子は、高い配列相同性を持つCYP21A1P擬似遺伝子の近傍に位置しています。この相同性により、分子レベルでの遺伝子解析が困難になり、 DNAの遺伝子間交換による機能喪失変異を引き起こすことがあります。
遺伝子
| CYP21A2 | |||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| 識別子 | |||||||||||||||||||||||||||||||
| 別名 | CYP21A2、CA21H、CAH1、CPS1、CYP21、CYP21B、P450c21B、シトクロムP450ファミリー21サブファミリーAメンバー2 | ||||||||||||||||||||||||||||||
| 外部ID | OMIM : 613815 ; MGI : 88591 ; HomoloGene : 68063 ; GeneCards : CYP21A2 ; OMA : CYP21A2 - オーソログ | ||||||||||||||||||||||||||||||
| EC番号 | 1.14.14.16,1.14.14.16 | ||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||
| ウィキデータ | |||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||

ヒトのステロイド21-ヒドロキシラーゼはCYP21A2遺伝子によってコードされており、この遺伝子には機能しない疑似遺伝子CYP21A1Pの1つまたは複数のコピーが付随している可能性がある。 [ 20 ] [ 21 ]この疑似遺伝子は、実際の機能遺伝子とエクソン情報の同一性の98%を共有している。 [ 22 ] [ 23 ]
偽遺伝子はゲノム中に広く存在し、複製過程における人工産物として発生します。しばしば「ジャンクDNA」と考えられていますが、研究により、これらの欠陥のあるコピーを保持することは有益な役割を担い、多くの場合、親遺伝子の制御に寄与することが示されています。[ 24 ]
マウスゲノムでは、Cyp21a2は擬似遺伝子であり、Cyp21a1は機能遺伝子である。[ 25 ]ニワトリとウズラでは、 Cyp21遺伝子は1つしか存在せず、その遺伝子座はCenpaとともに補体成分C4とTNX遺伝子の間に位置する。[ 26 ]
ヒトのCYP21A2は、6番染色体の主要組織適合性複合体III(MHCクラスIII)[ 27 ]に位置し、補体成分4遺伝子C4AとC4B、テネイシンX遺伝子TNXB、STK19に近接しています。[ 28 ] MHCクラスIIIはヒトゲノムの中で最も遺伝子密度の高い領域であり、2023年現在、機能や構造が未知の遺伝子が多数含まれています。[ 29 ] [ 27 ]
MHCクラスIII内では、CYP21A2はRCCXクラスター(遺伝子名RP ( STK19セリン/スレオニンキナーゼ19の旧称)、 [ 30 ] [ 31 ] C4、CYP21 、およびTNXからなる略語)内に位置しており、[ 32 ]これはヒトゲノムで最も複雑な遺伝子クラスターです。[ 33 ] RCCXセグメントの数は染色体あたり1~4個で変化し、 [ 30 ]モノモジュラーでは約15%、バイモジュラー(STK19-C4A-CYP21A1P-TNXA-STK19B-C4B-CYP21A2-TNXB)では75%、[ 31 ] [ 34 ]ヨーロッパ人ではトリモジュラーでは10%です。[ 35 ] RCCXユニットの四モジュール構造は非常にまれである。[ 36 ] [ 30 ] [ 35 ]モノモジュール構造では、すべての遺伝子が機能的、すなわちタンパク質をコードしているが、モジュール数が2以上の場合、各機能遺伝子のコピーは1つしか存在せず、残りは非コード擬似遺伝子である。ただし、常に活性コピーを持つC4遺伝子は例外である。 [ 30 ] [ 35 ]
CYP21A2遺伝子とCYP21A1P擬似遺伝子間の高い相同性とRCCX遺伝子座の複雑さのため、CYP21A2の分子診断は困難である。擬似遺伝子は、機能遺伝子と同一または類似の一塩基多型(SNP)を有する可能性があり、両者の区別が困難である。また、擬似遺伝子は機能遺伝子と組み換えられ、両方の特徴を持つハイブリッド遺伝子を形成する可能性がある。そのため、 CYP21A2のSNP検査では、偽陽性または偽陰性の結果が生じる可能性がある。[ 37 ]
全ゲノムシークエンシング技術は、DNAを小さな断片に分割し、それらをシークエンシングした後、重複部分に基づいて再構成するという手法に基づいています。しかし、CYP21A2とその擬似遺伝子は高い相同性と変異性を示すため、断片を遺伝子のいずれかのコピーに明確にマッピングすることはできません。これにより、アセンブリにエラーやギャップが生じたり、遺伝子内に存在する一部の変異が欠落したりする可能性があります。[ 38 ] [ 37 ]
ポリメラーゼ連鎖反応(PCR)分子診断では、選択的プライマーを用いて、特定の疾患や病状の診断または検出に関連するDNA配列の特定のセグメントを増幅する。プライマーが慎重に設計されていない場合、CYP21A2とCYP21A1P疑似遺伝子の両方、またはRCCXクラスターの異なるセグメントに結合し、偽陽性または偽陰性の結果が生じる可能性がある。したがって、CYP21A2のPCRでは、遺伝子と疑似遺伝子、および異なるRCCXモジュールを区別できる遺伝子座特異的プライマーの使用が必要である。さらに、PCRでは、 CYP21A2で頻繁に見られる大規模な遺伝子変換、欠失、重複などの複雑な変異を検出できない可能性がある。[ 39 ] [ 40 ] [ 38 ]
DNAサンプル中の特定のDNA配列を検出・定量化する手法であるサザンブロッティングも、 CYP21A2の解析には限界がある。この手法は時間がかかり、大量の良質なDNAを必要とするため、日常的な診断現場への適用は難しい。また、放射性バイオハザードを伴うため、安全性に懸念があり、多くの労力を要する。サザンブロッティングではキメラの接合部位を検出できない。CYP21A2遺伝子はミスマッチや再編成を起こしやすく、コピー数変異、大規模な遺伝子変換、小さな挿入・欠失、一塩基変異(SNP)など、さまざまな種類の複雑な変異が生じる。サザンブロッティングでは、これらすべての種類の変異を同時に検出することはできない。さらに、サザンブロッティングでは両親の遺伝子解析が必要であり、必ずしも実現可能または実用的ではない。[ 38 ] [ 41 ]
したがって、CYP21A2遺伝子を正確に解析するには、より長いDNA断片を配列決定し、遺伝子の構造と変異に関するより多くの情報を得ることができるターゲットロングリードシーケンシングなどの、より特殊で感度の高い手法が必要である。しかし、この手法は臨床応用には広く利用できず、また費用も高額である。[ 42 ] [ 43 ] [ 44 ]
タンパク質
ステロイド21-ヒドロキシラーゼは、シトクロムP450ファミリーに属するモノオキシゲナーゼ酵素の一種で、494個のアミノ酸残基から成り、分子量は55,000です。この酵素は、研究されている他のP-450酵素と最大28%の相同性があります。[ 45 ]
構造的には、このタンパク質は進化的に保存された4つのαヘリックス束からなるコア構造を有している(このような遺伝的保存性の重要性は、このタンパク質構造のこの側面の機能的重要性を示す上で重要である)。さらに、2つのαヘリックス、2組のβシート、そしてヘム補因子結合ループを有している。[ 46 ] ヒト酵素の各サブユニットは、合計13本のαヘリックスと9本のβストランドで構成され、三角柱状の三次構造に折り畳まれている。[ 12 ]
活性部位を定義する鉄(III)ヘム基は、各サブユニットの中心に位置しています。ヒト酵素は一度に1つの基質にしか結合しません。[ 12 ]一方、よく特徴づけられているウシ酵素は2つの基質に結合できます。[ 47 ]ヒト酵素とウシ酵素はアミノ酸配列の80%が同一ですが、構造的には異なり、特にループ領域では顕著であり、二次構造要素にも顕著に見られます。 [ 12 ]
種
ステロイド21-ヒドロキシラーゼの変異体は、すべての脊椎動物に見られます。[ 48 ]
Cyp21は、基底脊索動物と脊椎動物の種分化以前に脊索動物に初めて出現した。[ 49 ] 5億年以上前に出現した初期の無顎魚類であるウミヤツメは、Cyp21の進化と出現に関する貴重な知見を提供している。ウミヤツメは、哺乳類で見られるような11-デオキシコルチゾールをコルチゾールに変換する11β-ヒドロキシラーゼ酵素を欠いている。その代わりに、ウミヤツメは、CYP21によって触媒される反応の産物である11-デオキシコルチゾールを、ミネラルコルチコイド特性を持つ主要なグルココルチコイドホルモンとして利用している。これは、少なくとも5億年前の初期脊椎動物進化の過程で出現した、複雑で非常に特異的なコルチコステロイドシグナル伝達経路の存在を示唆している。[ 50 ]
魚類、両生類、爬虫類、鳥類、哺乳類などの脊椎動物において、Cyp21はグルココルチコイドとミネラルコルチコイドの生合成に関与しており、そのため脊椎動物におけるストレス反応、電解質バランスと血圧、免疫系、代謝の調節に必須である。[ 51 ]
Cyp21は哺乳類の間で比較的保存されており、その構造、発現、調節にはいくつかのバリエーションが見られます。[ 51 ]アカゲザルとオランウータンはCyp21のコピーを2つ持ち、チンパンジーは3つ持っていますが、偽遺伝子(CYP21A1P)は霊長類の中ではヒトにのみ存在します。[ 52 ]
組織および細胞内分布
ステロイド21-ヒドロキシラーゼは、副腎皮質内の小胞体膜のミクロソームに局在する。[ 10 ]これは、ステロイド17-ヒドロキシラーゼとアロマターゼとともに、3つのミクロソームステロイド生成シトクロムP450酵素の1つである。[ 53 ]
複数の組織で発現し、肝臓で最も豊富に発現するシトクロムP450スーパーファミリーの他の酵素とは異なり、成人ではステロイド21-ヒドロキシラーゼは、ステロイド11β-ヒドロキシラーゼやアルドステロン合成酵素とともに、ほぼ副腎でのみ発現しています。[ 54 ] [ 55 ]
2023年現在、ヒト細胞内でコードされているタンパク質の主な細胞内局在は不明であり、細胞解析が待たれている。[ 56 ]
機能

ステロイド21-ヒドロキシラーゼという酵素は、 ステロイドのC21位を水酸化します。 [ 13 ]ステロイドは天然に存在する、または合成された有機化合物のグループであり、ステロイドはすべて4つの環からなる一次構造を共有しています。この酵素は、ステロイド生体分子のC21位にヒドロキシル基( -OH)を付加する化学反応を触媒します。この位置はD環の側鎖にあります。
この酵素は、モノオキシゲナーゼ酵素のシトクロムP450スーパーファミリーに属します。シトクロムP450酵素は、薬物代謝やコレステロール、ステロイド、その他の脂質の合成に関わる多くの反応を触媒します。
ステロイド21-ヒドロキシラーゼはコルチゾールとアルドステロンの生合成に必須である。[ 57 ] [ 58 ]
メカニズム

ステロイド21-ヒドロキシラーゼはシトクロムP450酵素であり、その基質特異性と比較的高い触媒効率で知られています。[ 48 ]
他のシトクロムP450酵素と同様に、ステロイド21-水酸化酵素はシトクロムP450触媒サイクルに関与し、 NADPH - P450還元酵素と一電子移動反応を行う。ステロイド21-水酸化酵素は、プロゲステロンおよび17-ヒドロキシプロゲステロンの水酸化に非常に特異的である。これは、進化的および機能的に類似したP450酵素である17-水酸化酵素が幅広い基質を有することとは著しく対照的である。[ 59 ]
ステロイド21-ヒドロキシラーゼがプロゲステロン、17α-ヒドロキシプロゲステロン、21-デソキシコルチゾンのC21位にヒドロキシル(-OH)を付加する化学反応[ 60 ]は1952年に初めて記述されました。[ 61 ]
酵母で発現させたヒト酵素の研究では、当初17-ヒドロキシプロゲステロンがステロイド21-ヒドロキシラーゼの好ましい基質として分類されましたが、[ 59 ] [ 62 ] [ 63 ]、その後の精製されたヒト酵素の分析により、17-ヒドロキシプロゲステロンよりもプロゲステロンのK Mが低く、触媒効率が高いことがわかりました。 [ 12 ]
ヒトにおけるステロイド21-ヒドロキシラーゼのプロゲステロン変換触媒効率は、37℃で約1.3 x 10 7 M −1 s −1である。これは、現在報告されているP450酵素の中で最も触媒効率が高く、近縁のウシステロイド21-ヒドロキシラーゼよりも触媒効率が高いことを意味する。 [ 14 ] CH結合の切断による一次炭素ラジカルの生成が、水酸化における律速段階であると考えられている。 [ 12 ]
臨床的意義
先天性副腎過形成
CYP21A2遺伝子の遺伝子変異は、酵素の発達に障害を引き起こし、21-水酸化酵素欠損による先天性副腎過形成(CAH)を引き起こします。機能遺伝子と偽遺伝子が関与する遺伝子変換イベントは、ステロイド21-水酸化酵素欠損症の多くの症例の原因となっています。[ 64 ] CAHは常染色体劣性疾患です。CAHには複数の形態があり、患者に残存する酵素機能の量に基づいて、古典型と非古典型として定義されます
古典的形態は約1インチ10000対1インチ先天性副腎過形成症は、世界中で約2万人が出生しているCAHの一種で、 [ 58 ] [ 65 ]塩類喪失型(尿からナトリウムが過剰に排泄され、低ナトリウム血症と脱水症状を引き起こす)と単純男性化型の両方が含まれます。酵素活性の完全な喪失が塩類喪失型の原因となります。ステロイド21-水酸化酵素の構造変異は、先天性副腎過形成症の臨床的重症度に関係しています。コルチゾールとアルドステロンの欠乏は、ステロイドがナトリウム恒常性の調節に役割を果たしているため、生命を脅かすナトリウム喪失と関連しています。単純男性化CAH患者(酵素機能約1~2%)[ 58 ]は適切なナトリウム恒常性を維持していますが、小児期の成長加速や女児の性器不明瞭など、塩類喪失型と共通する他の症状も示します。
非古典型は最も軽度の病状で、酵素機能の約20%から50%を保持します。[ 58 ]この型は、軽度で臨床的に無症状のコルチゾール障害と関連していますが、[ 65 ]思春期後のアンドロゲン過剰と関連しています。[ 66 ]
非典型的先天性副腎過形成
21-水酸化酵素欠損症による非古典的先天性副腎過形成症(NCCAH)は、より軽度で発症が遅い先天性副腎過形成症です。民族集団による有病率は1/1000から1/1000まで様々です。1000対1インチ50 . [ 58 ]この疾患に罹患している人の中には、関連する徴候や症状が全くない人もいますが、高アンドロゲン血症の症状を経験する人もいます。[ 58 ] [ 65 ] [ 66 ]
NCCAHの女性は通常、出生時には正常な女性器を有しています。後年、この疾患の徴候や症状として、ニキビ、多毛症、男性型脱毛症、月経不順、不妊症などが現れることがあります。[ 58 ] [ 65 ] [ 25 ]
NCCAHの男性に関する研究は、女性に関する研究に比べて少ない。これは、男性は一般的に無症状であるためである。[ 25 ] [ 58 ]しかし、男性はニキビ[ 67 ] [ 68 ]や早期脱毛を呈することがある。[ 69 ] [ 70 ]
症状は通常思春期以降に診断されますが、子供では副腎皮質機能亢進が早まることがあります。[ 71 ]
他の病状に関する研究
CYP21A2遺伝子の遺伝子変異がどのように病態につながるかについては、現在も研究が進められています。この遺伝子の変異は常染色体優性遺伝の後極白内障を引き起こすことが報告されており、ステロイド21-ヒドロキシラーゼが眼の水晶体におけるアルドステロンとコルチゾールの副腎外生合成に関与している可能性を示唆しています。[ 72 ]
歴史
1950年代と1960年代には、コレステロールからプロゲステロンへの複雑な経路を介したステロイド生成経路が特定され、その中には、シトクロムP450酵素によって媒介される21位の水酸化反応(21位水酸化)を含む特定の酵素段階を示すコルチゾール合成経路が含まれていました。[ 73 ]その後、シトクロムP450酵素が記述され、ステロイドの21位水酸化はシトクロムP450と関連付けられました。[ 74 ] [ 73 ]
1980年代と1990年代には、部分長のウシCyp21 cDNAクローンがヒトCYP21A2に関連することが特定されました。[ 75 ] [ 73 ]研究者らは、先天性副腎過形成(CAH)に関連するCYP21A2遺伝子の変異を発見しました。[ 73 ]
1990年代以降、特定の変異がCAHの様々な形態や重症度と相関していることが明らかになりました。診断精度の向上のため、遺伝子型と表現型の相関関係が研究されました。[ 73 ]
参照
参考文献
- ^ 「UniProt」www.uniprot.org。2023年11月28日時点のオリジナルよりアーカイブ。2023年11月26日閲覧
- ^マリノ S、ペレス ガリード N、ラミレス P、プジャーナ M、ドラトラー G、ベルゴロスキー A、マリノ R (2020)。 「乾燥血痕サンプル中の CYP21A2 遺伝子の分子分析」。メディシナ。80 ( 3) : 197–202。PMID 32442933 。
- ^ Kaewkot A, Boonkaewwan C, Noosud J, Kayan A (2017年11月). 「豚のドリップロスと相関するシトクロムP450c21(CYP21)タンパク質の発現レベル」. Animal Science Journal . 88 (11): 1855– 1859. doi : 10.1111/asj.12863 . PMID 28677294 .
- ^ Mizrachi D, Wang Z, Sharma KK, Gupta MK, Xu K, Dwyer CR, Auchus RJ (2011年5月). 「ヒトシトクロムP450c21がプロゲステロン21-ヒドロキシラーゼである理由」.生化学. 50 ( 19): 3968–74 . doi : 10.1021/bi102078e . PMC 3165045. PMID 21446712 .
- ^ 「EC 1.14.14.16に関する情報 - ステロイド21-モノオキシゲナーゼ - BRENDA酵素データベース」www.brenda-enzymes.org。2020年10月11日時点のオリジナルよりアーカイブ。2020年9月21日閲覧。
- ^ムカンガ M、滝沢 K、青木 Y、浜野 S、手塚 M (2020 年 2 月)。「ミネラルコルチコイド生合成酵素およびミネラルコルチコイド受容体をコードする遺伝子の発現、ならびにウシ卵胞および黄体におけるミネラルコルチコイドのレベル」。生殖と発達のジャーナル。66 (1): 75–81 .土井: 10.1262/jrd.2019-127。PMC 7040213。PMID 31839646。
- ^ Sarafoglou K, Lorentz CP, Otten N, Oetting WS, Grebe SK (2012年7月). 「新生児スクリーニング時代における21α-水酸化酵素欠損による先天性副腎過形成の分子生物学的検査」. Clinical Genetics . 82 (1): 64– 70. doi : 10.1111/j.1399-0004.2011.01694.x . PMID 21534945. S2CID 7197547 .
- ^ベルガマスキ R、リヴィエリ C、ウゲッティ C、カンデローロ E、エギット MG、ピキエッキオ A、コジ V、バスティアナッロ S (2006 年 3 月)。 「先天性副腎過形成における脳白質障害」。神経学のアーカイブ。63 (3): 413–6 .土井: 10.1001/archneur.63.3.413。PMID 16540460。
- ^マルコ W、カリーナ=ファスカ B、ワッカーマン=ラモス A、ケーラー B (2000)。 「21β-ヒドロキシラーゼ欠損症を条件とする先天性副腎過形成 - 臨床的考察」。内分泌学、糖尿病 I Choroby Przemiany Materii Wieku Rozwojowego (ポーランド語)。6 (1): 67–9 . PMID 14640134。
- ^ a b
 この記事には、「NCBI: CYP21A2 シトクロムP450 ファミリー21 サブファミリーA メンバー2」のパブリックドメイン資料が組み込まれています。参照配列コレクション。国立生物工学情報センター。 2020年11月30日閲覧。
この記事には、「NCBI: CYP21A2 シトクロムP450 ファミリー21 サブファミリーA メンバー2」のパブリックドメイン資料が組み込まれています。参照配列コレクション。国立生物工学情報センター。 2020年11月30日閲覧。この遺伝子は、シトクロムP450スーパーファミリーの酵素のメンバーをコードしています。シトクロムP450タンパク質は、薬物代謝やコレステロール、ステロイド、その他の脂質の合成に関与する多くの反応を触媒するモノオキシゲナーゼです。このタンパク質は小胞体に局在し、21番目の位置でステロイドを水酸化します。その活性は、コルチゾールやアルドステロンなどのステロイドホルモンの合成に必要です。この遺伝子の変異は先天性副腎過形成を引き起こします。関連する偽遺伝子がこの遺伝子の近くにあります。ステロイド21-水酸化酵素欠損症の多くの症例は、機能遺伝子と偽遺伝子が関与する遺伝子変換イベントに起因すると考えられています。この遺伝子には、異なるアイソフォームをコードする2つの転写バリアントが見つかっています。
- ^ Ryan KJ, Engel LL (1957年3月). 「ステロイドの炭素21位における水酸化」(PDF) . The Journal of Biological Chemistry . 225 (1): 103–14 . doi : 10.1016/S0021-9258(18)64913-0 . PMID 13416221. 2020年3月25日時点のオリジナルよりアーカイブ(PDF) . 2009年10月17日閲覧。
- ^ a b c d e f Pallan PS, Wang C, Lei L, Yoshimoto FK, Auchus RJ, Waterman MR, Guengerich FP, Egli M (2015年5月). 「ヒトシトクロムP450 21A2、主要ステロイド21-水酸化酵素:プロゲステロン基質複合体の構造と律速的C-H結合切断」. The Journal of Biological Chemistry . 290 (21): 13128–43 . doi : 10.1074/jbc.M115.646307 . PMC 4505568. PMID 25855791 .
- ^ a b Neunzig J, Milhim M, Schiffer L, Khatri Y, Zapp J, Sánchez-Guijo A, et al. (2017年3月). 「CYP21A2によって生成されるステロイド代謝物16(β)-OH-アンドロステンジオンはCYP19A1の基質として働く」. The Journal of Steroid Biochemistry and Molecular Biology . 167 : 182– 191. doi : 10.1016/j.jsbmb.2017.01.002 . PMID 28065637. S2CID 36860068 .
- ^ a b Guengerich FP, Waterman MR, Egli M (2016年8月). 「シトクロムP450の機能に関する最近の構造的知見」 . Trends in Pharmacological Sciences . 37 (8): 625–40 . doi : 10.1016/j.tips.2016.05.006 . PMC 4961565. PMID 27267697 .
- ^ Sushko TA, Gilep AA, Usanov SA (2012年6月). 「ステロイドホルモン生合成に関与するミクロソームシトクロムP450 CYP17とCYP21の分子間相互作用のメカニズム」.生化学. Biokhimiia . 77 (6): 585–92 . doi : 10.1134/S0006297912060041 . PMID 22817457. S2CID 18927484 .
- ^ a b c ENSG00000231852, ENSG00000206338, ENSG00000233151, ENSG00000232414, ENSG00000235134 GRCh38: Ensembl リリース 89: ENSG00000198457, ENSG00000231852, ENSG00000206338, ENSG00000233151, ENSG00000232414, ENSG00000235134 – Ensembl、2017年5月
- ^ a b c GRCm38: Ensemblリリース89: ENSMUSG00000024365 – Ensembl、2017年5月
- ^ 「ヒトPubMedリファレンス:」。米国国立医学図書館、国立生物工学情報センター。
- ^ 「マウスPubMedリファレンス:」米国国立医学図書館、国立生物工学情報センター。
- ^
 この記事には、「CYP21A2 シトクロムP450 ファミリー21 サブファミリーA メンバー2 [ ホモ・サピエンス (ヒト)]」のパブリックドメイン資料が含まれています。参考配列コレクション。国立生物工学情報センター。
この記事には、「CYP21A2 シトクロムP450 ファミリー21 サブファミリーA メンバー2 [ ホモ・サピエンス (ヒト)]」のパブリックドメイン資料が含まれています。参考配列コレクション。国立生物工学情報センター。 - ^ Baumgartner-Parzer S, Witsch-Baumgartner M, Hoeppner W (2020年10月). 「21-水酸化酵素欠損症の分子遺伝学的検査と報告に関するEMQNベストプラクティスガイドライン」. European Journal of Human Genetics . 28 (10): 1341– 1367. doi : 10.1038/ s41431-020-0653-5 . PMC 7609334. PMID 32616876. S2CID 220295067 .
- ^東雄一、吉岡秀次、山根正之、後藤 修、藤井(栗山)雄一(1986年5月). 「ヒト染色体上に直列に配列する2つのステロイド21-ヒドロキシラーゼ遺伝子の完全ヌクレオチド配列:偽遺伝子と真遺伝子」 .米国科学アカデミー紀要. 83 (9 ) : 2841–5 . Bibcode : 1986PNAS...83.2841H . doi : 10.1073/pnas.83.9.2841 . PMC 323402. PMID 3486422 .
- ^コンコリーノ P、リッツァ R、コステラ A、カロッツァ C、ズッピ C、カポルオンゴ E (2017 年 6 月)。 「21-ヒドロキシラーゼ欠損症を引き起こすCYP21A2イントロン変異」。代謝: 臨床および実験。71 : 46–51 .土井: 10.1016/j.metabol.2017.03.003。PMID 28521877。
- ^ Witek J, Mohiuddin SS (2023).生化学, Pseudogenes . Treasure Island (FL): StatPearls Publishing. PM ID 31751022. NCBI NBK549832 .
- ^ a b c Parker KL, Chaplin DD, Wong M, Seidman JG, Smith JA, Schimmer BP (1985年12月). 「マウス副腎およびトランスフェクトされたY1副腎皮質腫瘍細胞におけるマウス21-ヒドロキシラーゼの発現」 . Proceedings of the National Academy of Sciences of the United States of America . 82 (23): 7860–4 . Bibcode : 1985PNAS...82.7860P . doi : 10.1073 / pnas.82.23.7860 . PMC 390869. PMID 2999780 .
- ^椎名 剛志、清水 誠、細道 健、小原 誠、渡辺 誠、半澤 健、他 (2004年6月). 「2つの鳥類(ウズラとニワトリ)MHC領域の比較ゲノム解析」 . Journal of Immunology . 172 (11): 6751–63 . doi : 10.4049/jimmunol.172.11.6751 . PMID 15153492 .
- ^ a b Yu CY (1999). 「ヒトMHC補体遺伝子クラスターの分子遺伝学」.実験および臨床免疫遺伝学. 15 ( 4): 213– 230. doi : 10.1159/000019075 . PMID 10072631. S2CID 25061446 .
- ^ White PC, Grossberger D, Onufer BJ, Chaplin DD, New MI, Dupont B, Strominger JL (1985年2月). 「ステロイド21-ヒドロキシラーゼをコードする2つの遺伝子は、ヒトの補体第4成分をコードする遺伝子の近傍に位置する」 . Proceedings of the National Academy of Sciences of the United States of America . 82 (4): 1089– 1093. Bibcode : 1985PNAS...82.1089W . doi : 10.1073/pnas.82.4.1089 . PMC 397199. PMID 2983330 .
- ^ Xie T, Rowen L, Aguado B, Ahearn ME, Madan A, Qin S, et al. (2003年12月). 「遺伝子密度の高い主要組織適合遺伝子複合体クラスIII領域の解析とマウスとの比較」 . Genome Research . 13 (12): 2621– 2636. doi : 10.1101/gr.1736803 . PMC 403804. PMID 14656967 .
- ^ a b c d Bánlaki Z, Doleschall M, Rajczy K, Fust G, Szilágyi A (2012年10月). 「RCCXコピー数変異体の精密な特性評価と拡張MHCハプロタイプとの関係」 . Genes and Immunity . 13 (7): 530– 535. doi : 10.1038/gene.2012.29 . PMID 22785613. S2CID 36582994 .
- ^ a bカロッッツァ C、フォカ L、デ・パオリス E、コンコリーノ P (2021). 「遺伝子と偽遺伝子: RCCX 遺伝子座と疾患の複雑さ」。内分泌学のフロンティア。12 709758. doi : 10.3389/fendo.2021.709758。PMC 8362596。PMID 34394006。
- ^ Sweeten TL, Odell DW, Odell JD, Torres AR (2008年1月). 「C4Bヌルアレルは、自閉症における隣接遺伝子CYP21A2の遺伝的多型とは関連がない」 . BMC Medical Genetics . 9 :1. doi : 10.1186/1471-2350-9-1 . PMC 2265260. PMID 18179706 .
- ^ Milner CM, Campbell RD (2001年8月). 「ヒトMHCクラスIII領域の遺伝的構成」 . Frontiers in Bioscience . 6 : D914– D926. doi : 10.2741/milner . PMID 11487476 .
- ^ Kim JH, Kim GH, Yoo HW, Choi JH (2023年6月). 「CAH-X症候群を含む21-水酸化酵素欠損症の診断における分子基盤と遺伝子検査戦略」Annals of Pediatric Endocrinology & Metabolism . 28 (2): 77– 86. doi : 10.6065/apem.2346108.054 . PMC 10329939. PMID 37401054 .
- ^ a b c Bánlaki Z、Szabó JA、Szilágyi Á、Patócs A、Prohászka Z、Füst G、Doleschall M (2013)。「CYP21A2遺伝子のハプロタイプによって追跡されるヒトRCCXコピー数変動の種内進化」。ゲノムバイオル進化。5 (1): 98–112 .土井: 10.1093/gbe/evs121。PMC 3595039。PMID 23241443。
- ^ Tsai LP, Lee HH (2012年9月). 「CYP21A1Pおよび重複したCYP21A2遺伝子の解析」. Gene . 506 (1): 261– 262. doi : 10.1016/j.gene.2012.06.045 . PMID 22771554 .
- ^ a b Arriba M, Ezquieta B (2022). 「ステロイド21-水酸化酵素欠損症の分子診断:実践的アプローチ」 . Front Endocrinol . 13 834549. doi : 10.3389/fendo.2022.834549 . PMC 9001848. PMID 35422767 .
- ^ a b c Karaoğlan M, Nacarkahya G, Aytaç EH, Keskin M (2021年11月). 「21-水酸化酵素欠損症小児におけるCYP21A2遺伝子型判定の課題:南東アナトリアにおける次世代シーケンシングを用いた遺伝子型と表現型の相関関係の解明」J Endocrinol Invest . 44 (11): 2395– 2405. doi : 10.1007/s40618-021-01546-z . PMID 33677812 . S2CID 232133292 .
- ^ Xu Z, Chen W, Merke DP, McDonnell NB (2013年11月). 「CYP21A2遺伝子の包括的な変異解析:先天性副腎過形成の分子診断への効率的な多段階アプローチ」 . J Mol Diagn . 15 (6): 745–53 . doi : 10.1016/j.jmoldx.2013.06.001 . PMC 5803549. PMID 24071710 .
- ^ 「ポリメラーゼ連鎖反応(PCR)ファクトシート」Genome.gov。2023年12月3日時点のオリジナルよりアーカイブ。 2023年12月3日閲覧。
- ^ 「サザンブロッティング — ナレッジハブ」 GeNotes . 2023年12月3日時点のオリジナルよりアーカイブ。 2023年12月3日閲覧。
- ^ Guo X, Zhang Y, Yu Y, Zhang L, Ullah K, Ji M, Jin B, Shu J (2023). 「訂正:先天性副腎過形成の妊娠:補助的生殖と妊娠合併症。系統的レビューとメタアナリシス」 . Front Endocrinol . 14 1269711. doi : 10.3389/fendo.2023.1269711 . PMC 10575760. PMID 37842302 .
- ^足立 英之、中川 亮、辻(細川) 明生、ガウ 正治、桐野 聡、与儀 明生、中谷 浩、高澤 健、山口 剛、小正 剛、村上 正治、田島 剛、長谷川 剛、山田 剛、森尾 剛、小原 修、鹿島田 功(2023年10月)。 「21-水酸化酵素欠損症の遺伝子診断のためのワンステップPCRを用いたMinIONベースのロングリードシーケンスアプリケーション」。J Clin Endocrinol Metab。109 (3): 750– 760。doi : 10.1210 /clinem/ dgad577。PMID 37804107。S2CID 263742489。
- ^ Zhang X, Gao Y, Lu L, Cao Y, Zhang W, Sun B, Wu X, Tong A, Chen S, Wang X, Mao J, Nie M (2023). 「21-ヒドロキシラーゼ欠損症患者におけるCYP21A2変異の包括的検出のための標的ロングリードシーケンシング」Journal of Endocrinological Investigation . 47 (4): 833– 841. doi : 10.1007/s40618-023-02197- y . PMID 37815751. S2CID 263800944 .
- ^ “Steroid 21-hydroxylase | DrugBank Online” . go.drugbank.com . 2023年11月28日時点のオリジナルよりアーカイブ。 2023年11月27日閲覧。
- ^ Werck-Reichhart D, Feyereisen R (2000). 「シトクロムP450:成功物語」 .ゲノム生物学. 1 (6) REVIEWS3003. doi : 10.1186 / gb-2000-1-6-reviews3003 . PMC 138896. PMID 11178272 .
- ^ Zhao B, Lei L, Kagawa N, Sundaramoorthy M, Banerjee S, Nagy LD, Guengerich FP, Waterman MR (2012年3月). 「ステロイド21-ヒドロキシラーゼ(シトクロムP450 21A2)の2つの基質を含む3次元構造は、疾患関連変異の局在を明らかにする」 . The Journal of Biological Chemistry . 287 (13): 10613–22 . doi : 10.1074/jbc.M111.323501 . PMC 3323056. PMID 22262854 .
- ^ a b Graham SE, Peterson JA (2002). 「配列アラインメント、変動性、そして気まぐれ」.シトクロムP450 パートC. Methods in Enzymology. Vol. 357. Academic Press. pp. 15– 28. doi : 10.1016/s0076-6879(02)57661-8 . ISBN 978-0-12-182260-6 . PMID 12424893
- ^ Baker ME, Nelson DR, Studer RA (2015年7月). 「副腎および性ステロイドに対する反応の起源:酵素とステロイド受容体の乱交と共進化の役割」. J Steroid Biochem Mol Biol . 151 : 12– 24. doi : 10.1016/j.jsbmb.2014.10.020 . PMID 25445914. S2CID 21649057 .
- ^ Barany A, Shaughnessy CA, McCormick SD (2021年3月). 「ウミヤツメ(Petromyzon marinus)の腸管におけるNa+/K+-ATPaseのコルチコステロイドによる制御」.一般・比較内分泌学. 307 113756. Bibcode : 2021GCEnd.30713756B . doi : 10.1016/ j.ygcen.2021.113756 . PMID 33741310. S2CID 232296805 .
- ^ a b Cameron PU, Tabarias HA, Pulendran B, Robinson W, Dawkins RL (1990). 「中心MHCゲノムの保全:ヤギにおける補体、HSP70、TNF遺伝子のPFGEマッピングとRFLP解析」.免疫遺伝学. 31 (4): 253–64 . doi : 10.1007/BF00204897 . PMID 1970334. S2CID 22716959 .
- ^ Kawashima A, Satta Y (2014). 「シトクロムP450の基質依存的進化:解毒型の急速なターンオーバーと生合成型の保全」. PLOS ONE . 9 (6) e100059. Bibcode : 2014PLoSO...9j0059K . doi : 10.1371/journal.pone.0100059 . PMC 4076195. PMID 24977709 .
- ^ Auchus RJ, Miller WL (2015). 「ステロイドプロセシングにおけるP450酵素」.シトクロムP450:構造、メカニズム、生化学(第4版). Springer International Publishing. pp. 851– 879. doi : 10.1007/978-3-319-12108-6_12 . ISBN 978-3-319-12107-9。
- ^ Korzekwa K (2014). 「酸化代謝の酵素反応速度論:シトクロムP450」.薬物代謝における酵素反応速度論. 分子生物学の方法. 第1113巻. Humana Press. pp. 149– 166. doi : 10.1007/978-1-62703-758-7_8 . ISBN 978-1-62703-757-0 . ISSN 1940-6029 . PMID 24523112
- ^ 「CYP21A2の組織発現」 . The Human Protein Atlas . 2023年11月28日時点のオリジナルよりアーカイブ。 2023年11月27日閲覧。
- ^ 「CYP21A2 細胞内RNA発現」 . The Human Protein Atlas . 2023年11月28日時点のオリジナルよりアーカイブ。 2023年11月27日閲覧。
- ^ Araújo RS, Mendonca BB, Barbosa AS, Lin CJ, Marcondes JA, Billerbeck AE, Bachega TA (2007年10月). 「CYP21A2とCYP21A1Pプロモーター領域間のマイクロコンバージョンは、非古典型21-水酸化酵素欠損症を引き起こす」. The Journal of Clinical Endocrinology and Metabolism . 92 (10): 4028–34 . doi : 10.1210/jc.2006-2163 . PMID 17666484 .
- ^ a b c d e f g h Speiser PW, Arlt W, Auchus RJ, Baskin LS, Conway GS, Merke DP, et al. (2018年11月). 「ステロイド21-水酸化酵素欠損による先天性副腎過形成:内分泌学会臨床診療ガイドライン」 .臨床内分泌代謝学ジャーナル. 103 (11): 4043– 4088. doi : 10.1210/jc.2018-01865 . PMC 6456929. PMID 30272171 .
- ^ a b Auchus RJ, Sampath Kumar A, Andrew Boswell C, Gupta MK, Bruce K, Rath NP, Covey DF (2003年1月). 「プロゲステロンのエナンチオマー(ent-プロゲステロン)はヒトシトクロムP450c17およびP450c21の競合的阻害剤である」. Archives of Biochemistry and Biophysics . 409 (1): 134– 44. doi : 10.1016/s0003-9861(02)00491-5 . PMID 12464252 .
- ^ Rosenfeld G, Ungar F, Dorfman RI, Pincus G (1955). 「放射線照射と副腎ステロイド生成:放射線照射を受けた単離灌流子牛副腎によるステロイド変換」.内分泌学. 56 (1): 24–9 . doi : 10.1210/endo-56-1-24 . PMID 13220521 .
- ^ Dorfman RI, Hayano M (1952年3月). 「副腎ホモゲネートのプロゲステロン、17-ヒドロキシプロゲステロン、および21-デオキシコルチゾンに対する作用」.生化学・生物理学アーカイブ. 36 (1): 237–9 . doi : 10.1016/0003-9861(52)90397-4 . PMID 14934270 .
- ^ Lorence MC, Trant JM, Mason JI, Bhasker CR, Fujii-Kuriyama Y, Estabrook RW, Waterman MR (1989年8月). 「ウシ副腎シトクロムP450C21をコードする完全長cDNAの発現」.生化学・生物理学アーカイブ. 273 (1): 79– 88. doi : 10.1016/0003-9861(89)90164-1 . PMID 2502949 .
- ^ Wu DA, Hu MC, Chung BC (1991年4月). 「サッカロミセス・セレビシエにおける野生型および変異型ヒトシトクロムP450c21の発現と機能研究」. DNA and Cell Biology . 10 (3): 201–9 . doi : 10.1089/dna.1991.10.201 . PMID 1707279 .
- ^ “NCBI: CYP21A2 シトクロムP450 ファミリー21 サブファミリーA メンバー2” . 国立生物工学情報センター. 2020年10月28日時点のオリジナルよりアーカイブ。2020年11月30日閲覧。
この遺伝子は、シトクロムP450スーパーファミリー酵素のメンバーをコードしています。シトクロムP450タンパク質は、薬物代謝やコレステロール、ステロイド、その他の脂質の合成に関与する多くの反応を触媒するモノオキシゲナーゼです。このタンパク質は小胞体に局在し、ステロイドの21位を水酸化します。その活性は、コルチゾールやアルドステロンなどのステロイドホルモンの合成に必要です。この遺伝子の変異は先天性副腎過形成を引き起こします。関連する偽遺伝子がこの遺伝子の近くにあります。ステロイド21-水酸化酵素欠損症の多くの症例は、機能遺伝子と偽遺伝子が関与する遺伝子変換イベントに起因すると考えられています。この遺伝子には、異なるアイソフォームをコードする2つの転写バリアントが見つかっています。
 この記事には、パブリック ドメインであるこのソースからのテキストが組み込まれています。
この記事には、パブリック ドメインであるこのソースからのテキストが組み込まれています。 - ^ a b c d Merke DP, Auchus RJ (2020年9月). 「21-水酸化酵素欠損による先天性副腎過形成」. The New England Journal of Medicine . 383 (13): 1248–1261 . doi : 10.1056/NEJMra1909786 . PMID 32966723. S2CID 221884108 .
- ^ a b Miller WL, Auchus RJ (2011年2月). 「ヒトステロイド生成とその障害の分子生物学、生化学、生理学」 .内分泌レビュー. 32 (1): 81– 151. doi : 10.1210/er.2010-0013 . PMC 3365799. PMID 21051590 .
- ^ Sharquie KE, Noaimi AA, Saleh BO, Anbar ZN (2009年12月). 「イラク人健康男性と尋常性ざ瘡患者における21-α水酸化酵素欠損症および関連性ホルモンの頻度」サウジアラビア医学ジャーナル. 30 (12): 1547–50 . PMID 19936418 .
- ^ Falhammar H, Nordenström A (2015年9月). 「21-水酸化酵素欠損による非典型的先天性副腎過形成:臨床所見、診断、治療、および転帰」.内分泌. 50 ( 1): 32– 50. doi : 10.1007/s12020-015-0656-0 . PMID 26082286. S2CID 23469344 .
- ^ New MI (2006年11月). 「広範な臨床経験:非古典的21-水酸化酵素欠損症」 . The Journal of Clinical Endocrinology and Metabolism . 91 (11): 4205–14 . doi : 10.1210/jc.2006-1645 . PMID 16912124.
女性および男性における頭髪の脱毛は恥ずかしいものであり、5α-還元酵素阻害剤による治療が必要となる
。 - ^ファインゴールドKR、アナワルトB、ボイスA、クロウソスG、デ・ハーダーWW、ダンガンK、グロスマンA、ハーシュマンJM、ホフラントJ、カルツァスG、コッホC、コップP、コルボニッツM、マクラクランR、モーリーJE、ニューM、パーネルJ、シンガーF、ストラタキスCA、トレンスDL、ウィルソンDP、ヤウM、グジュラル J、新しいミシガン州 (2019 年 4 月)先天性副腎過形成:診断と緊急治療。 MDText.com。PMID 25905311。2020年11月14日のオリジナルからアーカイブ。2021 年3 月 25 日に取得。
- ^ Witchel SF , Azziz R (2010). 「非典型的先天性副腎過形成」 . International Journal of Pediatric Endocrinology . 2010 625105. doi : 10.1155/2010/625105 . PMC 2910408. PMID 20671993 .
- ^ Berry V, Pontikos N, Ionides A, Kalitzeos A, Quinlan RA, Michaelides M (2022年4月). 「CYP21A2遺伝子の病原性変異は、孤立性常染色体優性先天性後極白内障を引き起こす」 . Ophthalmic Genet . 43 (2): 218– 223. doi : 10.1080/13816810.2021.1998556 . PMID 34748434. S2CID 243861798. 2024年2月2日時点のオリジナルよりアーカイブ。2024年2月2日閲覧。
- ^ a b c d e Miller WL, White PC (2023年1月). 「副腎研究の歴史:古代解剖学から現代分子生物学まで」 . Endocr Rev. 44 ( 1): 70– 116. doi : 10.1210/endrev/bnac019 . PMC 9835964. PMID 35947694 .
- ^山崎 秀次編 (2014).シトクロムP450研究50年. doi : 10.1007/978-4-431-54992-5 . ISBN 978-4-431-54991-8. S2CID 27237884 .
- ^ Miller WL (2020). 「テネイシンXの発見と初期研究」 . Front Immunol . 11 612497. doi : 10.3389/fimmu.2020.612497 . PMC 7829301. PMID 33505400
外部リンク
- GeneReviews/NCBI/NIH/UWの21-水酸化酵素欠損型先天性副腎過形成に関するエントリ
- 21-ヒドロキシラーゼ欠損先天性副腎過形成症に関するOMIMエントリ
- 21-ヒドロキシラーゼを介したプロゲステロンからのデオキシコルチコステロンの合成(画像) 2021年4月26日アーカイブ、Wayback Machineにて
- 米国国立医学図書館医学件名表(MeSH)のステロイド+21-ヒドロキシラーゼ
- UCSC ゲノム ブラウザのヒトCPS1ゲノムの位置とCPS1遺伝子の詳細ページ。
- UCSC ゲノム ブラウザのヒトCYP21A2ゲノムの位置とCYP21A2遺伝子の詳細ページ。
- PDBe-KBのUniProt : P08686 (ステロイド 21-ヒドロキシラーゼ)のPDBで利用可能なすべての構造情報の概要。
この記事には、パブリック ドメインである米国国立医学図書館のテキストが組み込まれています。









