アブサンチン
 | |
 | |
| 名前 | |
|---|---|
| IUPAC名 (1R,2R,5S,8S,9S,12S,13R,14S,15S,16R,17S,20S,21S,24S)-12,17-ジヒドロキシ-3,8,12,17,21,25-ヘキサメチル-6,23-ジオキサヘプタシクロ[13.9.2.01,16.02,14.04,13.05,9.020,24]ヘキサコサ-3,25-ジエン-7,22-ジオン | |
| 識別子 | |
3Dモデル(JSmol) | |
| チェビ |
|
| チェムブル |
|
| ケムスパイダー |
|
PubChem CID | |
| ユニイ |
|
CompToxダッシュボード(EPA) | |
| |
| |
| プロパティ | |
| C 30 H 40 O 6 | |
| モル質量 | 496.635 |
特に記載がない限り、データは標準状態(25 °C [77 °F]、100 kPa)における材料のものです。 | |
アブシンチンは、ヨモギ(Artemisia absinthium )という植物から天然に生成されるトリテルペンラクトンです。アブサンの独特の風味の原因となる、最も苦味のある化学物質の一つです。 [ 1 ]この化合物は生物活性を示し、抗炎症剤としての効果が期待されています。[ 2 ]また、同じくヨモギに含まれる神経毒であるツジョンと混同しないように注意してください。
化学構造
アブシンチン(1)の複雑な構造はセスキテルペンラクトンに分類され、イソプレン(4)由来の5炭素「構成要素」(3)から化学的に誘導される天然化合物の大きなカテゴリーに属します。完全な構造は、グアイアノリドの5員環上のアルケンにおいて、天然に存在すると考えられるディールス・アルダー反応によって結合した2つの同一のモノマー(2)で構成されています。

全合成
(+)-アブシンチンの全合成は、2004年にZhangらによって行われた[ 3 ] 。市販の試薬であるサントニン(1)を原料とし、10段階の合成過程を経て、最終収率は18.6%と報告されている。合成の基本は、元の6員環炭素環を7員環に環拡大し、グアイアノリドモノマー(2)骨格を形成し、続いてディールス・アルダーカップリング(3)を行い、最終的に立体化学修飾を行って(+)-アブシンチン(4)を得るというものである。

生合成
Artemisia absinthiumにおけるアブシンチンの生合成の全容は解明されていないが、その大部分は、アブシンチンを得るのに必要な天然物前駆体から推測することができる。アブシンチンなどのテルペノイドはイソプレン「ユニット」で構成されていると言えるが、イソプレン単体では安定性が高く、直接反応しない。むしろ、イソプレンユニットは二リン酸として転移され、反応する。テルペンの命名法が示すように、アブシンチンの最初の前駆体であるファルネシル二リン酸[A]は15個の炭素、つまり3個のイソプレンユニットを含む。二リン酸の離脱(1)により、合成酵素内でカルボカチオンが生成され、これが分子の反対側の末端にある炭素-炭素二重結合(2)によって攻撃される。アルテミシアの生合成経路における最初の安定中間体は、おそらくゲルマクレンA [B]であり、これはこれまで植物のセスキテルペン合成経路でグアイアノリドの前駆物質として同定されている。[ 4 ]そこから、水酸化(3)が起こり、続いて酸化(4)を受けてアルデヒドとなり、さらに水酸化(5)されてカルボキシル基が形成される。(4)の後、最終生成物中のこの結合の還元により末端の炭素-炭素二重結合が消失するため、アブシンチンモノマーは他のゲルマクレンA下流生成物と区別される。この還元は必ずしもステップ(4)で起こるわけではなく、さらに下流で起こる可能性がある。カルボキシル基とヒドロキシル基が所定の位置にあることで、一般的なグアイアノリド合成経路で提案されているように、脱水(7)を経てグアイアノラクトン [C] が形成される可能性がある。[ 5 ]アブシンチンセスキテルペングアイアノリドモノマー [D] の形成は、ヒドロキシル化と二重結合転位 (8,9) から、天然に存在するディールス・アルダー反応 [10] を介してアブシンチン [E] への二量体化に直接先行すると仮定されており、この反応自体は自発的に良好な収率で起こり得るものの、関連する合成酵素によって促進される可能性が高い[ 3 ]が、典型的な天然物生合成よりも遅い。
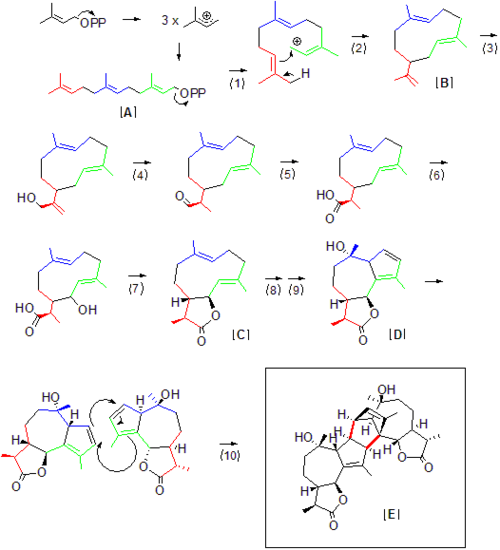
Artemisia absinthiumに特異的な合成酵素は、in vitroでこの特定のセスキテルペン形成を再現できるほど十分に単離されていないが、ここで提示する一般的な反応スキームは、別のセスキテルペンラクトンであるゲルマクレンAの生合成に利用されるテルペン中間体を用いたアブシンチン生合成の可能性のあるシナリオを示している。上記で提案された番号付き生合成ステップを合理化するのに役立つテルペン生合成の酵素類似体は以下の通りである。
- 一般的なセスキテルペン合成酵素を介したファルネシル二リン酸の離脱[ 6 ]
- 一般的なセスキテルペン合成酵素による閉環(#1と同様)[ 6 ]
- シトクロムP450酵素であるゲルマクレンA水酸化酵素による末端アリル炭素の水酸化。[ 6 ]
- アルコールを-ゲルマクレンA水酸化酵素で酸化してアルドールを得る。[ 6 ]
- ゲルマクレンA水酸化酵素によるアルコールのカルボキシル基への水酸化。[ 6 ]
- NADPHを介したアリル炭素の水酸化は、ラクトン環の閉環に先立つと想定される水酸化を介して起こる[ 6 ]
- ラクトン形成/閉環[ 6 ]
- 炭素-炭素三級二重結合におけるヒドロキシル化。
- 追加の5員環形成/環化[ 4 ]
- Artemisia absinthiumにおける未確認酵素を介したディールス・アルダーカップリング。
参考文献
- ^ Lachenmeier DW、Walch SG、Padosch SA、Kröner LU (2006)。 「アブサン - レビュー」。Crit Rev Food Sci Nutr。46 (5): 365–77 .土井: 10.1080/10408690590957322。PMID 16891209。S2CID 43251156。
- ^バジェノワ ED、アシュラフォワ RA、アリエフ KU、トゥリャガノフ、PD (1977)。化学。概要. 87 : 193909f.
{{cite journal}}: CS1 maint: 無題の定期刊行物 (リンク) - ^ a b c Zhang W, Luo S, Fang F, et al. (2005年1月). 「アブシンチンの全合成」 . Journal of the American Chemical Society . 127 (1): 18– 19. Bibcode : 2005JAChS.127...18Z . doi : 10.1021/ja0439219 . PMID 15631427 .
- ^クラーカーJW、フランセン MC、デ グルート A、ケーニッヒ WA、ボウメースター HJ (1998 年 8 月) 。「(+)-ゲルマクレン A 生合成: チコリにおける苦いセスキテルペン ラクトンの生合成における重要なステップ」。植物の生理学。117 (4): 1381–92 .土井: 10.1104/pp.117.4.1381。PMC 34902。PMID 9701594。
- ^ Kelsey, RG, Shafizadeh, F. (1979). 「アルテミシア属のセスキテルペンラクトンと系統分類」. Phytochemistry . 18 (10): 1591– 1611. Bibcode : 1979PChem..18.1591K . doi : 10.1016/0031-9422(79)80167-3 .
- ^ a b c d e f g de Kraker JW, Franssen MC, Dalm MC, de Groot A, Bouwmeester HJ (2001年4月). 「チコリ根におけるゲルマクレンAカルボン酸の生合成.セスキテルペンラクトン生合成に関与するシトクロムP450 (+)-ゲルマクレンAヒドロキシラーゼとNADP+依存性セスキテルペノイド脱水素酵素の証明」 . Plant Physiol . 125 (4): 1930– 40. doi : 10.1104/pp.125.4.1930 . PMC 88848. PMID 11299372 .
外部リンク
 ウィキメディア・コモンズのアブシンチン関連メディア
ウィキメディア・コモンズのアブシンチン関連メディア


