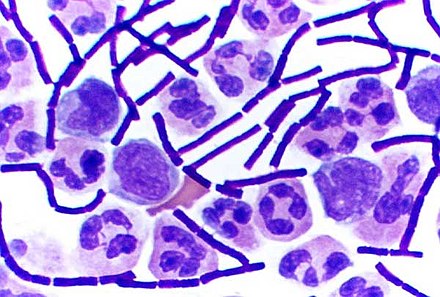
炭疽菌
 |
| 炭疽菌 | |
|---|---|
 | |
| 炭疽病の特徴である黒色の焼痂を伴う皮膚病変 | |
| 専門 | 感染症 |
| 症状 | 皮膚型:小さな水疱と周囲の腫れ 吸入型:発熱、胸痛、息切れ 腸型:吐き気、嘔吐、下痢、腹痛 注射型:発熱、膿瘍[ 1 ] |
| 通常の発症 | 接触後1日~2ヶ月[ 1 ] |
| 原因 | 炭疽菌[ 2 ] |
| 危険因子 | 動物を扱う仕事、旅行者、郵便局員、軍人[ 3 ] |
| 診断方法 | 血液中の抗体または毒素に基づき、微生物培養[ 4 ] |
| 予防 | 炭疽菌ワクチン接種、抗生物質[ 3 ] [ 5 ] |
| 治療 | 抗生物質、抗毒素[ 6 ] |
| 予後 | 治療を受けない場合、20~80%が死亡する[ 5 ] [ 7 ] |
| 頻度 | 年間2,000件以上[ 8 ] |
炭疽は、炭疽菌またはセレウス菌バイオ亜型炭疽菌という細菌 によって引き起こされる感染症です。[ 2 ]感染は通常、皮膚との接触、吸入、または腸管吸収によって起こります。[ 9 ]症状の発症は、感染後1日~2ヶ月です。[ 1 ]皮膚型では、小さな水疱とその周囲に腫れが現れ、多くの場合、中心が黒くなった無痛性の潰瘍に変化します。 [ 1 ]吸入型では、発熱、胸痛、息切れが見られます。[ 1 ]腸管型では、下痢(血が混じる場合もあります)、腹痛、吐き気、嘔吐が見られます。[ 1 ]
米国疾病管理予防センター(CDC)によると、皮膚炭疽病の最初の臨床的記述は、1752年にマレー、1769年にフルニエによってなされました。[ 10 ]それ以前は、炭疽病は歴史的記録にのみ記載されていました。ドイツの科学者ロベルト・コッホは、炭疽病の原因菌として炭疽菌(Bacillus anthracis)を初めて特定しました。 [ 10 ]
炭疽病は、感染性のある動物性食品に多く含まれる細菌の胞子との接触によって広がります。[ 11 ]接触には、吸入、飲食、または皮膚の損傷部位を介しての感染が含まれます。[ 11 ]通常、人から人へ直接広がることはありません。[ 11 ]危険因子には、動物や動物性食品を扱う人、軍人などがあります。[ 3 ]診断は、血液中の抗体または毒素の検出、または感染部位からのサンプルの培養によって確定されます。 [ 4 ]
炭疽菌ワクチンは、感染リスクの高い人に推奨されます。[ 3 ]炭疽菌に対する動物の予防接種は、過去に感染が発生した地域で推奨されます。[ 11 ]曝露後にシプロフロキサシン、レボフロキサシン、ドキシサイクリンなどの抗生物質を2ヶ月間投与することでも感染を予防できます。[ 5 ]感染した場合は、抗生物質と抗毒素による治療が行われます。[ 6 ]使用する抗生物質の種類と数は、感染の種類によって異なります。[ 5 ]感染が広範囲に及んでいる人には抗毒素が推奨されます。[ 5 ]
まれな病気であるヒト炭疽病は、アフリカ、中央アジア、南アジアで最もよく見られます。[ 12 ]南ヨーロッパでは他の大陸よりも頻繁に発生し、北ヨーロッパと北アメリカではまれです。[ 13 ]世界では、少なくとも年間2,000件の症例が発生し、米国では年間約2件です。[ 8 ] [ 14 ]皮膚感染症が症例の95%以上を占めています。[ 7 ]治療しない場合、皮膚炭疽病による死亡リスクは23.7%です。[ 5 ]腸管感染症の場合、死亡リスクは25〜75%ですが、呼吸器炭疽病の死亡率は、治療しても50〜80%です。[ 5 ] [ 7 ] 20世紀まで、炭疽病感染症は毎年何十万人もの人々と動物の命を奪っていました。[ 15 ]草食動物では、放牧中に胞子を食べたり、吸い込んだりすることで感染します。[ 12 ]人間は感染した動物を殺したり、食べたりすることで感染する可能性があります。[ 12 ]
いくつかの国や非国家グループが炭疽菌を兵器として開発している。[ 7 ]炭疽菌は1916年以来、生物兵器やバイオテロに使用されている。兵器化された炭疽菌の運搬方法としては、空中散布や家畜を介した散布が考えられる。第二次世界大戦では、大日本帝国の731部隊が中国に対して開発・使用したほか、イギリスのナチス・ドイツに対する計画でも研究された。ソ連、アメリカ、イラクの生物兵器計画では、兵器化された菌株が開発された。1975年、生物兵器禁止条約は生物兵器の「開発、生産、備蓄」を禁止した。それ以来、炭疽菌はバイオテロに使用されており、 2001年の米国炭疽菌攻撃や1993年の日本のオウム真理教による事件などがその例である。
語源
英語名は、ギリシャ語で石炭を意味するanthrax(ἄνθραξ )に由来し、 [ 16 ] [ 17 ]おそらくエジプト語源である[ 18 ] 。これは、皮膚炭疽菌感染症に罹患した人に特徴的な黒い皮膚病変が生じることに由来する。鮮やかな赤色の皮膚に囲まれた中央の黒い痂皮は、この病気の典型的な病変として古くから認識されてきた。英語で「anthrax」という語が初めて記録されたのは、1398年に翻訳されたバルトロメウス・アングリクスの著書『物の性質について』(1240年)である。[ 19 ]
炭疽病は歴史的に、症状、発生場所、そして感染しやすいと考えられていた集団に応じて、様々な名称で知られていました。シベリアペスト、カンバーランド病、炭疽病、脾臓熱、悪性浮腫、羊毛選別者病、ブラッドフォード病などです。[ 20 ]
徴候と症状
皮膚


.jpg/440px-Riehl_Zumbusch_Tafel_IV_(2).jpg)
皮膚炭疽病(ハイドポーター病とも呼ばれる)は、皮膚に炭疽が発生する病気です。最も多く(症例の90%以上)発生し、危険性も最も低い(治療による死亡率は低いが、治療しない場合の死亡率は23.7%)。[ 21 ] [ 5 ]皮膚炭疽病は、腫れ物のような皮膚病変として現れ、最終的には中心部が黒色になる潰瘍(痂皮)を形成します。黒色の焼痂は、多くの場合、感染部位に黒く黒い点(パンカビに似た形状)として集中し、刺激や痒みを伴う大きな皮膚病変または水疱として現れ、痛みを伴わない壊死性潰瘍となります。一般的に、皮膚感染症は、曝露後2~5日で胞子侵入部位に形成されます。あざや他のほとんどの病変とは異なり、皮膚炭疽感染症は通常、痛みを引き起こしません。近くのリンパ節が感染し、赤くなり、腫れ、痛みを伴う場合があります。病変の上にすぐにかさぶたができ、数週間で剥がれます。完全な回復にはさらに時間がかかる場合があります。[ 22 ]皮膚炭疽は、通常、炭疽菌の胞子が皮膚の切り傷から侵入することで発生します。この形態は、感染した動物や動物性製品を扱った場合に最もよく見られます。[ 23 ]
注射
2009年12月、スコットランドのグラスゴーとスターリング地域で注射ヘロイン使用者の間で炭疽菌の発生が発生し、14人が死亡した。[ 24 ]これは1960年以来イギリスで初めて記録された非職業性のヒト炭疽菌発生であった。[ 24 ]炭疽菌の発生源は、アフガニスタンで骨粉でヘロインを薄めたものと考えられている。 [ 25 ]注射による炭疽菌は、黒い部分を除いて皮膚炭疽菌に似た症状を示す可能性があり、[ 26 ]筋肉の深部に感染を引き起こし、より速く広がる可能性がある。[ 27 ]これにより認識と治療が困難になる可能性がある。
肺
吸入炭疽病は通常、曝露後1週間以内に発症しますが、最大2か月かかることもあります。[ 28 ]発症後数日間は、ほとんどの人に発熱、悪寒、倦怠感が現れます。[ 28 ]これらの症状には、咳、息切れ、胸痛、吐き気や嘔吐が伴う場合があり、吸入炭疽病をインフルエンザや市中肺炎と区別することが困難です。[ 28 ]これはしばしば前駆期と呼ばれます。[ 28 ]
翌日か翌々日には、息切れ、咳、胸痛がより一般的になるとともに、吐き気、嘔吐、精神状態の変化、発汗、頭痛など、胸部に関係しない症状が3分の1以上の人に現れる。[ 28 ]上気道症状は4分の1の人にしか現れず、筋肉痛はまれである。[ 28 ]精神状態の変化や息切れは、一般的に患者を医療機関に呼び込み、病気の劇症期を示す。[ 28 ]
肺自体ではなく、まず胸部のリンパ節に感染し、出血性縦隔炎と呼ばれる状態になります。胸腔内に血が溜まり、息切れを引き起こします。第二段階(肺炎)は、感染がリンパ節から肺に広がることで発生します。第二段階の症状は、第一段階の症状から数時間または数日以内に突然現れます。症状には、高熱、極度の息切れ、ショック、そして致死的な場合には48時間以内に急死するなどがあります。[ 29 ]
消化器系
消化管感染症は、炭疽菌に汚染された肉の摂取によって引き起こされることが多く、下痢(場合によっては血便)、腹痛、腸管の急性炎症、食欲不振などの症状を呈します。[ 30 ]吐血を伴う場合もあります。腸管、口腔、咽喉に病変が認められることもあります。炭疽菌は消化管に侵入すると、毒素を作り続けながら血流を介して全身に広がります。[ 31 ]
原因
細菌

炭疽菌は桿菌で、グラム陽性、通性嫌気性菌[ 32 ]の大きさが約 1 x 9 μm である。[ 2 ]この菌が病気を引き起こすことは、1876 年にロバート コッホが感染した牛から血液サンプルを採取し、菌を分離してマウスに移植したときに示された。 [ 33 ]この菌は通常、土壌中に胞子の形で存在し、この状態で数十年生存することができる。草食動物は、特にざらざらした、刺激性の、またはとがった植物を食べるときに、放牧中に感染することが多い。植物は消化管内に傷を引き起こし、細菌の胞子が組織に入り込むことを可能にすると考えられている。細菌は摂取されるか、開いた傷口に入ると、動物または人間の体内で増殖し始め、通常は数日または数週間以内に宿主を殺します。胞子は組織に侵入した部位で発芽し、その後循環によってリンパ管に広がり、そこで細菌が増殖します。[ 34 ]
炭疽菌は2種類の強力な外毒素と致死性の毒素を産生し、死に至らしめる。獣医師は、突然の死と体腔から滲み出る黒っぽい非凝固性の血液から、炭疽菌による死の可能性を見抜くことができる。死後、体内に残る炭疽菌のほとんどは、死後数分から数時間以内に嫌気性細菌に駆逐され消滅するが、出血や死骸の切開によって体外に排出された栄養型炭疽菌は、頑強な胞子を形成することがある。これらの栄養型細菌は伝染性ではない。[ 35 ]栄養型細菌1個につき1つの胞子が形成される。胞子形成の誘因は不明であるが、酸素分圧や栄養不足が関与している可能性がある。一度形成された胞子を根絶するのは非常に困難である。[ 36 ]
草食動物(および時折人間)の吸入による感染は、通常、吸入された胞子が気道を通って肺にある小さな気嚢(肺胞)に運ばれることから始まります。胞子は次に肺の清掃細胞(マクロファージ)に拾われ、小血管(リンパ管)を通って中央胸腔(縦隔)のリンパ節に運ばれます。炭疽菌の胞子と桿菌によって中央胸腔が損傷されると、胸痛や呼吸困難が起こることがあります。リンパ節に入った胞子は活性桿菌に発芽し、増殖して最終的にマクロファージを破裂させ、より多くの桿菌が血流に放出され、全身に広がります。血流に入ったこれらの桿菌は、致死因子、浮腫因子、防御抗原という3つのタンパク質を放出します。この3つはそれ自体には毒性はありませんが、組み合わせると人間にとって非常に致命的です。[ 37 ]防御抗原は他の2つの因子と結合して、それぞれ致死毒素と浮腫毒素を形成します。これらの毒素は、宿主の組織破壊、出血、そして死の主な原因となります。抗生物質の投与が遅すぎると、たとえ抗生物質によって細菌が根絶されたとしても、細菌が産生する毒素が致死量レベルで体内に残留するため、一部の宿主は中毒症で死亡します。[ 38 ]
- 炭疽菌
曝露と伝播
炭疽菌は、腸 (胃腸)、肺 (肺)、または皮膚 (経皮) を通じて人体に侵入し、侵入部位に応じて異なる臨床症状を引き起こします。[ 14 ]炭疽菌は通常、感染した人から感染していない人に広がることはありません。[ 14 ]この病気が人の体にとって致命的である場合、炭疽菌の塊が他の人への感染源となる可能性があり、さらなる汚染を防ぐために特別な予防措置を講じる必要があります。[ 14 ]肺炭疽菌は、治療せずに放置すると、ほぼ常に致命的です。[ 14 ]歴史的に、肺炭疽菌は羊毛の選別を行う人々の職業上の危険であったため、羊毛選別者病と呼ばれていました。[ 39 ]今日、この形態の感染症は先進国では非常にまれです。[ 39 ]皮膚炭疽菌は最も一般的な感染形態ですが、3 つの感染形態の中で最も危険性が低いものでもあります。[ 9 ]消化管炭疽病は治療せずに放置すると致命的になる可能性が高いが、非常にまれである。[ 9 ]

炭疽菌の胞子は、厳しい環境下で数十年、あるいは数世紀にもわたり生存することができる。[ 40 ]このような胞子は、南極大陸を含むすべての大陸で発見される。[ 41 ]感染した動物の墓地が荒らされると、70年後に感染を引き起こすことが知られている。[ 42 ]そのような事例の1つでは、接触の75年前のトナカイの死体が解凍されたことが原因で、少年が消化管炭疽病で死亡した。[ 43 ]炭疽菌の胞子は飲料水として使用される地下水を介して拡散し、数十人が入院したが、その多くは子供であった。[ 43 ]感染した動物やその製品(皮、羊毛、肉など)への職業上の曝露は、人間にとって通常の曝露経路である。[ 44 ]動物の死骸や動物製品に曝露した労働者は、特に炭疽病がより一般的である国では、最もリスクが高い。[ 44 ]野生動物と混じり合う野外で放牧されている家畜 における炭疽病は、米国やその他の地域で今でも時折発生している。 [ 44 ]米国では、金属加工が炭疽病に酷似した病気の危険因子として注目されている。[ 45 ]
羊毛や動物の皮を扱う労働者の多くは、日常的に低レベルの炭疽菌胞子に曝露されているが、ほとんどの曝露レベルは感染を引き起こすのに十分ではない。[ 46 ]致死的な感染は、約10,000~20,000個の胞子を吸入することで起こると報告されているが、この量は宿主の種によって異なる。[ 46 ]
メカニズム
炭疽病の致死性は、細菌の2つの主要な毒性因子によるものです。1つはポリD-グルタミン酸莢膜で、宿主の好中球による貪食から細菌を保護します。もう1つは炭疽毒素と呼ばれる3成分からなるタンパク質毒素で、防御抗原(PA)、浮腫因子(EF)、致死因子(LF)で構成されています。[ 47 ] PAとLFは致死毒素を産生し、PAとEFは浮腫毒素を産生します。これらの毒素はそれぞれ死と組織の腫脹(浮腫)を引き起こします。細胞に侵入するために、浮腫因子と致死因子は、炭疽菌が産生する防御抗原と呼ばれる別のタンパク質を使用します。防御抗原は宿主細胞の2つの表面受容体に結合します。その後、細胞プロテアーゼがPAを2つの断片、PA 20とPA 63に切断しますPA 20は細胞外液に解離し、毒性サイクルにおいてそれ以上の役割を果たさない。その後、 PA 63は他の6つのPA 63断片とオリゴマー化し、プレポアと呼ばれる7量体の環状構造を形成する。この形状になると、複合体は最大3つのEFまたはLFと競合的に結合し、耐性複合体を形成する。[ 37 ]次に受容体を介したエンドサイトーシスが起こり、新たに形成された毒性複合体は宿主細胞内部に侵入する。エンドソーム内の酸性環境は、7量体を活性化し、LFおよび/またはEFを細胞質に放出する。[ 48 ]この複合体がどのようにして細胞死をもたらすのかは、正確には分かっていない。
浮腫因子はカルモジュリン依存性アデニル酸シクラーゼである。アデニル酸シクラーゼは ATP からサイクリック AMP (cAMP) とピロリン酸への変換を触媒する。アデニル酸シクラーゼとカルモジュリンの複合体形成により、カルモジュリンはカルシウム誘導性シグナル伝達を刺激できなくなり、免疫応答が抑制される。[ 37 ]具体的には、LF は前述のプロセスによって好中球(貪食細胞の一種) を不活性化し、細菌を貪食できないようにする。歴史的に、致死因子はマクロファージにTNFとインターロイキン 1 ベータ(IL1β) を産生させると考えられてきた。TNF はサイトカインであり、その主な役割は免疫細胞を制御することであり、炎症とアポトーシスまたはプログラム細胞死を誘導することである。インターロイキン 1 ベータも炎症とアポトーシスを制御する別のサイトカインである。 TNFとIL-1βの過剰産生は、最終的に敗血症性ショックと死に至ります。しかしながら、最近のエビデンスによると、炭疽菌は心膜腔、胸膜腔、腹腔などの重篤な体腔、リンパ管、血管の内皮細胞も標的とし、体液や細胞の血管漏出を引き起こし、最終的には循環血液量減少性ショックと敗血症性ショックを引き起こすことが示唆されています。
診断

臨床材料中の炭疽菌を直接同定するために、様々な技術が用いられる場合があります。まず、検体をグラム染色します。バチルス属細菌は非常に大きく(長さ3~4μm)、長い鎖状に増殖することがあり、グラム陽性染色を示します。微生物が炭疽菌であることを確認するために、ポリメラーゼ連鎖反応に基づくアッセイや免疫蛍光顕微鏡検査などの迅速診断技術が使用される場合があります。[ 49 ]
すべてのバチルス属菌は、5%羊血液寒天培地およびその他の一般的な培養培地でよく増殖します。炭疽菌は、汚染された検体から分離するためにポリミキシン-リゾチーム-EDTA-酢酸タリウムを用いて分離することができ、重炭酸塩寒天培地は莢膜形成を誘導する同定方法として用いられます。バチルス属菌は通常、35℃、室温、または5% CO2の条件下で培養すると24時間以内に増殖します。重炭酸塩寒天培地を同定に使用する場合は、培地を5% CO2中で培養する必要があります。炭疽菌のコロニーは、中~大型で、灰色、扁平、不規則な形状をしており、渦巻き状の突起を有し、「クラゲの頭」のような外観を呈すると言われています。また、5%羊血液寒天培地では溶血性を示しません。この細菌は運動性がなく、ペニシリンに感受性があり、卵黄寒天培地上で広い範囲にレシチナーゼを産生する。炭疽菌の確定診断には、ガンマバクテリオファージ試験、間接赤血球凝集反応、抗体検出のための酵素結合免疫吸着法などがある。[ 50 ]炭疽菌の確定診断に最も適した沈降試験はアスコリ試験である。
予防
炭疽菌が潜伏している疑いのある遺体の皮膚や、体液との接触を避けるための予防措置が講じられます。[ 51 ]遺体は厳重に隔離する必要があります。血液サンプルを採取し、容器に密封して認可された研究所で分析し、炭疽菌が死因であるかどうかを確認します。遺体は気密性の高い納体袋に密封し、炭疽菌胞子の伝染を防ぐため焼却する必要があります。ポリクロームメチレンブルー(マクファディアン染色)で染色した血液塗抹標本中の、通常は非常に多数の莢膜を持つ桿菌を顕微鏡で観察することで、完全な診断が可能ですが、病原体の培養は依然として診断のゴールドスタンダードです。他者への汚染を防ぐために、遺体を完全に隔離することが重要です。[ 51 ]
遺体を取り扱う際には、ゴム手袋、ゴムエプロン、穴の開いていないゴム長靴などの不浸透性の防護服や防護具を使用する。特に傷や擦り傷がある場合は、皮膚を露出させてはならない。使い捨ての個人用保護具が望ましいが、入手できない場合はオートクレーブで除染することができる。使用済みの使い捨て用具は、使用後に焼却または埋め立てる。汚染された寝具や衣類はすべて二重のビニール袋に入れて隔離し、バイオハザード廃棄物として処理する。[ 51 ]米国国立労働安全衛生研究所(NIOSH)および鉱山安全衛生局(MSH)承認の高効率呼吸器など、小さな粒子を濾過できる呼吸器を着用する。 [ 52 ]ワンヘルスの観点から炭疽菌に対処することで、感染リスクが低減し、人間と動物の両方をより適切に保護することができる。[ 53 ]
ワクチン
家畜およびヒト用の炭疽菌ワクチンは、医学の歴史において重要な位置を占めてきました。フランスの科学者ルイ・パスツールは、 1881年に最初の効果的な獣医用ワクチンを開発しました。 [ 54 ] [ 55 ] [ 56 ]ヒト炭疽菌ワクチンは、1930年代後半にソビエト連邦で、1950年代に米国と英国で開発されました。現在FDA(米国食品医薬品局)が承認している米国のワクチンは、1960年代に開発されました。[ 57 ]
現在投与されているヒト炭疽菌ワクチンには、無細胞サブユニットワクチン(米国)と生ワクチン(ロシア)の種類がある。現在使用されている炭疽菌ワクチンはすべて、かなりの局所的および全身的反応性(紅斑、硬結、痛み、発熱)を示し、重篤な副作用が接種者の約1%に起こる。[ 58 ]米国製品のBioThraxはFDAの認可を受けており、以前は0、2、4週と6、12、18か月の6回投与の初回シリーズで投与され、免疫を維持するために毎年追加接種が行われていた。2008年にFDAは2週目の投与を省略することを承認し、現在は5回投与のシリーズが推奨されている。[ 59 ]この5回投与シリーズは、軍人、炭疽菌を取り扱う科学者、およびリスクを伴う仕事をしている一般人が接種できる。[ 60 ]現在研究されている新しい第二世代ワクチンには、組換え生ワクチンと組換えサブユニットワクチンがあります。20世紀には、生物兵器における炭疽菌の使用からアメリカ軍を守るために、現代の製品(バイオスラックス)が使用されたことが物議を醸しました。[ 61 ]
抗生物質
曝露した人には予防的な抗生物質の投与が推奨されます。[ 5 ]炭疽菌感染源を早期に発見することで、予防措置を講じることができます。2001年10月の炭疽菌攻撃を受けて、米国郵政公社(USPS)は大規模な郵便処理施設に生物検出システム(BDS)を設置しました。BDS対応計画は、消防、警察、病院、公衆衛生などの地元の対応機関と協力してUSPSによって策定されました。これらの施設の従業員は、炭疽菌、対応措置、予防薬について教育を受けています。炭疽菌が使用されたことの最終確認には時間差があるため、曝露の可能性のある人員に対する予防的な抗生物質治療はできるだけ早く開始する必要があります
治療
炭疽は、皮膚炭疽からの皮膚滲出液がまれに認められる場合を除いて、人から人へは感染しません。[ 62 ]しかし、人の衣類や身体が炭疽菌の胞子で汚染されている可能性があります。人を効果的に除染するには、抗菌石鹸と水で徹底的に洗い流します。廃水は漂白剤または他の抗菌剤で処理します。[ 63 ]物品を効果的に除染するには、30分以上お湯で煮沸します。塩素系漂白剤は表面の胞子や栄養細胞を破壊するのに効果がありませんが、ホルムアルデヒドは有効です。衣類を燃やすと胞子を破壊するのに非常に効果的です。除染後は、同じ感染源にさらされていない限り、炭疽病患者との接触者に対して予防接種、治療、隔離を行う必要はありません。
抗生物質
炭疽病の早期抗生物質治療は不可欠であり、治療が遅れると生存率が大幅に低下します。炭疽病やその他の細菌感染症の治療には、フルオロキノロン系薬剤(シプロフロキサシン)、ドキシサイクリン、エリスロマイシン、バンコマイシン、ペニシリンなどの大量の静脈内および経口抗生物質が含まれます。FDA承認の薬剤には、シプロフロキサシン、ドキシサイクリン、ペニシリンなどがあります。[ 64 ]肺炭疽病の疑いがある場合、死亡を防ぐために早期の抗生物質予防治療が不可欠です。炭疽病に対する新薬の開発には多くの試みが行われてきましたが、既存の薬でも早期に治療を開始すれば効果的です。[ 65 ]
モノクローナル抗体
2009年5月、ヒューマン・ゲノム・サイエンシズは、吸入炭疽病の緊急治療を目的とした新薬ラキシバクマブ(商品名ABthrax)の生物学的製剤承認申請(BLA、販売許可)を提出した。 [ 66 ] 2012年12月14日、米国食品医薬品局は、吸入炭疽病の治療薬としてラキシバクマブ注射剤を承認した。ラキシバクマブは、炭疽菌が産生する毒素を中和するモノクローナル抗体である。[ 67 ] 2016年3月、FDAは、炭疽菌が産生する毒素を中和するモノクローナル抗体を用いた2つ目の炭疽病治療薬を承認した。オビルトキサキシマブは、適切な抗菌薬との併用による吸入炭疽病の治療、および代替療法が利用できないまたは適切でない場合の予防のために承認されている。[ 68 ]
炭疽菌免疫グロブリン
2015年、炭疽菌免疫グロブリンはFDAによって承認されました。これは、炭疽菌ワクチン接種を受けた人の血漿から産生されるヒト免疫グロブリンです。その作用機序は、炭疽菌毒素を不活化する炭疽菌に対するモノクローナル抗体治療とは異なります。免疫剤として、体内で炭疽菌に対する自然免疫応答を高めます。[ 69 ] 重篤な副作用には、血栓症、溶血、無菌性髄膜炎、TRALI、アナフィラキシーなどがあります。[ 70 ]
薬剤耐性、抗体耐性、ワクチン耐性炭疽菌に対する生物学的製剤
多剤耐性、抗体耐性、ワクチン耐性炭疽菌の治療も可能です。Leglerら[ 71 ]は、ペグ化CapD(莢膜脱重合酵素)が、抗生物質、モノクローナル抗体、ワクチンを使用せずに、致死性エイムズ胞子によるLD50曝露に対する防御効果を発揮できることを示しました。CapD酵素は、細菌からポリ-D-グルタミン酸(PDGA)莢膜物質を除去し、自然免疫応答の感受性を高めます。莢膜のない細菌は、その後、排除されます。[ 72 ]

予後
皮膚炭疽は、感染部位が皮膚に限定されているため、致死因子、浮腫因子、防御抗原が重要な臓器に侵入して破壊するのを防ぐため、治療すれば致死的になることはほとんどありません[ 75 ]。治療を行わない場合、皮膚感染症の最大20%が中毒症に進行し、死亡します[ 76 ]
2001年以前は、吸入炭疽病の致死率は90%でしたが、それ以降は45%に低下しました。[ 28 ]吸入炭疽病が劇症化段階に進行した人はほぼ必ず死亡し、ある症例研究では死亡率が97%であることが示されています。[ 77 ]炭疽菌性髄膜脳炎もほぼ必ず致命的です。[ 78 ]
消化管炭疽感染症は治療可能ですが、治療開始時期に応じて、通常、死亡率は 25% ~ 60% になります。
注射炭疽病は炭疽病の中で最も稀な形態であり、ヘロインを注射する薬物使用者のグループでのみ発生したことが確認されている。[ 76 ]
疫学
世界では、年間少なくとも2,000件の症例が発生しています。[ 8 ]
アメリカ合衆国
アメリカ合衆国における最後の自然肺炭疽菌による死亡例は、1976年にカリフォルニア州で発生しました。パキスタンから輸入された汚染された羊毛を扱った家庭の織工が死亡したのです。病気の蔓延を最小限に抑えるため、遺体は密閉された金属製の容器に入れられた密閉プラスチック製の遺体袋でUCLAに搬送され、検死が行われました。 [ 79 ]
消化管炭疽病はアメリカ合衆国では非常に稀で、記録に残る症例は2件のみである。疾病管理予防センターによると、最初の症例は1942年に報告された。[ 80 ] 2009年12月、ニューハンプシャー州保健福祉省は成人女性の消化管炭疽病症例を確認した。CDCは感染源を調査し、女性がドラムサークルに参加していた際に使用したアフリカの太鼓から感染した可能性を検討した。[ 81 ]女性は太鼓の皮から胞子状の炭疽菌を吸入したとみられる。彼女は重篤になったが、吸入炭疽病ではなく消化管炭疽病であったため、アメリカの医療史上特異な例となった。感染が起きた建物は清掃されて再び一般に公開され、女性は回復した。ニューハンプシャー州の疫学者ジョディ・ディオンヌ・オドム氏は、「これは謎だ。なぜこんなことが起こったのか、本当に分からない」と述べた。[ 82 ]
2007年、コネチカット州ダンベリーで皮膚炭疽病の症例が2件報告されました。この症例は、伝統的なアフリカ風の太鼓を作る職人が、ニューヨーク市のディーラーから購入したヤギの皮(税関で既に通関済み)を扱っていた際に発生しました。皮を削っている最中にクモに噛まれ、胞子が血流に入り込みました。彼の息子も感染しました。[ 83 ]
1997年以降に発生した複数の症例は金属加工労働者、特に溶接工に関係しており、2022年の研究で「溶接工炭疽病」という用語が生まれました。金属加工と炭疽病の正確な関係は不明ですが、CDCの研究者による2022年の研究では、溶接から発生する金属煙が免疫抑制効果を持つ可能性があると推測されています。この研究ではまた、炭疽菌とセレウス菌は生存に鉄を必要とするため、溶接工は肺に過剰な鉄を蓄積する可能性があることも指摘されています。[ 84 ] [ 85 ]
クロアチア
2022年7月、サヴァ川沿いの氾濫原であるロニュスコ・ポリェの自然公園で、数十頭の牛が炭疽菌で死亡し、6人が軽度の皮膚症状で入院しました。[ 86 ]
イギリス
2008年11月、未処理の動物の皮を扱っていたイギリスの太鼓職人が炭疽菌で死亡した。[ 87 ] 2009年12月、スコットランドのグラスゴーとスターリング地域でヘロイン中毒者の間で炭疽菌の流行が発生し、14人が死亡した。[ 24 ]炭疽菌の発生源は、アフガニスタンでヘロインを骨粉で薄めたものと考えられている。[ 25 ]
歴史
発見
ドイツの医師であり科学者であったロベルト・コッホは、1875年にヴォルシュタイン(現在のポーランド、ヴォルシュティン)で炭疽病を引き起こす細菌を初めて特定しました。[ 33 ] [ 88 ] 19世紀後半の彼の先駆的な研究は、病気が微生物によって引き起こされる可能性があることを初めて実証したものの一つでした。画期的な一連の実験で、彼は炭疽菌のライフサイクルと感染経路を明らかにしました。彼の実験は、炭疽菌への理解を深めるだけでなく、自然発生説と細胞説をめぐる議論がまだ続いていた時代に、微生物が病気を引き起こす役割を解明するのにも役立ちました。コッホはその後、他の病気のメカニズムを研究し、結核を引き起こす細菌の発見により1905年のノーベル生理学・医学賞を受賞しました。 [ 89 ]
炭疽病の理解に最も大きな理論的貢献をしたのはコッホであると言えるが、他の研究者たちは、この病気をいかに予防するかという実践的な問題により関心を寄せていた。英国では、炭疽病は羊毛、梳毛、皮革、なめし革産業の労働者に影響を与え、恐怖の対象となっていた。ブラッドフォードに生まれ、同地を拠点とする医師ジョン・ヘンリー・ベルは、謎めいた致命的な「羊毛選別者病」と炭疽病を初めて関連づけ、1878年に両者が同一であることを示しました。[ 90 ] 20世紀初頭、幼少期に家族と共にブラッドフォードに定住したドイツ人細菌学者フリードリヒ・ヴィルヘルム・オイリッヒは、地元の炭疽病調査委員会で重要な研究を行った。オイリッヒはまた、1913年に設立された内務省の省庁調査委員会にも貴重な貢献をした。この委員会は、産業炭疽病という継続的な問題に対処するため設置された。[ 91 ]この立場での彼の仕事は、工場検査官のG・エルムハースト・ダッケリングとの協力が中心でしたが、炭疽菌予防法(1919年)の制定に直接つながりました。
最初のワクチン接種

19世紀、炭疽菌はフランスをはじめとする多くの国で大きな経済的課題となりました。馬、牛、羊は特に脆弱であり、ワクチン製造の研究のために国の資金が確保されました。フランスの科学者ルイ・パスツールは、重要なワイン産業と絹産業を守るのに役立つ方法の開発に成功した後、ワクチン製造を任されました。[ 92 ]
1881年5月、パスツールは助手のジャン=ジョゼフ・アンリ・トゥーサン、エミール・ルーらと共同で、プイィ・ル・フォールでワクチン接種の概念を実証する公開実験を行った。パスツールは羊25頭、ヤギ1頭、牛数頭からなる2つのグループを用意した。一方のグループの動物には、パスツールが調製した炭疽菌ワクチンを15日間隔で2回接種した。対照群にはワクチン接種を行わなかった。最初の接種から30日後、両グループに生きた炭疽菌の培養液を接種した。ワクチン接種を受けなかったグループの動物はすべて死亡したが、ワクチン接種を受けたグループの動物はすべて生き残った。[ 93 ]
この一見すると成功したように見える成果は、地元、国内、そして国際的な報道機関で広く報じられ、パスツールはワクチンをフランス国外へ輸出しようと精力的に努力しました。彼はその著名人としての地位を利用して、ヨーロッパとアジア各地にパスツール研究所を設立し、甥のアドリアン・ロアは1888年にオーストラリアを訪れ、ニューサウスウェールズ州で炭疽菌対策としてワクチンの導入を試みました。[ 94 ]結局、このワクチンはオーストラリアの農村部の厳しい気候では効果がなく、すぐに地元の研究者ジョン・ガンとジョン・マクガービー・スミスが開発したより強力なワクチンに取って代わられました。[ 95 ]
炭疽菌に対するヒトワクチンは1954年に利用可能になった。これは、獣医学で使用されていたパスツール型生細胞ワクチンではなく、無細胞ワクチンであった。改良された無細胞ワクチンは1970年に利用可能になった。[ 96 ]
遺伝子組み換え株
- トリエステ生まれの免疫学者マックス・スターンにちなんで名付けられた炭疽菌のスターン株は、炭疽菌毒素毒性プラスミドのみを含み、ポリグルタミン酸カプセル発現プラスミドを含まない、ワクチンとして使用される弱毒化株です。
- 1980年代にソ連の生物兵器計画によって作られた836株は、後にロサンゼルス・タイムズ紙によって「人類が知る炭疽菌の中で最も毒性が強く凶暴な株」と称された。[ 97 ] [ 98 ]
- 2001年の米国炭疽菌攻撃で使用された毒性の強いエイムズ株は、炭疽菌によるアウトブレイクの中で最も多くの報道を集めました。エイムズ株には2つの毒性プラスミドが含まれており、それぞれが炭疽菌毒素と呼ばれる3つのタンパク質からなる毒素とポリグルタミン酸カプセルをコードしています。
- それにもかかわらず、第二次世界大戦中に生物兵器として開発されたものの一度も使用されなかったVollum株の方がはるかに危険である。Vollum(誤ってVellumと呼ばれることもある)株は、1935年にオックスフォードシャーの牛から分離された。この同じ株は、グルイナード生物兵器実験で使用された。Vollumの変種である「Vollum 1B」は、1960年代に米国と英国の生物兵器計画で使用された。Vollum 1Bは、メリーランド州キャンプ(後のフォート)デトリックの米国陸軍生物戦研究所に勤務していた46歳の科学者、ウィリアム・A・ボイルズから分離されたと広く信じられている[99]。ボイルズは1951年にVollum株に偶然感染し死亡した。
社会と文化
現場の浄化
炭疽菌の芽胞は、放出後、環境中で非常に長期間生存することができます。炭疽菌に汚染された場所や物質を浄化するための化学的方法では、過酸化物、エチレンオキシド、サンディア泡沫剤、[ 100 ]二酸化塩素(ハート上院議員事務所ビルで使用)、[ 101 ]:8 過酢酸、オゾンガス、次亜塩素酸、過硫酸ナトリウム、次亜塩素酸ナトリウムを含む液体漂白剤などの酸化剤が使用される場合があります。炭疽菌の除染に有効であることが示されている非酸化剤には、臭化メチル、ホルムアルデヒド、メタムナトリウムなどがあります。これらの薬剤は細菌の芽胞を破壊します。前述の炭疽菌除染技術はすべて、米国環境保護庁(EPA)などが実施した実験室試験で有効であることが実証されています。[ 102 ]
炭疽菌胞子の除染技術は、胞子が付着している物質、温度や湿度などの環境要因、胞子の種類、炭疽菌株、使用される検査方法などの微生物学的要因によって影響を受ける。[ 103 ]
EPAは硬質表面処理用の漂白剤溶液を承認した。[ 104 ]二酸化塩素は炭疽菌汚染施設に対する優先的な殺生物剤として浮上しており、過去10年間に数多くの政府施設の処理に使用されてきた。[ 105 ]その主な欠点は、反応物をオンデマンドで入手するための現場処理が必要なことである。
このプロセスを加速させるために、鉄とテトラアミド大環状配位子からなる微量の無毒性触媒を炭酸ナトリウムと重炭酸ナトリウムと混合し、スプレー状にする。このスプレー剤を害虫が発生した場所に散布し、その後、tert-ブチルヒドロペルオキシドを含む別のスプレーを散布する。[ 106 ]
触媒法を用いると、30分以内に炭疽菌胞子を完全に破壊することができる。[ 106 ]標準的な触媒フリーの噴霧では、同じ時間内に胞子の半分以下しか破壊されない。
上院議員会館、汚染された郵便施設、そしてその他の米国政府および民間のオフィスビルの浄化作業は、環境保護庁(EPA)が主導する共同作業でした[ 101 ]。3 除染は可能ではあるものの、時間と費用がかかることが示されました。政府監査院(GAO)によると、上院議員会館の炭疽菌胞子除去には2,700万ドルの費用がかかりました。ワシントンD.C.のブレントウッド郵便施設の浄化には1億3,000万ドルの費用がかかり、26ヶ月かかりました。その後、より新しく、より費用のかからない方法が開発されました[ 107 ] 。
牧場や自然界における炭疽菌汚染地域の浄化は、はるかに問題が多い。死骸は焼却できるが[ 108 ]、大きな死骸を焼却するには3日かかる場合が多く、木材の少ない地域では現実的ではない。死骸は埋めることもできるが、胞子の再出現を防ぐのに十分な深さに大型動物を埋めるには、多くの人手と高価な道具が必要になる。胞子を殺すために死骸をホルムアルデヒドに浸すこともあったが、これには環境汚染の問題がある。炭疽菌が発生した場所を囲む広い範囲で植生をブロック焼きする試みがなされたが、これは環境破壊的ではあるが、健康な動物が死骸のある場所から新鮮な草を求めて移動する原因となる。野生生物保護活動家の中には、新鮮な炭疽菌の死骸を日よけ布や重いもので覆う実験を行った者もいる。これにより、一部の腐肉食動物が死骸を開けることができなくなり、死骸内の腐敗細菌が炭疽菌の栄養細胞を死滅させ、胞子形成を阻止することができます。ただし、この方法には欠点もあります。ハイエナなどの腐肉食動物は、ほぼあらゆる開口部から侵入することができるからです。
グルイナード島の実験場は国防省によってホルムアルデヒドと海水の混合物で除染されたと言われている。[ 109 ]同様の処理が米国の実験場に適用されたかどうかは明らかではない。
生物兵器

炭疽菌の胞子は生物兵器として使用されてきました。近代における最初の事例は、1916年、ドイツ参謀本部から供給された北欧の反乱軍がフィンランドでロシア帝国軍に対して炭疽菌を使用したことですが、その効果は不明です。[ 110 ]炭疽菌は、1930年代に満州で日本の関東軍731部隊によって生物兵器として初めて実験されました。この実験の一部には、戦争捕虜への意図的な感染が含まれており、数千人が死亡しました。当時、N剤と指定されていた炭疽菌は、1940年代に連合国によっても調査されました。[ 111 ]
1942年、ポートン・ダウンの英国人科学者らは、ベジタリアン作戦の研究を開始した。これは最終的に使われなかった生物兵器軍事作戦計画で、 Vollum-14578株の炭疽菌胞子に汚染された亜麻の種を含む動物飼料ペレットをナチス・ドイツの田園地帯に空輸するというものである。ペレットは牛が食べ、その牛が今度は人間に食べられることで、ドイツの戦争遂行に大きな妨害を与えることになっていた。同年、スコットランド高地の無人島グルイナード島で生物兵器のテストが実施され、ポートン・ダウンの科学者らは島の羊に対する炭疽菌の影響を研究した。最終的に500万個のペレットが作られたが、1944年にイギリス空軍の爆撃機を使用してドイツに投下する計画はオーバーロード作戦の成功とそれに続く連合軍によるフランスの解放の後、廃案になった。すべてのペレットは1945年に焼却炉で破壊されました。[ 112 ] [ 113 ] [ 114 ]
兵器化された炭疽菌は、米国が生物兵器禁止条約に署名した1972年以前、米国の備蓄の一部であった。[ 115 ]ニクソン大統領は1969年に米国の生物兵器計画の解体と既存の生物兵器備蓄の破棄を命じた。1978年から79年にかけて、ローデシア政府は反乱軍に対する作戦中に牛や人間に対して炭疽菌を使用した。[ 116 ]ソ連はヴォズロジェニヤ島のカントゥベクで100~200トンの炭疽菌胞子を製造・保管していたが、1992年に放棄され、2002年に破壊された。[ 117 ]
アメリカ軍とイギリス陸軍の隊員は、生物兵器攻撃の脅威がある地域では、任務に就く前に炭疽菌の予防接種を定期的に受けなくなりました。[ 61 ]
スベルドロフスク事件(1979年4月2日)
1972年に生物兵器生産停止協定に署名したにもかかわらず、ソ連政府はその後も生物兵器計画を継続し、数百トンの炭疽菌を生産した。1979年4月2日、モスクワの東約1,370キロに位置するスベルドロフスク(現在のロシア連邦エカテリンブルク)の100万人以上の住民の一部が、付近の生物兵器施設から偶然に漏れた炭疽菌にさらされた。少なくとも94人が感染し、そのうち68人以上が死亡した。漏れから4日後に1人が死亡し、死者数がピーク時には8日間で10人が死亡し、最後の1人は6週間後に死亡した。徹底的な清掃、ワクチン接種、医療介入により、約30人の犠牲者が救助された。[ 118 ] KGBによる広範囲にわたる隠蔽と記録の破壊は1979年からロシアのボリス・エリツィン大統領が1992年にこの炭疽菌事故を認めるまで続いた。ジャンヌ・ギユマンは1999年に、ロシアとアメリカの合同チームが1992年にこの事故を調査したと報告した。[ 118 ] [ 119 ] [ 120 ]
生物兵器施設(コンパウンド19)の真向かいにある陶磁器工場の夜勤労働者のほぼ全員が感染し、そのほとんどが死亡した。そのほとんどが男性だったため、NATO加盟国の一部はソ連が性別を特定した兵器を開発したのではないかと疑った。[ 121 ]政府は、炭疽菌に汚染された肉の消費が感染源であるとし、検査を受けていない肉が市内に入ってくると、そのすべてを没収するよう命じた。また、野良犬はすべて射殺し、人々は感染した動物との接触を禁じられた。さらに、18歳から55歳までの自主避難と炭疽菌ワクチン接種プログラムが実施された。[ 122 ]
隠蔽工作を裏付けるため、ソ連の医学・法学雑誌は、家畜の炭疽病の発生に関する記事を掲載した。この炭疽病は、感染した肉を摂取した人々に胃腸炭疽病を引き起こし、また、動物と接触した人々に皮膚炭疽病を引き起こした。すべての医療記録と公衆衛生記録はKGBによって押収された。[ 122 ]この発生は医学的問題を引き起こしただけでなく、西側諸国がソ連の秘密の生物兵器計画にさらに疑念を抱き、疑わしい場所の監視を強化するきっかけとなった。1986年、米国政府はこの事件の調査を許可され、軍事兵器施設から放出されたエアロゾル炭疽菌による曝露であると結論付けた。[ 123 ] 1992年、エリツィン大統領は、ソ連が1972年の生物兵器条約に違反したという「噂」が真実であると「確信している」と認めた。ソ連は、米国や英国と同様に、生物兵器計画に関する情報を国連に提出することに同意していたが、既知の施設については省略し、兵器計画を認めることはなかった。[ 121 ]
炭疽菌によるバイオテロ
理論的には、炭疽菌の胞子は最小限の特殊な設備と大学1年生の微生物学教育で培養できます。[ 124 ]生物兵器に適した大量の炭疽菌のエアロゾルを製造するには、広範な実践的知識、訓練、そして高度な設備が必要です。[ 125 ]
2001年に米国で起きた炭疽菌攻撃では、濃縮された炭疽菌胞子がバイオテロに使用され、胞子を詰めた郵便物が郵送された。 [ 126 ]郵便物は複数の報道機関と2人の民主党上院議員(サウスダコタ州のトム・ダシュル上院議員とバーモント州のパトリック・リーヒ上院議員)に送られた。その結果、22人が感染し、5人が死亡した。[ 37 ]これらの攻撃に使用された物質はわずか数グラムであり、2008年8月、米国司法省は米国政府に雇用されている上級バイオ防衛研究者のブルース・アイヴィンズが犯人であると考えていると発表した。[ 127 ]これらの事件はまた、多くの炭疽菌デマを生み出した。
これらの事件を受けて、米国郵政公社は主要な配送センターにバイオハザード検出システムを設置し、郵便物を通じて輸送される炭疽菌を積極的に検査するようになりました。[ 128 ] 2020年現在、これらのシステムによる陽性警報は発生していません。[ 129 ]
郵便物の除染
郵便炭疽菌攻撃といたずら事件を受けて、米国郵政公社はガンマ線照射とシプコ・インダストリーズ社が供給した独自の酵素製剤による処理により、一部の郵便物を滅菌しました。[ 130 ]
高校生が行った科学的実験は後に医療毒性学ジャーナルに掲載され、家庭用電気アイロンを最高温度(少なくとも400°F(204°C))で少なくとも5分間使用すると、一般的な郵便封筒内のすべての炭疽菌胞子を死滅させるはずであると示唆した。[ 131 ] [ 132 ]
その他の動物
炭疽病は主に牛、羊、山羊などの草食動物に感染しますが、幅広い哺乳類、鳥類、さらには人間も感染する可能性があります。感染は通常、汚染された土壌や植物に含まれる胞子を摂取することで起こります。宿主の体内に入ると、胞子は活性細菌に変化し、致死性の毒素を産生して重篤な症状を引き起こします。感染した動物は高熱、呼吸の速さ、痙攣を示すことが多く、数時間から数日以内に死亡する可能性があります。炭疽病の存在は、家畜管理や野生生物保護活動にとって大きな課題となる可能性があり、感染した動物や汚染された製品との接触を通じて人間に感染する可能性があるため、動物の健康と公衆衛生の両方にとって重要な懸念事項となっています。感染した動物はよろめき、呼吸困難、震えを起こし、最終的には数時間以内に倒れて死亡する可能性があります。[ 133 ]
炭疽病は犬や猫では特に稀で、2001年に米国で1件の症例が報告されています。[ 134 ]炭疽病の発生は、一部の野生動物の集団では定期的に発生します。[ 135 ]
ロシアの研究者たちは、北極圏の永久凍土には炭疽菌に感染したトナカイの死骸が約150万体存在し、胞子は永久凍土中で105年間生存する可能性があると推定しています。[ 136 ]北極圏の地球温暖化によって永久凍土が融解し、死骸から炭疽菌の胞子が放出されるリスクがあります。2016年には、熱波で解凍した75年前のトナカイの死骸が炭疽菌の発生源と関連付けられ、トナカイの炭疽菌感染症が発生しました。[ 137 ] [ 138 ]
参考文献
- ^ a b c d e f「症状」。CDC 。 2014年7月23日。2016年5月11日時点のオリジナルよりアーカイブ。2016年5月14日閲覧
- ^ a b c「炭疽菌に関する基本情報」CDC。2015年9月1日。2016年5月17日時点のオリジナルよりアーカイブ。 2016年5月14日閲覧。
- ^ a b c d「Who Is at Risk」 . CDC . 2015年9月1日. 2016年5月11日時点のオリジナルよりアーカイブ。2016年5月14日閲覧。
- ^ a b「診断」 . CDC . 2015年9月1日. 2016年5月11日時点のオリジナルよりアーカイブ。2016年5月14日閲覧。
- ^ a b c d e f g h i Hendricks KA, Wright ME, Shadomy SV, Bradley JS, Morrow MG, Pavia AT, et al. (2014年2月). 「成人における炭疽病の予防と治療に関する疾病管理予防センター専門家委員会会議」 . Emerging Infectious Diseases . 20 (2). doi : 10.3201/eid2002.130687 . PMC 3901462. PMID 24447897 .
- ^ a b「治療」 . CDC. 2016年1月14日. 2016年5月11日時点のオリジナルよりアーカイブ。2016年5月14日閲覧。
- ^ a b c d「炭疽菌」 FDA 2015年6月17日. 2016年5月7日時点のオリジナルよりアーカイブ。 2016年5月14日閲覧。
- ^ a b c炭疽菌:世界の状況ギデオン・インフォマティクス社 2016年 p.12. ISBN 978-1-4988-0861-3 2017年9月10日時点のオリジナルよりアーカイブ
- ^ a b c「炭疽菌の種類」 CDC 、 2024年7月21日。2016年5月11日時点のオリジナルよりアーカイブ。 2016年5月14日閲覧。
- ^ a b Mikesell P, Ivins BE, Ristroph JD, Vodkin MH, Dreier TM, Leppla SH (1983). 「プラスミド、パスツール、炭疽菌」 ASMニュース49 ( 7).
- ^ a b c d「感染経路」 CDC 、 2015年9月1日。2016年12月26日時点のオリジナルよりアーカイブ。 2016年5月14日閲覧。
- ^ a b c Turnbull P (2008).ヒトおよび動物における炭疽病(PDF) (第4版). ジュネーブ: 世界保健機関. pp. 20, 36. ISBN 978-92-4-154753-6 2016年11月30日時点のオリジナルよりアーカイブ(PDF)
- ^ Schlossberg D (2008).臨床感染症. ケンブリッジ大学出版局. p. 897. ISBN 978-1-139-57665-9 2017年9月10日時点のオリジナルよりアーカイブ
- ^ a b c d e「炭疽菌」。CDC 。国立新興・人獣共通感染症センター。2009年8月26日。2016年12月26日時点のオリジナルよりアーカイブ。2016年5月14日閲覧
- ^ Cherkasskiy BL (1999年8月). 「過去および現代の炭疽菌感染巣の国家登録簿」 . Journal of Applied Microbiology . 87 (2): 192– 95. doi : 10.1046/j.1365-2672.1999.00868.x . PMID 10475946. S2CID 6157235 .
- ^ ἄνθραξ .リデル、ヘンリー・ジョージ;スコット、ロバート;ペルセウス・プロジェクトのギリシャ語-英語辞典.
- ^ Harper D. 「炭疽菌」。オンライン語源辞典。
- ^ Breniquet C, Michel C (2014). 『古代近東の羊毛経済』 Oxbow Books. ISBN 978-1-78297-634-9 2016年8月27日時点のオリジナルよりアーカイブ– Googleブックス経由
- ^デ・トレヴィサ J (1398)。Bartholomaeus Anglicus の De Proprietatibus Rerum。
- ^ Stark J (2013). 『現代炭疽病の誕生 1875–1920:地域、国家、そして世界の疾病史の統合』ロンドン:ピカリング&チャット.
- ^ 「皮膚炭疽病」 CDC 、 2014年7月21日。2018年1月21日時点のオリジナルよりアーカイブ。 2018年2月16日閲覧。
- ^ 「炭疽菌に関するQ&A:兆候と症状」。緊急事態への備えと対応。米国疾病対策予防センター。2003年。2007年4月5日時点のオリジナルよりアーカイブ。 2007年4月19日閲覧。
- ^ Akbayram S, Doğan M, Akgün C, Peker E, Bektaş MS, Kaya A, et al. (2010). 「トルコ東部における皮膚炭疽病の小児における臨床所見」.小児皮膚科. 27 (6): 600–06 . doi : 10.1111/j.1525-1470.2010.01214.x . PMID 21083757. S2CID 37958515 .
- ^ a b c「スコットランドにおける薬物使用者間の炭疽菌感染症の発生、2009年12月から2010年12月まで」(PDF)。HPS 。国立炭疽菌感染症発生対策チームによる報告書。2011年12月。2013年10月20日時点のオリジナル(PDF)からアーカイブ。 2013年12月14日閲覧。
- ^ a b McNeil Jr DG (2010年1月12日). 「炭疽菌:スコットランドでヘロイン使用者6人が炭疽菌中毒で死亡」 .ニューヨーク・タイムズ. 2016年1月2日時点のオリジナルよりアーカイブ。
- ^ 「炭疽病 – 症状と原因」メイヨークリニック。2023年1月25日時点のオリジナルよりアーカイブ。 2023年1月25日閲覧。
- ^ “Injection Anthrax | Anthrax | CDC” . www.cdc.gov . 2019年1月28日. 2020年9月16日時点のオリジナルよりアーカイブ。 2020年9月16日閲覧。
- ^ a b c d e f g h炭疽菌 – 第4章 – 2020年イエローブック | トラベラーズヘルス。CDC。2020年6月6日時点のオリジナルよりアーカイブ。 2020年3月14日閲覧。
- ^ USAMRIID (2011). USAMRIID 生物学的傷害の医療管理ハンドブック(PDF) (第7版).米国政府印刷局. ISBN 978-0-16-090015-02015年2月9日時点のオリジナル(PDF)からのアーカイブ。
2001年の攻撃ではCFRはわずか45%でしたが、それ以前のIAのCFRは85%を超えていました(37ページ)。
- ^ 「消化管炭疽病」 .米国疾病予防管理センター. 2013年8月23日. 2015年2月11日時点のオリジナルよりアーカイブ。 2015年2月10日閲覧。
- ^ Frankel AE, Kuo SR, Dostal D, Watson L, Duesbery NS, Cheng CP, et al. (2009年1月). 「炭疽病の病態生理学」 . Frontiers in Bioscience . 14 (12): 4516–24 . doi : 10.2741 / 3544 . PMC 4109055. PMID 19273366 .
- ^ Koehler TM (2009年12月). 「炭疽菌の生理学と遺伝学」 . Molecular Aspects of Medicine . 30 (6): 386– 396. doi : 10.1016/j.mam.2009.07.004 . PMC 2784286. PMID 19654018 .
- ^ a bコッホ R (1876)。「Untersuhungen über Bakterien: V. Die Ätiologie der Milzbrand-Krankheit, begründet auf die Entwicklungsgeschichte des Bacillus anthracis 」 [細菌の研究: V. 炭疽菌の個体発生に基づく炭疽病の病因[Cohns]] (PDF)。Beiträge zur Biologie der Pflanzen。2 (2): 277–310。2011年 7月18 日のオリジナルからアーカイブ(PDF) 。
- ^ Hughes R, May AJ, Widdicombe JG (1956年8月). 「炭疽病の病因におけるリンパ系の役割」 . British Journal of Experimental Pathology . 37 (4): 343–49 . PMC 2082573. PMID 13364144 .
- ^ Liu H, Bergman NH, Thomason B, Shallom S, Hazen A, Crossno J, et al. (2004年1月). 「炭疽菌胞子の形成と組成」 . Journal of Bacteriology . 186 (1): 164– 78. Bibcode : 2004JBact.186..164L . doi : 10.1128/JB.186.1.164-178.2004 . PMC 303457. PMID 14679236 .
- ^ 「消毒、除染、燻蒸、焼却」『ヒトと動物の炭疽病』 (第4版)、世界保健機関、2008年、 2025年3月5日閲覧。
- ^ a b c d Pimental RA, Christensen KA, Krantz BA, Collier RJ (2004年9月). 「炭疽菌毒素複合体:7量体防御抗原は致死因子と浮腫因子に同時に結合できる」.生化学および生物理学的研究通信. 322 (1): 258–62 . Bibcode : 2004BBRC..322..258P . doi : 10.1016/j.bbrc.2004.07.105 . PMID 15313199 .
- ^ Sweeney DA, Hicks CW, Cui X, Li Y, Eichacker PQ (2011年12月). 「炭疽菌感染症」 . American Journal of Respiratory and Critical Care Medicine . 184 (12): 1333–41 . doi : 10.1164/rccm.201102-0209CI . PMC 3361358. PMID 21852539 .
- ^ a b Metcalfe N (2004年10月). 「羊毛選別者病の歴史:ヨークシャーの始まりは国際的な未来か?」.職業医学. 54 (7): 489–93 . doi : 10.1093/occmed/kqh115 . PMID 15486181 .
- ^ Bloomfield R (2012年4月12日). 「現場で人骨が発見され、クロスレール工事が停止」イブニング・スタンダード. 2023年10月25日時点のオリジナルよりアーカイブ。 2023年11月2日閲覧。
- ^ Hudson JA, Daniel RM, Morgan HW (1989年8月). 「地熱加熱された南極土壌由来の好酸性および好熱性バチルス菌株」 . FEMS Microbiology Letters . 60 (3): 279–82 . doi : 10.1111/j.1574-6968.1989.tb03486.x .
- ^ Guillemin J (1999).炭疽菌:致死的なアウトブレイクの調査. インターネットアーカイブ. バークレー:カリフォルニア大学出版局. ISBN 978-0-520-22204-5。
{{cite book}}: CS1 maint: 発行者の所在地 (リンク) - ^ a b Luhn A (2016年8月8日). 「気候変動で炭疽菌に感染したトナカイが解凍され、シベリアの子供が死亡」 . Wired . ISSN 1059-1028 . 2016年8月17日時点のオリジナルよりアーカイブ。2023年11月2日閲覧
- ^ a b c「ヒトにおける炭疽菌」、『ヒトと動物における炭疽菌』(第4版)、世界保健機関、2008年、2022年6月18日時点のオリジナルよりアーカイブ、2023年11月2日閲覧。
- ^ 「ウェルダー炭疽病について」米国疾病予防管理センター(CDC)2025年12月18日。 2026年1月5日閲覧。
- ^ a b Chambers J, Yarrarapu SN, Mathai JK (2023). 「炭疽菌感染症」 . StatPearls . Treasure Island (FL): StatPearls Publishing. PM ID 30571000. 2022年4月28日時点のオリジナルよりアーカイブ。 2023年11月2日閲覧。
- ^ Gao M (2006年4月27日). 「炭疽菌中毒の分子的根拠」イリノイ大学アーバナ・シャンペーン校. 2016年12月26日時点のオリジナルよりアーカイブ。 2016年12月26日閲覧。
- ^ Chvyrkova I, Zhang XC, Terzyan S (2007年8月). 「炭疽菌毒素の致死因子は防御抗原のモノマーに結合する」 .生化学および生物理学的研究通信. 360 (3): 690–95 . Bibcode : 2007BBRC..360..690C . doi : 10.1016/j.bbrc.2007.06.124 . PMC 1986636. PMID 17617379 .
- ^ Levinson W (2010).医学微生物学および免疫学レビュー(第11版).
- ^ Forbes BA (2002). Bailey & Scott's Diagnostic Microbiology (第11版).
- ^ a b c「安全と健康に関するトピック | 炭疽菌 – 管理と予防 | 労働安全衛生局」www.osha.gov。2019年12月22日時点のオリジナルよりアーカイブ。2019年12月22日閲覧。
- ^ 「人工呼吸器」国立個人防護技術研究所、国立労働安全衛生研究所。2009年4月30日。 2017年7月31日時点のオリジナルよりアーカイブ。
- ^世界保健機関、国連食糧農業機関、世界獣疫事務局(2019年)。「多部門一体のワンヘルスアプローチ:各国における人獣共通感染症対策のための三者ガイド」 IRIS、ISBN 978-92-4-151493-4 2023年10月14日時点のオリジナルよりアーカイブ。2023年10月8日閲覧
- ^ Cohn DV (1996年2月11日). 「ルイ・パスツールの生涯と時代」ルイビル大学歯学部. 2008年4月8日時点のオリジナルよりアーカイブ。 2008年8月13日閲覧。
- ^ Mikesell P, Ivins BE, Ristroph JD, Vodkin MH, Dreier TM, Leppla SH (1983). 「プラスミド、パスツール、炭疽菌」(PDF) . ASM News . 49 : 320–22 . 2017年8月8日時点のオリジナル(PDF)からアーカイブ。 2017年6月8日閲覧。
- ^ “Robert Koch (1843–1910)” . About.com ドイツ語. About.com. 2008年7月5日時点のオリジナルよりアーカイブ。 2008年8月13日閲覧。
- ^ Joellenbeck LM、Zwanziger LL、Durch JS、Strom BL他(米国医学研究所炭疽菌ワクチンの安全性と有効性評価委員会)(2002年)「エグゼクティブサマリー」炭疽菌ワクチン:安全か?効果はあるか?米国国立科学アカデミー出版局(米国) 。 2024年5月19日閲覧。
- ^ Splino M, Patocka J , Prymula R, Chlibek R (2005). 「炭疽菌ワクチン」 . Annals of Saudi Medicine . 25 (2): 143– 149. doi : 10.5144/0256-4947.2005.143 . PMC 6147967. PMID 15977694 .
- ^ 「2008年12月11日付承認書」。食品医薬品局。2017年6月29日時点のオリジナルよりアーカイブ。2017年6月8日閲覧。
- ^ “炭疽菌感染症予防ワクチン | CDC” . www.cdc.gov . 2020年11月18日. 2023年1月25日時点のオリジナルよりアーカイブ。 2023年1月25日閲覧。
- ^ a b Schrader E (2003年12月23日). 「軍、炭疽菌ワクチン接種を中止へ」ロサンゼルス・タイムズ. 2016年12月26日時点のオリジナルよりアーカイブ。2016年12月26日閲覧。
- ^ “How People Are Infected | Anthrax | CDC” . www.cdc.gov . 2019年1月9日. 2016年12月26日時点のオリジナルよりアーカイブ。 2020年9月16日閲覧。
- ^ 「対応活動中にどのように除染すべきか?」米国労働安全衛生局。2016年12月26日時点のオリジナルよりアーカイブ。 2016年12月26日閲覧。
- ^ 「CDC炭疽菌Q&A:治療」 。 2011年5月5日時点のオリジナルよりアーカイブ。2011年4月4日閲覧。
- ^ Doganay M, Dinc G, Kutmanova A, Baillie L (2023年3月). 「ヒト炭疽病:診断と治療の最新情報」 .診断. 13 (6): 1056. doi : 10.3390/diagnostics13061056 . PMC 10046981. PMID 36980364 .
- ^ 「HGSI、炭疽菌治療薬ABthraxのFDA承認を要求」 Forbes.AP通信. 2009年5月21日. 2014年10月18日時点のオリジナルよりアーカイブ。
- ^ 「FDA、吸入炭疽病の治療薬としてラキシバクマブを承認」食品医薬品局. 2012年12月17日時点のオリジナルよりアーカイブ。 2012年12月14日閲覧。
- ^ニュースリリース(2016年3月21日)「FDA、吸入炭疽病の新たな治療法を承認」 FDA。 2016年3月24日時点のオリジナルよりアーカイブ。
- ^ 「炭疽菌免疫グロブリン(静脈内投与) - 副作用と用途」メイヨークリニック。 2026年1月13日閲覧。
- ^ 「アントラシルの処方情報」(PDF)
- ^ Legler PM, Little SF, Senft J, Schokman R, Carra JH, Compton JR, et al. (2021年12月). 「ペグ化環状置換カプセル脱重合酵素による実験的炭疽菌の治療」. Science Translational Medicine . 13 (623) eabh1682. doi : 10.1126/scitranslmed.abh1682 . PMID 34878819 .
- ^ YouTubeで抗生物質耐性炭疽菌に対する人工酵素を公開
- ^ a b Hu X, Legler PM, Khavrutskii I, Scorpio A, Compton JR, Robertson KL, et al. (2012年2月). 「γ-グルタミルトランスペプチダーゼのドナー基質およびアクセプター基質特異性の探究」.生化学. 51 (6): 1199– 1212. doi : 10.1021/bi200987b . PMID 22257032 .
- ^ Wu R, Richter S, Zhang RG, Anderson VJ, Missiakas D, Joachimiak A (2009年9月). 「炭疽菌トランスペプチダーゼ酵素CapDの結晶構造」 . The Journal of Biological Chemistry . 284 (36): 24406– 24414. doi : 10.1074/jbc.M109.019034 . PMC 2782033. PMID 19535342 .
- ^ Holty JE, Bravata DM, Liu H, Olshen RA, McDonald KM, Owens DK (2006年2月). 「系統的レビュー:1900年から2005年までの1世紀にわたる吸入炭疽病症例」Annals of Internal Medicine . 144 (4): 270–80 . doi : 10.7326/0003-4819-144-4-200602210-00009 . PMID 16490913 . S2CID 8357318 .
- ^ a b “Types of Anthrax | CDC” . www.cdc.gov . 2020年11月19日. 2016年5月11日時点のオリジナルよりアーカイブ。 2023年1月25日閲覧。
- ^ Holty JE, Bravata DM, Liu H, Olshen RA, McDonald KM, Owens DK (2006年2月). 「系統的レビュー:1900年から2005年までの1世紀にわたる吸入炭疽病症例」Annals of Internal Medicine . 144 (4): 270–80 . doi : 10.7326/0003-4819-144-4-200602210-00009 . PMID 16490913 . S2CID 8357318 .
- ^ Lanska DJ (2002年8月). 「炭疽菌性髄膜脳炎」.神経学. 59 (3): 327–34 . doi : 10.1212/wnl.59.3.327 . PMID 12177364. S2CID 37545366 .
- ^ Suffin SC, Carnes WH, Kaufmann AF (1978年9月). 「家庭で作業する職人における吸入炭疽病」. Human Pathology . 9 (5): 594–97 . doi : 10.1016/S0046-8177(78)80140-3 . PMID 101438 .
- ^ Schweitzer S (2010年1月4日). 「ドラマーの炭疽菌事件が公衆衛生上の追及を促す」 .ボストン・グローブ. 2013年12月14日時点のオリジナルよりアーカイブ。 2014年10月19日閲覧。
- ^ 「PROMED: 炭疽菌、ヒト – 米国: (ニューハンプシャー州)」 Promedmail.org、2009年12月26日。2011年9月27日時点のオリジナルよりアーカイブ。 2014年3月17日閲覧。
- ^ 「PROMED: 炭疽菌、ヒト – 米国: (ニューハンプシャー州)」 Promedmail.org、2010年4月18日。2011年9月27日時点のオリジナルよりアーカイブ。 2014年3月17日閲覧。
- ^ Kaplan T (2007年9月6日). 「コネチカット州在住者2名から炭疽菌が発見、うち1名はドラマー」 . The New York Times . 2020年11月24日時点のオリジナルよりアーカイブ。 2020年5月16日閲覧。
- ^ Mole B (2026年1月2日). 「健康な18歳の溶接工が炭疽菌で瀕死の重傷—9例目の不可解な症例」 . Arstechnica . Condé Nast . 2026年1月3日閲覧。
- ^ de Perio MA, Hendricks KA, Dowell CH, Bower WA, Burton NC, Dawson P, et al. (2022年3月26日). 「溶接工炭疽:職業病のレビュー」 . Pathogens . 11 ( 4). MDPI: 402. doi : 10.3390/pathogens11040402 . PMC 9029013. PMID 35456077 .
- ^ 「クロアチア:自然公園の死んだ牛から炭疽菌が見つかる」ワシントン・ポスト、AP通信。2022年7月16日。2022年7月22日時点のオリジナルよりアーカイブ。 2022年7月19日閲覧。
- ^ 「炭疽菌を吸い込んだ男性が死亡」 BBCニュース、2008年11月2日。2016年3月7日時点のオリジナルよりアーカイブ。
- ^ Madigan M, Martinko J編 (2005). Brock Biology of Microorganisms (第11版). Prentice Hall. ISBN 978-0-13-144329-7。
- ^ 「1905年のノーベル生理学・医学賞」。ノーベル賞。ノーベル財団。2020年5月23日時点のオリジナルよりアーカイブ。2021年10月4日閲覧
- ^ 「ジョン・ヘンリー・ベル医学博士、MRCS」 .ブリティッシュ・メディカル・ジャーナル. 2 (2386): 735–36 . 1906年9月22日. doi : 10.1136/bmj.2.2386.735 . PMC 2382239 .
- ^ 「炭疽菌による産業感染」英国医学雑誌2 ( 2759):1338.1913年11月15日.PMC2346352 .
- ^ Jones S (2010). 「小さな包みの中の死:炭疽菌の小史」ボルチモア:ジョンズ・ホプキンス大学出版局.
- ^ Decker J (2003). 『致死的な病気と伝染病、炭疽菌』 Chelesa House Publishers. pp. 27–28 . ISBN 978-0-7910-7302-5。
- ^ガイソン・G (2014).ルイ・パスツールの私的科学. プリンストン大学出版局
- ^ Stark J (2012). 「炭疽菌とオーストラリアの世界的文脈:1850~1920年頃のイギリスおよびフランスとの理論と実践の国際交流」『健康と歴史』14 (2): 1– 25. doi : 10.5401/healthhist.14.2.0001 . S2CID 142036883 .
- ^ 「炭疽菌と炭疽菌ワクチン - ワクチン予防可能な疾患の疫学と予防」。国家予防接種プログラム。米国疾病予防管理センター。2006年1月。 2012年8月24日時点のオリジナルよりアーカイブ。
- ^ Willman D (2007年7月1日). 「バイオテロの脅威を売り込む」ロサンゼルス・タイムズ.
- ^ Jacobsen A (2015). 『ペンタゴンの頭脳:アメリカの最高機密軍事研究機関DARPAの無修正の歴史』ニューヨーク:リトル・ブラウン・アンド・カンパニー293頁.
- ^ Shane S (2001年12月23日). 「陸軍、炭疽菌の増殖を促すために被害者の血液を採取」 . Boston Sun. UCLA疫学部サイト. 2009年12月29日時点のオリジナルよりアーカイブ。 2009年8月6日閲覧。
- ^ 「炭疽菌駆除剤として最もよく知られるサンディア国立研究所の除染製剤が、家庭内のカビにも効果を発揮」 2007年4月26日。 2008年9月5日時点のオリジナルよりアーカイブ。 2008年8月13日閲覧。
- ^ a b Wang X (2015年5月12日). 「キャピトル・ヒルの炭疽菌除去」(PDF) . EPA同窓会. 2018年9月30日時点のオリジナル(PDF)からアーカイブ。
- ^ 「屋内および屋外環境の改善」 。 2013年10月13日時点のオリジナルよりアーカイブ。2013年10月10日閲覧。
- ^ Wood JP, Adrion AC (2019年4月). 「建材や屋外資材に付着した炭疽菌およびその他の胞子形成細菌の不活化のための除染技術のレビュー」 .環境科学技術. 53 (8): 4045–62 . Bibcode : 2019EnST...53.4045W . doi : 10.1021/acs.est.8b05274 . PMC 6547374. PMID 30901213 .
- ^ 「漂白剤を用いた炭疽菌などの微生物の駆除」応用微生物学会。2008年5月17日時点のオリジナルよりアーカイブ。 2008年8月13日閲覧。
- ^ Rastogi VK, Ryan SP, Wallace L, Smith LS, Shah SS, Martin GB (2010年5月). 「炭疽菌胞子で汚染された建物内壁の除染における二酸化塩素の有効性の体系的評価」 .応用環境微生物学. 76 (10): 3343–3e51. Bibcode : 2010ApEnM..76.3343R . doi : 10.1128/AEM.02668-09 . PMC 2869126. PMID 20305025 .
- ^ a b「農薬廃棄が環境に優しく」サイエンスニュース。2011年6月29日時点のオリジナルよりアーカイブ。2009年6月8日閲覧。
- ^ Wessner D, Dupont C, Charles T, Neufeld J (2020年12月3日). Microbiology . John Wiley & Sons. ISBN 978-1-119-59249-5。
- ^ Broad WJ (2002年3月1日). 「炭疽菌専門家、感染死体の焼却で罰金刑に」 .ニューヨーク・タイムズ. 2016年12月26日時点のオリジナルよりアーカイブ。2016年12月26日閲覧
- ^ 「英国の『炭疽菌島』「 . BBCニュース. 2001年7月25日. 2016年12月26日時点のオリジナルよりアーカイブ。 2016年12月26日閲覧。
- ^ Bisher J (2003年8月). 「フィンランドにおける炭疽菌破壊工作、あるいはフォン・ローゼン男爵の砂糖でコーティングされた炭疽菌兵器」 .軍事史. pp. 17– 22. 2017年3月24日時点のオリジナルよりアーカイブ
。第一次世界大戦中、テロリストはフィンランド独立のために炭疽菌の使用を企てた
- ^ 「DOD技術情報」(PDF)。2023年10月31日時点のオリジナルよりアーカイブ(PDF) 。 2023年10月31日閲覧。
- ^コールLA (1990).秘密の雲:人口密集地域における陸軍の細菌戦実験. ロウマン・アンド・リトルフィールド. ISBN 978-0-8226-3001-2。
- ^ロバートソン・D. 「サダムの細菌戦争計画は、オックスフォードの牛1頭にまで遡る」タイムズ紙。2005年12月25日時点のオリジナルよりアーカイブ
- ^「英国は炭疽菌でドイツを全滅させる計画を立てた」サンデー・ヘラルド、グラスゴー、2001年10月14日。
- ^ Croddy EA、Wirtz JJ編 (2005).大量破壊兵器:世界的な政策、技術、歴史に関する百科事典ABC-CLIO. p. 21. ISBN 978-1-85109-490-5 2017年2月22日時点のオリジナルよりアーカイブ
- ^ Martin D (2001年11月16日). 「伝統医療従事者、国際的認知を求める」 . Southern African News Features . 2013年5月11日時点のオリジナルよりアーカイブ。 2014年10月19日閲覧。
- ^ Pala C (2003年3月22日). 「炭疽菌は永久に埋葬された」 .ワシントン・タイムズ. 2021年5月17日時点のオリジナルよりアーカイブ。 2020年8月26日閲覧。
- ^ a b Guillemin J (2000). 「炭疽菌:致死的なアウトブレイクの調査」 . New England Journal of Medicine . 343 (16). カリフォルニア大学出版局: 275–77 . doi : 10.1056/NEJM200010193431615 . ISBN 978-0-520-22917-4. PMID 11041763.
- ^ 「ペスト戦争:1979年の炭疽菌漏洩」 .フロントライン. PBS. 2008年9月17日時点のオリジナルよりアーカイブ。2008年8月13日閲覧
- ^ Fishbein MC. 「炭疽菌 - ロシアより愛をこめて」 .感染症:原因、種類、予防、治療、そして事実. MedicineNet.com. 2008年10月24日時点のオリジナルよりアーカイブ。 2008年8月13日閲覧。
- ^ a bアリベック K (1999)。バイオハザード。ニューヨーク:デルタ出版。ISBN 978-0-385-33496-9。
- ^ a b Meselson M, Guillemin J, Hugh-Jones M, Langmuir A, Popova I, Shelokov A, et al. (1994年11月). 「1979年のスベルドロフスク炭疽菌アウトブレイク」. Science . 266 ( 5188): 1202–08 . Bibcode : 1994Sci...266.1202M . doi : 10.1126/science.7973702 . PMID 7973702
- ^ Sternbach G (2003年5月). 「炭疽菌の歴史」. The Journal of Emergency Medicine . 24 (4): 463–67 . doi : 10.1016/S0736-4679(03)00079-9 . PMID 12745053 .
- ^ Barney J (2012年10月17日). 「バージニア大学の研究者、土壌で炭疽菌が増殖・繁殖できると発見」バージニア大学保健システム. バージニア大学のサイト. 2012年10月21日時点のオリジナルよりアーカイブ。 2013年10月1日閲覧。
- ^ 「炭疽菌は生物兵器として」 BBCニュース、2001年10月10日。2016年5月5日時点のオリジナルよりアーカイブ。 2016年4月16日閲覧。
- ^ Cole LA (2009). 『炭疽菌からの手紙:バイオテロ専門家がアメリカを震撼させた攻撃を調査 ― 事件は終結したのか?』SkyhorsePublishing. ISBN 978-1-60239-715-6。
- ^ Bohn K (2008年8月6日). 「米国当局、研究者が炭疽菌殺人犯であると宣言」 CNN. 2008年8月8日時点のオリジナルよりアーカイブ。2008年8月7日閲覧
- ^ 「セフェイド社とノースロップ・グラマン社、炭疽菌検査カートリッジの購入で合意」。セキュリティ製品。2007年8月16日。2011年7月16日時点のオリジナルよりアーカイブ。 2009年3月26日閲覧。
- ^ 「USPS BDS FAQ」(PDF)。2022年10月9日時点のオリジナルよりアーカイブ(PDF) 。
- ^ 「Latest Facts Update」 USPS、2002年2月12日。2009年5月9日時点のオリジナルよりアーカイブ。 2008年8月13日閲覧。
- ^ Roberge MR (2006年6月). 「郵便で届いたバチルス胞子:炭疽菌問題の解決」 . Journal of Medical Toxicology . 2 (2): 64– 67. doi : 10.1007/BF03161173 . ISSN 1556-9039 . PMC 3550055. PMID 18072116 .
- ^ 「17歳の青年が炭疽菌不活性化剤を開発」 NBCニュース、2006年2月23日。2014年10月7日時点のオリジナルよりアーカイブ。
- ^ 「炭疽菌 | FAQs」 . テキサス州DSHS. 2023年10月25日時点のオリジナルよりアーカイブ。 2023年10月19日閲覧。
- ^ 「犬は炭疽菌に感染するのか?」Canine Nation . 2001年10月30日. 2012年4月6日時点のオリジナルよりアーカイブ。2007年2月17日閲覧。
- ^ Dragon DC, Elkin BT, Nishi JS, Ellsworth TR (1999年8月). 「カナダにおける炭疽病のレビューと北部バイソンにおけるこの疾患研究への示唆」 . Journal of Applied Microbiology . 87 (2): 208–13 . doi : 10.1046/j.1365-2672.1999.00872.x . PMID 10475950 .
- ^ Revich BA, Podolnaya MA (2011). 「永久凍土の融解は東シベリアの歴史的な牛の埋葬地を混乱させる可能性がある」 . Global Health Action . 4 : 8482. doi : 10.3402/gha.v4i0.8482 . PMC 3222928. PMID 22114567 .
- ^ 「ヤマルで炭疽菌感染症が流行し40人が入院、半数以上が子供」。2016年7月30日時点のオリジナルよりアーカイブ。
- ^ Luhn A (2016年8月8日). 「気候変動で炭疽菌に感染したトナカイが凍りつき、シベリアの子供が死亡」 Wired. 2016年8月17日時点のオリジナルよりアーカイブ。 2016年8月19日閲覧。
さらに詳しい情報
- ヒトと動物における炭疽病(PDF)(第4版)。ジュネーブ:世界保健機関。2008年。ISBN 978-92-4-154753-6 2016年11月30日時点のオリジナル(PDF)からのアーカイブ
- 「ミミズと炭疽菌」サイエンティフィック・アメリカン誌、57号、1881年7月23日。