生体医学工学
_01.JPG/440px-Операционная._ФЦН_(Тюмень)_01.JPG)

生物医学工学(BME)または医療工学は、工学原理と設計概念を医療分野(診断や治療など)の医学および生物学に応用する分野です。BMEはまた、診断、モニタリング、治療など、医療処置の進歩のために論理科学を統合します。[ 1 ] [ 2 ]また、生物医学エンジニアの業務範囲には、病院における既存の医療機器の管理(関連する業界標準を遵守しながら)も含まれます。これには、調達、定期検査、予防保守、機器の推奨作成などが含まれており、生物医学機器技術者(BMET)または臨床エンジニアとしても知られています。
バイオメディカル工学は、他の多くの工学分野と比較して、最近、独自の分野として浮上しました。[ 3 ]このような進化は、新しい分野が、既存の分野間の学際的な専門分野からそれ自体が1つの分野と見なされるように移行するときに一般的です。バイオメディカル工学の仕事の多くは、幅広いサブフィールド(以下を参照)にまたがる研究開発で構成されています。バイオメディカル工学の著名な応用には、生体適合性プロテーゼ、臨床機器からマイクロインプラントに至るさまざまな診断および治療用医療機器、 MRIやEKG / ECGなどの画像技術、再生組織の成長、バイオ医薬品を含む医薬品の開発などがあります。
サブフィールドと関連フィールド
バイオインフォマティクス

バイオインフォマティクスは、生物学的データを理解するための手法とソフトウェアツールを開発する学際的な分野です。学際的な科学分野であるバイオインフォマティクスは、コンピュータサイエンス、統計学、数学、工学を融合し、生物学的データを分析・解釈します。
バイオインフォマティクスは、コンピュータプログラミングを方法論の一部として用いる生物学研究全般を指す包括的な用語であると同時に、特にゲノミクス分野において繰り返し用いられる特定の解析「パイプライン」を指す用語としても捉えられています。バイオインフォマティクスの一般的な用途には、候補遺伝子およびヌクレオチド(SNP)の同定が含まれます。多くの場合、こうした同定は、疾患の遺伝的基盤、固有の適応、望ましい特性(特に農業用種)、あるいは集団間の差異をより深く理解することを目的として行われます。より形式張らない形では、バイオインフォマティクスは核酸やタンパク質の配列における組織原理の理解も試みます。
バイオメカニクス
.jpg/440px-B09685P005_(1).jpg)
バイオメカニクスは、生物全体から臓器、細胞、細胞小器官に至るまで、あらゆるレベルの生物システムの機械的側面の構造と機能を、力学の手法を用いて研究する学問です。[ 4 ] [ 5 ]
生体材料
生体材料とは、生体システムと相互作用する物質、表面、または構造を指します。科学分野としての生体材料は約50年前に誕生しました。生体材料の研究は、生体材料科学または生体材料工学と呼ばれています。この分野は、その歴史を通して着実かつ力強い成長を遂げており、多くの企業が新製品開発に多額の資金を投資しています。生体材料科学は、医学、生物学、化学、組織工学、材料科学の要素を包含しています。
生物医学光学
生物医学光学は、物理学、工学、生物学の原理を組み合わせて、生物組織と光の相互作用、およびこれをセンシング、イメージング、および治療にどのように利用できるかを研究します。[ 6 ]光学イメージング、顕微鏡検査、眼底検査、分光法、および治療を含む幅広い用途があります。生物医学光学の技術とテクノロジーの例には、光干渉断層撮影(OCT)、蛍光顕微鏡検査、共焦点顕微鏡検査、および光線力学療法(PDT) が含まれます。たとえば、OCT は光を使用して、目の網膜や心臓の冠動脈などの内部構造の高解像度の 3 次元画像を作成します。蛍光顕微鏡検査では、特定の分子を蛍光色素で標識し、光を使用して可視化することで、生物学的プロセスと疾患のメカニズムに関する洞察が得られます。最近では、補償光学が生物組織の収差を補正することでイメージングを支援し、レーザー手術や網膜イメージングなどの手順でより高解像度のイメージングと精度の向上を可能にしています。
組織工学
組織工学は、遺伝子工学(下記参照)と同様に、バイオテクノロジーの主要分野であり、BME とかなり重複しています。
組織工学の目標の一つは、臓器移植を必要とする患者のために、腎臓や肝臓などの人工臓器(生物学的材料を用いて)を作製することです。生物医学エンジニアは現在、そのような臓器の作製方法を研究しています。研究者たちは、この目的に向けて、ヒト幹細胞から強固な顎骨[ 7 ]や気管[ 8 ]を作製しました。また、いくつかの人工膀胱が実験室で作製され、ヒト患者への移植に成功しています。[ 9 ]合成成分と生物学的成分の両方を使用するバイオ人工臓器も、人工バイオリアクター構造内で肝細胞を使用する肝臓補助装置など、研究の焦点となっています。[ 10 ]

遺伝子工学
遺伝子工学、組み換えDNA技術、遺伝子改変・操作(GM)、遺伝子スプライシングは、生物の遺伝子を直接操作する技術を指す用語です。遺伝子操作の間接的な方法である従来の育種とは異なり、遺伝子工学では分子クローニングや形質転換といった最新の技術を用いて、標的遺伝子の構造と特性を直接改変します。遺伝子工学技術は、数多くの応用分野で成功を収めています。例えば、作物栽培技術の改善(医療分野への応用ではありませんが、生物システム工学の項を参照)、改変細菌を用いた合成ヒトインスリンの製造、ハムスター卵巣細胞におけるエリスロポエチンの製造、そして研究用オンコマウス(がんマウス)などの新しいタイプの実験用マウスの作製などが挙げられます。
神経工学
神経工学(ニューロエンジニアリングとも呼ばれる)は、工学技術を用いて神経系を理解、修復、置換、または強化する分野です。神経エンジニアは、生体神経組織と非生体構造の境界面における設計上の問題を解決する上で、独自の能力を備えています。神経工学は、将来の義肢開発を含む、様々な分野に貢献することができます。例えば、認知神経義肢(CNP)は精力的に研究されており、義肢装着者に補助装置を操作するための信号を送るためのチップインプラントを可能にするでしょう。[ 11 ]
製薬工学
製薬工学は、薬物工学、新規薬物送達とターゲティング、製剤技術、化学工学の単位操作、そして製剤分析を含む学際的な科学です。より良い医療を提供するために化学物質に関する技術を活用することに重点を置いているため、 薬学の一部とみなされることもあります。
病院および医療機器

これは非常に広範なカテゴリであり、基本的には、主に化学的手段(医薬品など)または生物学的手段(ワクチンなど)によって意図された結果を達成せず、代謝を伴わないすべてのヘルスケア製品が対象となります。
医療機器は、以下の用途での使用を目的としています。
- 病気やその他の症状の診断
- 病気の治癒、緩和、治療、または予防において。
例としては、ペースメーカー、輸液ポンプ、人工心肺、透析装置、人工臓器、インプラント、義肢、矯正レンズ、人工内耳、眼球補綴、顔面補綴、身体補綴、歯科インプラントなどが挙げられます。
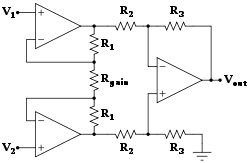
光造形法は、医療用モデリングが物理的な物体を作成するために用いられている実例です。臓器や人体のモデリングに加え、新興工学技術は現在、革新的な治療法[ 12 ]、[ 13 ] 、複雑な疾患の患者モニタリング[ 14 ]のための新しいデバイスの研究開発にも利用されています。
医療機器は、米国では次のように規制および分類されています(規制も参照)。
- クラスIの機器は、使用者への危害の可能性が最小限であり、クラスIIまたはクラスIIIの機器よりも設計が簡素化されていることが多いです。このカテゴリの機器には、舌圧子、便器、弾性包帯、検査用手袋、手持ち式手術器具、その他類似の一般的な機器が含まれます。
- クラスII機器は、クラスI機器の一般的な管理に加えて、特別な管理の対象となります。特別な管理には、特別なラベル表示要件、必須の性能基準、市販後調査などが含まれる場合があります。このクラスの機器は通常、非侵襲性であり、X線装置、PACS(画像通信システム)、電動車椅子、輸液ポンプ、手術用ドレープなどが含まれます。
- クラス III の機器では通常、クラス I の一般的な管理に加えて、機器の安全性と有効性を確認するための科学的レビューである市販前承認 (PMA) または市販前通知 (510k) が必要です。例としては、人工心臓弁、股関節および膝関節インプラント、シリコンゲル充填乳房インプラント、インプラント小脳刺激装置、インプラント型ペースメーカーパルス発生器、骨内インプラントなどがあります。
医療画像
医療/生物医学イメージングは、医療機器の主要な分野です。この分野では、臨床医が直接的または間接的に、(大きさや位置などにより)目に見えないものを「見る」ことを可能にします。これには、超音波、磁気、紫外線、放射線などの手段が用いられます。
一方、ナビゲーションガイド付き機器は、脳へのカテーテル留置や栄養チューブ留置システムなどにおいて、電磁気追跡技術を活用しています。例えば、ENvizion Medical社のENvueは、経腸栄養チューブ留置用の電磁ナビゲーションシステムです。このシステムは、外部磁場発生器と複数の電磁受動センサーを使用することで、患者の体型に合わせて画面を拡大縮小し、栄養チューブの先端の位置と方向をリアルタイムで表示します。これにより、医療スタッフは消化管内での正しい留置を確実に行うことができます。[ 15 ]

画像診断技術は医療診断に不可欠な場合が多く、通常は病院にある最も複雑な機器であり、これには透視検査、磁気共鳴画像法(MRI)、核医学、陽電子放出断層撮影(PET)、PET-CT スキャン、 X 線やCT スキャンなどの投影放射線撮影、断層撮影、超音波、光学顕微鏡、電子顕微鏡が含まれます。
医療用インプラント
インプラントは、失われた生物学的構造を置き換え、その機能を果たすために作られた医療機器の一種です(移植とは、生体組織の移植を指します)。インプラントの体と接触する表面は、最も機能性が高いものに応じて、チタン、シリコン、アパタイトなどの生体材料で作られています。人工ペースメーカーや人工内耳のように、インプラントには電子機器が組み込まれている場合もあります。皮下薬物送達デバイス(埋め込み型錠剤や薬剤溶出ステントなど)のように、生体活性インプラントもあります。


バイオニクス
人工の身体部位の置換は、バイオニクスの多くの応用分野の一つです。人体システムの特性と機能に関する複雑かつ徹底的な研究に着目するバイオニクスは、いくつかの工学的問題の解決に応用することができます。目、耳、その他の器官の様々な機能とプロセスを綿密に研究することで、カメラ、テレビ、無線送信機と受信機、その他多くの機器の改良への道が開かれました。
生体医療センサー
近年、マイクロ波技術をベースとしたバイオメディカルセンサーが注目を集めています。病状の診断とモニタリングの両方において、特定の用途向けに様々なセンサーを製造できます。例えば、マイクロ波センサーは、下肢外傷のモニタリングにおいて、X線を補完する技術として使用することができます。[ 16 ]このセンサーは誘電特性をモニタリングすることで、皮下組織(骨、筋肉、脂肪など)の変化を検知できます。そのため、治癒過程の異なる時期に測定を行うと、外傷の治癒に合わせてセンサーの応答も変化します。
臨床工学
臨床工学は、病院やその他の臨床現場における医療機器や技術の実際の導入を扱うバイオメディカル工学の一分野です。臨床工学技師の主な役割には、バイオメディカル機器技術者(BMET)のトレーニングと監督、技術製品/サービスの選定とその導入におけるロジスティクス管理、検査/監査に関する政府規制当局との連携、そして他の病院スタッフ(医師、管理者、IT担当者など)への技術コンサルタントとしての役割などがあります。臨床工学技師はまた、臨床経験に基づいた将来的な設計改善について医療機器メーカーに助言や協力を行うとともに、最先端技術の進歩を監視し、それに応じて調達パターンを方向転換します。
技術の実用化に本質的に重点を置くため、革新的な研究開発や臨床導入まで何年もかかるアイデアではなく、段階的な再設計や再構成に重点を置く傾向があります。しかしながら、臨床エンジニアがバイオメディカル・イノベーションの軌跡に影響を与えることができるこの時間軸を拡大しようとする取り組みが活発化しています。臨床エンジニアは様々な役割において、使用現場に近い視点と製品・プロセスエンジニアリングの訓練を融合させることで、主要な設計者とエンドユーザーの間に「橋渡し」の役割を果たします。臨床エンジニアリング部門では、バイオメディカルエンジニアだけでなく、オペレーションズ・リサーチ/最適化、ヒューマンファクター、コスト分析などに取り組むために、産業エンジニア/システムエンジニアも採用することがあります。また、安全なシステムを設計するための手順については、安全工学の項を参照してください。臨床エンジニアリング部門は、マネージャー、スーパーバイザー、エンジニア、テクニシャンで構成されています。病院のベッド数80床につきエンジニア1人という比率です。臨床エンジニアには、侵襲的物品の FDA リコールを監視するために、製薬会社や関連店舗を監査する権限も与えられています。
リハビリテーション工学

リハビリテーション工学は、障害のある人々が直面する問題に対する技術的解決策を設計、開発、適応、試験、評価、適用、そして普及するために、工学科学を体系的に応用する学問です。リハビリテーション工学が対象とする機能領域には、移動、コミュニケーション、聴覚、視覚、認知、そして就労、自立生活、教育、そして地域社会への統合に関連する活動が含まれます。[ 1 ]
リハビリテーションエンジニアの中には、リハビリテーション工学(通常はバイオメディカル工学の専門分野)の修士号を取得している人もいますが、ほとんどのリハビリテーションエンジニアは、バイオメディカル工学、機械工学、または電気工学の学士号または大学院学位を取得しています。ポルトガルの大学では、リハビリテーション工学とアクセシビリティの学士号と修士号を取得できます。[ 7 ] [ 9 ]英国でリハビリテーションエンジニアになるには、コベントリー大学ヘルスデザイン&テクノロジー研究所などの大学の理学士優等学位コースを修了する必要があります。[ 10 ]
障害を持つ人々のリハビリテーションのプロセスには、多くの場合、ユーザーが社会、商業、レクリエーションの主流に参加できるようにするための歩行補助具などの補助装置の設計が含まれます。
規制上の問題
過去数十年間、医療機器に起因する患者への多くの事故に対応するため、規制上の課題は絶えず増加しています。例えば、2008年から2011年にかけて、米国ではクラスIに分類される医療機器のFDAリコールが119件発生しました。米国食品医薬品局(FDA)によると、クラスIリコールは「製品の使用または曝露によって深刻な健康被害または死亡が発生する可能性が合理的に高い状況」を指します[ 17 ]。
国ごとの法律にかかわらず、主要な規制の目的は世界中で一致しています。[ 18 ]たとえば、医療機器規制では、製品は1)安全で、2)効果的であり、3)製造されるすべての機器に適用可能である必要があります。
製品は、患者、使用者、および第三者が、その意図された使用において、傷害や死亡などの物理的ハザードの許容できないリスクにさらされない場合、安全であると言えます。危険な機器には、その使用から得られる便益と比較して、残留リスクを許容可能なレベルに低減するための保護対策を導入する必要があります。
製品は、製造業者が意図した用途において規定通りに機能する場合に有効とされます。有効性の証明は、臨床評価、性能基準への適合、または既に市販されている機器との実質的同等性の実証によって行われます。
前述の特性は、医療機器の製造品目すべてにおいて確保されなければなりません。そのためには、医療機器のライフサイクル全体にわたって安全性と有効性に影響を与える可能性のあるすべての関連組織およびプロセスに対して、品質システムを導入する必要があります。
医療機器工学分野は、工学の中でも最も規制の厳しい分野の一つであり、バイオメディカルエンジニアとして働く人は、規制法を専門とする弁護士やその他の専門家と日常的に相談し、協力しなければなりません。米国食品医薬品局(FDA)は、医療機器、医薬品、生物製剤、複合製品を管轄する、米国における主要な医療規制当局です。FDAの政策決定の主眼は、医療製品の安全性と有効性であり、これらは21 CFR 829規制に規定されている品質システムを通じて保証される必要があります。さらに、バイオメディカルエンジニアは、理学療法機器(医療機器でもある)など、「消費者」向けの機器や技術を開発することが多いため、これらも消費者製品安全委員会(CPSC)の規制を受ける場合があります。最大のハードルは、510K「クリアランス」(通常はクラス2機器)または市販前「承認」(通常は医薬品およびクラス3機器)です。
欧州では、安全性と有効性と品質は「適合性評価」を通じて保証されます。適合性評価とは、「製造業者が自社の機器が欧州医療機器規則(EMD)の要件に準拠していることを証明する方法」と定義されています。医療機器指令(MDM)は、認証のための詳細な手順を規定しています。一般的に、これらの手順には、リスク管理ファイル、技術ファイル、品質管理システムの成果物など、特定の成果物に含まれる試験と検証が含まれます。リスク管理ファイルは、その後の設計および製造工程の条件となる最初の成果物です。リスク管理段階では、機器の使用によって患者に期待されるベネフィットに関して、製品リスクが許容可能なレベルに低減されるように製品を推進する必要があります。技術ファイルには、医療機器認証を裏付けるすべての文書データと記録が含まれています。FDAの技術ファイルは、異なる構造で構成されているものの、同様の内容を含んでいます。品質システムの成果物には通常、製品ライフサイクル全体を通じて品質を保証する手順が含まれます。米国および世界中で、品質管理システムには通常、同じ規格(ISO 13485)が適用されます。

欧州連合(EU)には、欧州加盟国によって認定された「ノーティファイド・ボディ(Notified Body)」と呼ばれる認証機関があります。ノーティファイド・ボディは、製造業者が作成する適合宣言書があれば販売に十分なクラスI機器を除くすべての医療機器について、認証プロセスの有効性を保証する必要があります。製品が医療機器規則(EU)2017/745で要求されるすべての手順に合格すると、その機器はCEマークを貼付できるようになります。これは、機器が意図されたとおりに使用された場合、安全かつ有効であると考えられることを示し、 EU域内で販売できることを意味します。
異なる規制体制により、特定の技術が、より有利な規制形態に応じて、米国または欧州で最初に開発されるという結果になることがあります。各国は国境を越えた流通を促進するために実質的な調和を図ることがよくありますが、規制の最適な範囲に関する哲学的な相違が障害となる場合があります。より厳格な規制は直感的には魅力的に思えますが、批評家は、命を救う開発へのアクセスを遅らせるというトレードオフコストを非難しています。
RoHS II
指令 2011/65/EU(通称 RoHS 2)は、2002 年に最初に導入された法律を改正したものです。元の EU 法律「電気・電子機器における特定有害物質の制限」(RoHS 指令 2002/95/EC)は、2011 年 7 月に発行され、一般に RoHS 2 として知られる 2011/65/EU に置き換えられました。RoHS は、電子機器に循環する危険物質、特に毒素や重金属を制限することを目指しており、これらの物質は、機器のリサイクル時に環境に放出されます。
RoHS 2の適用範囲が拡大され、医療機器や産業機器など、これまで除外されていた製品も対象となりました。さらに、製造業者は適合性リスク評価書と試験報告書を提出する義務を負うようになり、提出しない場合はその理由を説明する義務も負うようになりました。RoHS指令の適用対象となる電気電子機器が有害物質の制限値を満たし、CEマークを製品に表示することを保証する責任は、製造業者だけでなく、輸入業者や販売業者も初めて共有することになります。
IEC 60601
在宅医療電気医療機器に関する新しい国際規格IEC 60601は、在宅医療環境で使用される機器の要件を定義しています。IEC 60601-1-11 (2010)は、IEC 60601第3版シリーズの他の適用可能な規格とともに、幅広い家庭用およびポイントオブケア医療機器の設計と検証に組み込む必要があります。
EN 欧州版規格の実施義務日は 2013 年 6 月 1 日です。米国 FDA は 2013 年 6 月 30 日に規格の使用を義務付けており、カナダ保健省は最近、義務付け日を 2012 年 6 月から 2013 年 4 月に延長しました。北米の機関は新規デバイスの申請にのみこれらの規格を義務付けますが、EU はより厳格なアプローチを採用し、市場に投入されるすべての該当デバイスに在宅ヘルスケア規格の考慮を義務付けます。
AS/NZS 3551:2012
AS/ANS 3551:2012は、オーストラリアとニュージーランドの医療機器管理に関する規格です。この規格は、臨床現場(例えば病院)における幅広い医療資産の維持管理に必要な手順を規定しています。[ 19 ]この規格は、IEC 606101規格に基づいています。
この規格は、調達、受入テスト、メンテナンス(電気安全および予防メンテナンステスト)、廃止など、医療機器管理の幅広い要素をカバーしています。
トレーニングと認定
教育
生物医学エンジニアには、工学と生物学の両方の相当の知識が必要であり、通常、生物医学工学 (BME) または BME と重複する可能性が高い他の工学分野の学士号 (B.Sc.、BS、B.Eng.、または BSE)、修士号 (MS、M.Sc.、MSE、または M.Eng.)、または博士号 (Ph.D.、またはMD-PhD [ 20 ] [ 21 ] [ 22 ] ) を取得しています。BME への関心が高まるにつれて、多くの工科大学に生物医学工学科またはプログラムが設置され、学部レベル (B.Sc.、BS、B.Eng.、または BSE) から博士課程レベルまで幅広い教育プログラムが提供されています。生物医学工学は、他の分野の学際的なハイブリッド専門分野ではなく、独自の分野として最近になって登場してきました。あらゆるレベルのBME(生物医学・医療・メディア関連)プログラムが普及しつつあり、その中には生物医学工学の理学士号も含まれています。この学位は十分な生物科学の内容を網羅しており、多くの学生が医学部進学準備のための「医学部進学準備」として利用しています。医療技術の向上は、原因と結果の両方として、生物医学エンジニアの数が増加すると予想されています。[ 23 ]
米国では、ますます多くの学部課程がABETの認定バイオエンジニアリング/バイオメディカルエンジニアリングプログラムとして認められるようになっています。2023年現在、155のプログラムがABETの認定を受けています。[ 24 ]
カナダとオーストラリアでは、生物医学工学の認定大学院プログラムが一般的です。[ 25 ]例えば、マクマスター大学は生物医学工学の修士号、医学博士号/博士号、博士号を提供しています。[ 26 ]カナダで最初の学部BMEプログラムは、4年間の工学士プログラムとしてグエルフ大学で提供されました。 [ 27 ]モントリオール工科大学も生物医学工学の学士号を提供しています。 [ 28 ]フリンダース大学も同様です。[ 29 ]
多くの学位と同様に、プログラムの評判とランキングは、就職や大学院入学において、学位取得者の選好度に影響を与える可能性があります。多くの学部学位の評判は、大学の大学院プログラムや研究プログラムとも関連しており、研究資金や研究量、出版物、引用数といった具体的な評価要素があります。特にビジネス・メディカル・メディシン(BME)分野では、大学の病院や医学部のランキングも、そのBME学科/プログラムの評判を左右する重要な要素となります。
大学院教育は、BME において特に重要な側面である。多くの工学分野(機械工学や電気工学など)では、その分野の初級職に就くために大学院レベルの訓練は必要ないが、BME の職の大多数では大学院レベルの訓練が望ましい、または必須とさえされている。[ 30 ] BME 関連の職業のほとんどは、製薬や医療機器開発など科学研究を伴うため、大学院教育はほぼ必須となっている(学部学位では通常、十分な研究訓練と経験を必要としないため)。これは修士または博士レベルの学位である。特定の専門分野では博士号が他の分野よりも著しく一般的であるが、大多数を占めることはほとんどない(学術界を除く)。実際、何らかの大学院資格の必要性が非常に高いと認識されているため、一部の学部の BME プログラムでは、修士号を取得する意思やその後の医学部への進学を明示していない学生が BME を専攻することを積極的に阻止している。
他の科学分野と同様に、BME(ビジネス・メディカル・メディシン)の大学院プログラムは非常に多様で、特定のプログラムでは、分野内の特定の側面に重点が置かれている場合があります。また、BMEの学際的な性質から、他分野のプログラム(大学の医学部や他の工学部など)との広範な共同研究が特徴となる場合もあります。修士課程および博士課程では、通常、出願者にBME、または他の工学分野(および特定の生命科学のコースワーク)、もしくは生命科学(および特定の工学のコースワーク)の学士号取得が求められます。
BME 教育も世界各地で大きく異なっている。米国は、大規模なバイオテクノロジー部門、多数の主要大学、および比較的少ない国内障壁のおかげで、BME 教育および訓練機会の発展において大きな進歩を遂げてきた。一方、大規模なバイオテクノロジー部門と優れた教育システムを持つヨーロッパは、依然として存在する国家間の管轄権の障壁の一部を欧州共同体が取り除こうと試みているため、統一基準の作成に問題を抱えている。最近では、BIOMEDEA などの BME 関連の教育および職業基準を開発するための取り組みが活発化している。[ 31 ]オーストラリアなど他の国々も、BME 教育の欠陥を認識し、是正に取り組んでいる。[ 32 ]また、ハイテクへの取り組みは通常先進国の特徴であるため、世界の一部の地域では、BME を含む教育の発展が遅れる傾向がある。
免許/認定
他の学識のある専門職と同様に、各州には登録プロフェッショナル エンジニア(PE) としてのライセンスを取得するための特定の (かなり類似した) 要件がありますが、米国では、業界では、ほとんどの場合、エンジニアとして雇用されるためにそのようなライセンスは必要ありません (事実上、大多数のアメリカ人エンジニアに適用される産業免除と呼ばれる例外のため)。米国のモデルでは、一般的に、公共の福祉、安全、生命、健康、財産の保護に影響するエンジニアリング サービスを提供する現役エンジニアにのみライセンスが必要であり、民間企業で働くエンジニアで、公共またはその他の企業、教育、政府に直接エンジニアリング サービスを提供していないエンジニアにはライセンスは不要です。これは、法律や医学と同様、エンジニアリングの実践にもライセンスが法的に必要である他の多くの国では特に当てはまりません。
オーストラリアなど一部の国ではバイオメディカルエンジニアリングは規制されていますが、登録は通常推奨されるだけで必須ではありません。[ 33 ]
英国では、医療工学、バイオエンジニアリング、または生物医学工学の分野で働く機械エンジニアは、機械技術者協会(Institution of Mechanical Engineers)を通じて公認エンジニアの資格を取得できます。同協会は医学・健康工学部門も運営しています。[ 34 ]医学物理工学協会(IPEM)には、生物医学工学の修士課程の認定委員会があり、IPEMを通じて公認エンジニアの資格を取得することもできます。
エンジニアリングの基礎試験は、米国のほとんどの管轄区域で実施される 2 つの資格試験のうち最初の (より一般的な) 試験であり、現在は生物学をカバーしています (厳密には BME ではありません)。2 つ目の試験は「Principles and Practices, Part 2」または「Professional Engineering 試験」と呼ばれ、受験者は特定のエンジニアリング分野の内容を選択してテストを受けることができます。現在、この試験には BME のオプションがありません。つまり、資格取得を目指すバイオメディカル エンジニアは、別のカテゴリでこの試験を受ける準備をする必要があります (ほとんどの管轄区域では分野の専門分野を認めていないため、これは実際の資格には影響しません)。ただし、生物医学工学協会 (BMES) は、2009 年の時点で、資格取得を目指すバイオメディカル エンジニアを容易にするために、この試験の BME 専用バージョンを実装する可能性を検討しています。
政府機関による登録に加え、民間の専門機関や業界団体も、様々なレベルの認定資格を提供しています。その一例が、臨床工学技師向けの認定臨床工学技師(CCE)です。
キャリアの見通し
2012年には、米国で約19,400人のバイオメディカルエンジニアが雇用されており、この分野は2012年から2022年にかけて5%(平均より速いペース)成長すると予測されていました。[ 35 ]バイオメディカルエンジニアリングは、他の一般的なエンジニアリング職種と比較して、女性エンジニアの割合が最も高い分野です。2023年現在、この学位取得者には19,700件の求人があり、この分野の平均給与は約100,730ドル、時給は約48.43ドルです。また、2023年から2033年にかけて、雇用は7%増加すると予想されています(前回の平均よりも速いペースです)。
著名人
- ジュリア・トゥテルマン・アプター(故人) – 神経生理学研究の最初の専門家の一人[ 36 ]であり、生物医学工学協会の創設メンバー[ 37 ]
- アール・バッケン(故人) - 最初のトランジスタ式ペースメーカーを発明し、メドトロニックの共同創設者。
- フォレスト・バード(故人) – 飛行士であり、人工呼吸器の発明の先駆者
- YC Fung(故人) -カリフォルニア大学サンディエゴ校名誉教授。多くの人から現代バイオメカニクスの創始者と考えられている[ 38 ]
- レスリー・ゲデス(故人)は、パデュー大学名誉教授で、電気技師、発明家、2000人以上のバイオメディカルエンジニアの教育者であり、火傷治療から小型除細動器、靭帯修復から未熟児用小型血圧モニター、心肺蘇生法(CPR )の新しい方法に至るまで、50年以上にわたる貢献により、 2006年にジョージ・ブッシュ大統領から国家技術賞を受賞しました[ 39]。
- ウィレム・ヨハン・コルフ(故人) -血液透析と人工臓器の分野の先駆者
- ロバート・ランガー– MITの研究所教授。世界最大のBME研究所を運営し、薬物送達と組織工学の先駆者[ 40 ]
- ジョン・マクラウド(故人) –ケース・ウェスタン・リザーブ大学でインスリンの共同発見者の一人。
- アルフレッド・E・マン– 物理学者、起業家、慈善家。生物医学工学の分野の先駆者。[ 41 ]
- J・トーマス・モーティマー – ケース・ウェスタン・リザーブ大学名誉生体医学工学教授。機能的電気刺激(FES)のパイオニア[ 42 ]
- ロバート・M・ネレム–ジョージア工科大学名誉教授。再生組織とバイオメカニクスのパイオニアであり、300以上の論文を発表。彼の論文は累計2万回以上引用されている。
- P.ハンター・ペッカム – ケース・ウェスタン・リザーブ大学生体医学工学・整形外科教授。機能的電気刺激(FES)のパイオニア[ 43 ]
- ニコラス A. ペパス–テキサス大学オースティン校工学部教授。薬物送達、生体材料、ハイドロゲル、ナノバイオテクノロジーの先駆者。
- ロバート・プロンジー–デューク大学名誉教授、電気生理学の先駆者[ 44 ]
- オットー・シュミット(故人) –バイオミメティクスの研究でBMEに多大な貢献をした生物物理学者
- アッシャー・シャピロ(故人) - MITの研究所教授。BME分野、医療機器(大動脈内バルーンなど)の発展に貢献。
- ゴルダナ・ヴニャク=ノヴァコビッチ–コロンビア大学教授、組織工学とバイオリアクター設計の先駆者
- ジョン・G・ウェブスター–ウィスコンシン大学マディソン校名誉教授、電気生理学的信号記録用計装アンプ分野の先駆者
- フレッド・ワイベル、『バイオメディカル機器と測定』の共著者
- UAウィテカー(故人) -ウィテカー財団の提供者。同財団は、様々な大学に7億ドル以上を提供し、30のBMEプログラムの創設と13の建物の建設資金援助を行うことで、BMEの研究と教育を支援した[ 45 ]
参照
- バイオメディシン – 医学の分野
- 心臓物理学
- 計算解剖学 – 生物学の学際分野
- 医学物理学 – 医学やヘルスケアにおける物理学の応用
- フィジオーム – 生物の全体的な生理学的ダイナミクス
- 生物医学工学および計測プログラム(BEIP)
参考文献
- ^ a bジョン・デニス・エンダール、ジョセフ・D・ブロンズィーノ (2012).バイオメディカルエンジニアリング入門. アカデミック・プレス. pp. 16–. ISBN 978-0-12-374979-6. 2024年7月26日時点のオリジナルよりアーカイブ。2016年2月22日閲覧。
- ^ Fakhrullin, Rawil; Lvov, Yuri 編 (2014).細胞表面工学. スマートマテリアルシリーズ. ケンブリッジ: 王立化学協会. doi : 10.1039/9781782628477 . ISBN 978-1-78262-847-7. 2021年1月25日時点のオリジナルよりアーカイブ。2019年3月28日閲覧。
- ^ネベッカー、フレデリック (2001). 「アメリカ合衆国におけるバイオメディカルエンジニアリングの出現」.国際技術史委員会. 7 : 75–94 . JSTOR 23786025 .
- ^ Alexander R. McNeill (2005). 「動物の運動の力学」 . Current Biology . 15 (16): R616– R619. doi : 10.1016/j.cub.2005.08.016 . PMID 16111929. S2CID 14032136 .
- ^ Hatze, Herbert (1974). 「バイオメカニクスという用語の意味」. Journal of Biomechanics . 7 (12): 189– 190. doi : 10.1016/0021-9290(74)90060-8 . PMID 4837555 .
- ^ 「生物医学光学入門」(PDF)。2024年7月26日時点のオリジナルよりアーカイブ(PDF) 。 2018年1月25日閲覧。
- ^ a b「幹細胞から作られた顎骨」 BBCニュース、2009年10月10日。2009年10月11日時点のオリジナルよりアーカイブ。 2009年10月11日閲覧。
- ^ Walles T.気管支バイオエンジニアリング:満たされていない医療ニーズを満たすバイオテクノロジー. Adv Drug Deliv Rev. 2011; 63(4–5): 367–74.
- ^ a b「医師、患者自身の細胞から臓器を培養」 CNN、2006年4月3日。2017年5月25日時点のオリジナルよりアーカイブ。2006年10月2日閲覧。
- ^ a bヒト細胞を使った初の人工肝臓装置の試験開始Archived 2011-01-05 at the Wayback Machine , University of Chicago , February 25, 1999
- ^リチャード・A・アンダーセン、ユン・ジョン・ファン、グラント・H・マリケン (2010). 「認知神経補綴」 . Annual Review of Psychology . 61 : 169–C3. doi : 10.1146/annurev.psych.093008.100503 . ISSN 0066-4308 . PMC 2849803. PMID 19575625 .
- ^ヘデ、シャンテシュ;ナグラジ州ヒュルゴル(2006 年 10 月)。」「ナノ」:がんの新たな宿敵 Hede S, Huilgol N – J Can Res Ther . cancerjournal.net . 2 (4). 2015年12月22日時点のオリジナルよりアーカイブ。2007年2月2日閲覧。
- ^ Couvreur, Patrick; Vauthier, Christine (2006). 「ナノテクノロジー:複雑な疾患を治療するためのインテリジェントデザイン」 .製薬研究. 23 (7): 1417–1450(34). doi : 10.1007/s11095-006-0284-8 . PMID 16779701. S2CID 1520698 .
- ^ Curtis, Adam SG; Dalby, Matthew; Gadegaard, Nikolaj (2006). 「ナノトポグラフィーに起因する細胞シグナル伝達:ナノ医療機器への影響」. Nanomedicine . 1 (1): 67– 72. doi : 10.2217/17435889.1.1.67 . ISSN 1743-5889 . PMID 17716210 .
- ^ Jacobson, Lewis E.; Olayan, May; Williams, Jamie M.; Schultz, Jacqueline F.; Wise, Hannah M.; Singh, Amandeep; Saxe, Jonathan M.; Benjamin, Richard; Emery, Marie; Vilem, Hilary; Kirby, Donald F. (2019年11月1日). 「小口径栄養チューブ留置のための新規電磁気デバイスの実現可能性と安全性」 . Trauma Surgery & Acute Care Open . 4 (1) e000330. doi : 10.1136/tsaco-2019-000330 . ISSN 2397-5776 . PMC 6861064. PMID 31799414. 2023年3月3日時点のオリジナルよりアーカイブ。2023年3月3日閲覧。
- ^ Shah, Syaiful; Velander, Jacob; Mathur, Parul; Perez, Mauricio; Asan, Noor; Kurup, Dhanesh; Blokhuis, Taco; Augustine, Robin (2018-02-21). 「下肢外傷リハビリテーションにおける生体内マイクロ波反射率と超音波測定を用いたスプリットリング共振器センサーの浸透深度評価」 . Sensors . 18 (2): 636. Bibcode : 2018Senso..18..636S . doi : 10.3390/s18020636 . ISSN 1424-8220 . PMC 5855979. PMID 29466312 .
- ^米国食品医薬品局、医療機器および放射線放出機器のリコール[1]
- ^ 「医療機器規制:世界的概要と指針」(PDF)世界保健機関(WHO)2003年。2013年10月25日時点のオリジナルよりアーカイブ(PDF) 。 2013年9月13日閲覧。
- ^ AS/NZS 3551:2012 医療機器管理プログラム. Standards Australia. 2016年10月18日. ISBN 978-1-74342-277-9. 2014年3月11日時点のオリジナルよりアーカイブ。2016年10月18日閲覧。
- ^ 「MD-PhDプログラム」ジョンズ・ホプキンス大学生物医学工学部。2022年11月29日時点のオリジナルよりアーカイブ。 2022年11月29日閲覧。
- ^ "PhD+MD" .ダートマス工学部. 2022年11月29日時点のオリジナルよりアーカイブ。2022年11月29日閲覧。
- ^ 「医師・エンジニア養成プログラム」ウェルドン・スクール・オブ・バイオメディカル・エンジニアリング – パデュー大学. 2022年11月29日時点のオリジナルよりアーカイブ。 2022年11月29日閲覧。
- ^米国労働統計局– エンジニアのプロフィール2006年2月19日アーカイブ、 Wayback Machine
- ^ “Disciplines. Countries. USA” . 2023年2月20日時点のオリジナルよりアーカイブ。2023年2月20日閲覧。
- ^ Goyal, Megh R. (2018-01-03).バイオエンジニアリングと生物工学における科学技術用語. CRC Press. ISBN 978-1-351-36035-7. 2024年7月26日時点のオリジナルよりアーカイブ。2023年5月5日閲覧。
- ^ 「学位オプション」マクマスター生物医学工学部eng.mcmaster.ca. 2019年10月24日時点のオリジナルよりアーカイブ。 2019年10月24日閲覧。
- ^ 「2010–2011 学部課程カレンダー – 生物医学工学」 . グエルフ大学. 2010年9月7日. 2024年7月26日時点のオリジナルよりアーカイブ。 2024年4月7日閲覧。
- ^ “生物医学バカロレア” .ポリテクニックモントリオール。 2018年1月15日。 2020年10月12日のオリジナルからアーカイブ。2020 年10 月 11 日に取得。
- ^ 「工学士(生物医学)(優等学位)」フリンダース大学。2024年7月26日時点のオリジナルよりアーカイブ。 2019年10月24日閲覧。
- ^ 「エンジニアの雇用見通し」米国労働統計局。 2011年12月19日時点のオリジナルよりアーカイブ。
- ^ "BIOMEDEA" . 2005年9月. 2008年5月6日時点のオリジナルよりアーカイブ。
- ^ Lithgow, BJ (2001年10月25日). 「バイオメディカルエンジニアリングカリキュラム:米国、欧州、オーストラリアの比較」 . 2008年5月1日時点のオリジナルよりアーカイブ。
- ^ 「National Engineering Register」 . Engineers Australia. 2008年1月5日時点のオリジナルよりアーカイブ。 2023年3月11日閲覧。
- ^ 「Medical Engineering: Homepage」 . Institution of Mechanical Engineers . 2007年5月2日時点のオリジナルよりアーカイブ。
- ^米国労働省労働統計局。職業展望ハンドブック 2014-15年版:バイオメディカルエンジニア。 2021年4月17日アーカイブ。Wayback Machineにて。
- ^ 「シカゴ在住、眼科医兼研究者のジュリア・アプター博士(61歳)」『ニューヨーク・タイムズ』 1979年4月18日。ISSN 0362-4331。2023年3月1日時点のオリジナルよりアーカイブ。 2023年3月1日閲覧。
- ^ Fagette Jr., Paul H.; Horner, Patricia I., eds. (2004). Celebrating 35 years of Biomedical Engineering: An Historical Perspective (PDF) . Landover, MD: Biomedical Engineering Society . p. 4. 2023年3月1日時点のオリジナルよりアーカイブ(PDF) . 2023年3月1日閲覧。
- ^ Kassab, Ghassan S. (2004). 「YC "Bert" Fung: 現代バイオメカニクスの父」(PDF) . Mechanics & Chemistry of Biosystems . 1 (1). Tech Science Press: 5– 22. doi : 10.3970/mcb.2004.001.005 . PMID 16783943. 2007年12月2日時点のオリジナル(PDF)からのアーカイブ。
- ^ 「レスリー・ゲデス – 2006年アメリカ国家技術賞」 2007年7月31日. 2021年11月7日時点のオリジナルよりアーカイブ。 2011年9月24日閲覧– YouTubeより。
- ^ O'Neill, Kathryn M. (2006年7月20日). 「同僚たちがランガー氏の30年間の革新を称える」 MITニュースオフィス. 2014年2月18日時点のオリジナルよりアーカイブ。 2007年3月16日閲覧。
- ^ Gallegos, Emma (2010年10月25日). 「アルフレッド・E・マン科学研究財団(AMF)」 . Aemf.org. 2012年7月24日時点のオリジナルよりアーカイブ。 2011年9月24日閲覧。
- ^ "J. Thomas Mortimer" . CSE Faculty/Staff Profiles . engineering.case.edu. 2023年5月2日時点のオリジナルよりアーカイブ。 2018年6月14日閲覧。
- ^ “P. Hunter Peckham, PhD | Distinguished University Professor | Case Western Reserve University” . Distinguished University Professor | Case Western Reserve University . 2018年4月25日. 2024年7月26日時点のオリジナルよりアーカイブ。 2018年6月14日閲覧。
- ^ 「ロバート・プロンジー、ファイザー・プラット名誉教授」デューク大学BME学部Fds.duke.edu 2009年6月5日時点のオリジナルよりアーカイブ。 2009年10月11日閲覧。
- ^ 「The Whitaker Foundation」 Whitaker.org。2011年9月25日時点のオリジナルよりアーカイブ。2011年9月24日閲覧。
45. ^米国労働統計局、米国労働省、職業展望ハンドブック、「バイオエンジニアとバイオメディカルエンジニア」、2024年10月27日閲覧。
さらに読む
- ブロンズィーノ、ジョセフ・D.(2006年4月)『バイオメディカルエンジニアリングハンドブック(第3版)』[CRC Press] ISBN 978-0-8493-2124-5. 2015年2月24日時点のオリジナルよりアーカイブ。2009年6月22日閲覧。
- ヴィラファネ、カルロス(2009年6月)『バイオメッド:学生の視点から』(初版)[Techniciansfriend.com] ISBN 978-1-61539-663-4. 2021年2月13日時点のオリジナルよりアーカイブ。2010年12月22日閲覧。
外部リンク
 ウィキメディア・コモンズにおける生物医学工学関連のメディア
ウィキメディア・コモンズにおける生物医学工学関連のメディア


