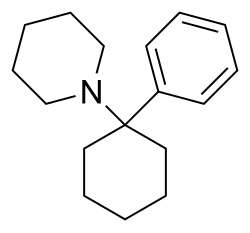
フェンシクリン
 | |
 | |
| 臨床データ | |
|---|---|
| 商号 | セルニル、セルニラン(いずれも販売終了) |
| その他の名前 | CI-395; フェニルシクロヘキシルピペリジン; 「エンジェルダスト」[ 1 ] |
| AHFS / Drugs.com | フェンサイクリジン |
| 依存責任 | 身体的:低 心理的:中程度[ 2 ] |
| 中毒責任 | 変動性があり、低いものから高いものまで報告されている[ 3 ] [ 2 ] |
| 投与経路 | 喫煙、注射、鼻から吸い込む、口から摂取する[ 4 ] [ 5 ] |
| 薬物クラス | NMDA受容体拮抗薬、全身麻酔薬、解離性幻覚剤[ 4 ] |
| ATCコード |
|
| 法的地位 | |
| 法的地位 | |
| 薬物動態データ | |
| 代謝 | 肝臓におけるCYP450酵素による酸化的水酸化、グルクロン酸抱合 |
| 代謝物 | PCHP、PPC、PCAA |
| 作用発現 | 2~60分[ 6 ] |
| 消失半減期 | 7~46時間 |
| 作用持続時間 | 6~48時間[ 6 ] |
| 排泄 | 尿 |
| 識別子 | |
| |
| CAS番号 |
|
| PubChem CID | |
| IUPHAR/BPS | |
| ドラッグバンク |
|
| ケムスパイダー |
|
| ユニイ | |
| ケッグ |
|
| チェビ |
|
| チェムブル |
|
| CompToxダッシュボード(EPA) | |
| ECHA 情報カード | 100.150.427 |
| 化学および物理データ | |
| 式 | C 17 H 25 N |
| モル質量 | 243.394 g·mol −1 |
| 3Dモデル(JSmol) | |
| 融点 | 46.5℃(115.7℉) |
| 沸点 | 136℃(277℉) |
| |
| |
| データページ | |
| フェンシクリジン(データページ) | |
 北 北 はい (これは何ですか?)(確認) はい (これは何ですか?)(確認) | |
フェンシクリジンまたはフェニルシクロヘキシルピペリジン(PCP)は、ストリートドラッグとしてエンジェルダストなどの別名でも知られ、主にその著しい精神変容作用のために娯楽目的で用いられる解離性麻酔薬である。 [ 1 ] [ 4 ] PCPは幻覚、歪んだ音知覚、精神病的行動を引き起こす可能性がある。[ 4 ] [ 7 ] [ 8 ]娯楽用薬物として、通常は喫煙されるが、経口摂取、鼻から吸い込む、または注射することもある。[ 4 ] [ 5 ] [ 7 ]大麻やタバコと混合されることもある。[ 1 ] [ 4 ]
副作用としては、妄想、依存症、自殺リスクの増加、過剰摂取による発作や昏睡などが挙げられる。[ 7 ]使用を中止してもフラッシュバックが起こることがある。 [ 8 ]化学的には、PCPはアリールシクロヘキシルアミン類に属する。[ 4 ] [ 9 ] [ 10 ] PCPは主にNMDA受容体拮抗薬として作用する。[ 9 ]
PCPは米国で最も一般的に使用されています。[ 11 ]米国での使用は1970年代にピークを迎えましたが、[ 12 ] 2005年から2011年の間に、この薬剤による救急外来の受診が増加しました。[ 7 ] 2022年現在、米国では12年生の約0.7%が前年にPCPを使用したと報告しており、25歳以上の米国人の1.7%が人生のある時点でPCPを使用したと報告しています。[ 13 ]
レクリエーション用途

フェンシクリジンは解離状態を誘発する能力のために使用される。[ 14 ]
効果
行動への影響は投与量によって異なります。低用量では、四肢の麻痺と酩酊状態を引き起こし、よろめき、歩行の不安定さ、ろれつが回らない、目の充血、平衡感覚の喪失などの症状が現れます。中用量(鼻腔内投与5~10 mg、または筋肉内または静脈内投与0.01~0.02 mg/kg)では鎮痛作用と麻酔作用が得られます。高用量では痙攣を引き起こす可能性があります。[ 15 ]この薬物は、しばしば管理が不十分な条件下で違法に製造されるため、使用者は実際に摂取している量に気付かない可能性があります。[ 16 ]
心理的影響としては、身体イメージの著しい変化、自我の境界の喪失、妄想、離人症などが挙げられます。精神病、興奮、不快感、幻覚、視力低下、多幸感、自殺衝動、そして時折の攻撃的行動も報告されています。[ 17 ] [ 18 ] : 48–49 [ 15 ] PCPは、強さ、力、無敵感といった感情を引き起こすだけでなく、精神を麻痺させる効果も引き起こす可能性があります。[ 5 ]
1970年代の薬物乱用警告ネットワークによる調査では、PCPによって引き起こされた暴力に関するメディアの報道は大きく誇張されており、暴力事件はまれで、薬物使用に関係なく攻撃的であると評判の個人に限られていることが示されています。 [ 18 ] : 48 まれではありますが、PCP中毒の個人が妄想や幻覚によって引き起こされた可能性のある予測できない行動をとる事件が公表されています。[ 19 ]よく挙げられるその他の事件の種類には、器物損壊や、歯を抜くなどの様々なタイプの自傷行為が含まれます。[ 18 ] : 48 [ 19 ]これらの影響は1950年代と1960年代の医療目的での使用では注目されていませんでしたが、PCPによる身体的暴力の報告は根拠がないことがしばしば示されています。[ 20 ] [ 21 ]
娯楽目的での薬物摂取は、統合失調症の発作に似た感情的・認知的障害を伴う精神病状態を引き起こすこともある。[ 22 ] [ 23 ]使用者は一般的に現実から切り離された感覚を報告している。[ 24 ]
症状は「RED DANES」という記憶法で要約される:激怒、紅斑(皮膚の発赤)、瞳孔散大、妄想、健忘、眼振(横に動くときの眼球の振動)、興奮、皮膚の乾燥。[ 25 ]
中毒
PCPは自己投与され、側坐核のD1型中型有棘ニューロンでΔFosBの発現を誘導し、[ 3 ] [ 26 ]、したがって、PCPの過剰使用は依存症を引き起こすことが知られています。[ 3 ] PCPの報酬効果と強化効果は、少なくとも部分的には、側坐核のD1型中型有棘ニューロンへのグルタミン酸入力におけるNMDA受容体を阻害することによって媒介されます。 [ 3 ] PCPは動物実験で条件付け場所嫌悪と条件付け場所嗜好を生み出すことが示されている。[ 27 ]
統合失調症
2019年のレビューによると、幻覚剤誘発性精神病(PCPを含む)の診断から統合失調症への移行率は26%でした。これは大麻誘発性精神病(34%)より低いものの、アンフェタミン誘発性精神病(22%)、オピオイド誘発性精神病(12%)、アルコール誘発性精神病(10%)、鎮静剤誘発性精神病(9%)よりは高い数値でした。一方、「短期、非定型、その他特定不能」精神病の統合失調症への移行率は36%でした。[ 28 ]
投与方法
PCPには複数の投与経路があります。最も一般的なのは、粉末状の薬物を鼻から吸入することです。また、PCPは経口摂取、皮下注射、静脈注射、あるいはマリファナやタバコに混ぜて喫煙することもあります。[ 29 ]
- PCPは喫煙によって摂取される可能性があります。「フライ」や「シェルム」は、PCPに浸して乾燥させたマリファナやタバコを指す俗語です。[ 30 ]
- PCP塩酸塩は、純度に応じて吸入(鼻から吸入)することができます。これは「エンジェルダスト」と呼ばれることがよくあります。[ 29 ]
- 薬剤を配合した粉末を圧縮して経口錠剤にすることもできます。これは通常「ピースピル」と呼ばれます。[ 29 ]
- 遊離塩基は疎水性であるため、皮膚や粘膜から吸収される可能性があります(多くの場合、意図せず吸収されます)。この形態の薬物は一般に「ワック」と呼ばれます。[ 29 ]
中毒の管理
PCP中毒の管理は、主に支持療法(呼吸、循環、体温のコントロール)と、初期段階での精神症状の治療から構成されます。[ 31 ] [ 32 ] [ 33 ]ロラゼパムなどのベンゾジアゼピンは、興奮や発作(存在する場合)のコントロールに選択される薬剤です。フェノチアジンやハロペリドールなどの定型抗精神病薬は精神病症状のコントロールに使用されてきましたが、ジストニアなどの多くの望ましくない副作用を引き起こす可能性があるため、その使用はもはや好まれていません。 フェノチアジンは、発作閾値を下げ、高体温を悪化させ、PCPの抗コリン作用を増強する可能性があるため、特に危険です。 [ 31 ] [ 32 ]抗精神病薬を投与する場合は、ハロペリドールの筋肉内投与が推奨されています。[ 33 ] [ 34 ] [ 35 ]
強制利尿(塩化アンモニウム、またはより安全なアスコルビン酸を使用)は、体内からのPCPのクリアランスを増加させる可能性があり、過去には除染対策として多少物議を醸しながら推奨されていました。[ 31 ] [ 32 ] [ 33 ]しかし、現在ではPCP投与量の約10%のみが腎臓で除去されることが分かっており、尿クリアランスの増加はほとんど影響がありません。さらに、尿の酸性化はアシドーシスを引き起こし、 PCP毒性の珍しい症状ではない横紋筋融解症(筋肉の破壊)を悪化させる可能性があるため、危険です。 [ 31 ] [ 32 ]
薬理学
薬力学
| サイト | Ki ( nM ) | アクション | 種 | 参照 |
|---|---|---|---|---|
| NMDAツールチップ N-メチル-D-アスパラギン酸受容体 | 59 | 敵対者 | 人間 | [ 38 ] [ 39 ] |
| モアツールチップ μ-オピオイド受容体 | 10,000以上 | ND | 人間 | [ 38 ] |
| ドールツールチップ δ-オピオイド受容体 | 10,000以上 | ND | 人間 | [ 38 ] |
| 韓国語ツールチップ κ-オピオイド受容体 | 10,000以上 | ND | 人間 | [ 38 ] |
| いいえツールチップ ノシセプチン受容体 | 10,000以上 | ND | 人間 | [ 38 ] |
| σ 1 | 10,000以上 | アゴニスト | モルモット | [ 38 ] [ 40 ] |
| σ 2 | 136 | アゴニスト | ねずみ | [ 38 ] |
| D2 | 10,000以上 | ND | 人間 | [ 38 ] |
| D 2ハイ | 2.7~4.3 144 ( EC 50 ) | 部分作動薬 | ラット/ヒトヒト | [ 41 ] [ 42 ] [ 43 ] |
| 5-HT 2A | 10,000以上 | ND | 人間 | [ 38 ] |
| 5-HT 2A高 | ≥5,000 | 部分的 アゴニスト | ねずみ | [ 42 ] [ 44 ] |
| サートツールチップ セロトニントランスポーター | 2,234 | 阻害剤 | 人間 | [ 38 ] |
| ネットツールチップ ノルエピネフリントランスポーター | 10,000以上 | 阻害剤 | 人間 | [ 38 ] |
| ダットツールチップ ドーパミントランスポーター | 10,000以上 | 阻害剤 | 人間 | [ 38 ] |
| PCP 2 | 154 | アゴニスト | 人間 | [ 39 ] |
| [ 3 H] 5-HTの取り込み | 1,424 ( IC 50 ) | 阻害剤 | ねずみ | [ 45 ] |
| [ 3 H] NIS結合 | 16,628 (IC 50 ) | 阻害剤 | ねずみ | [ 45 ] |
| [ 3 H] DAの取り込み | 347 (IC 50 ) | 阻害剤 | ねずみ | [ 45 ] |
| [ 3 H] CFT結合 | 1,547 (IC 50 ) | 阻害剤 | ねずみ | [ 45 ] |
| 値はK i (nM)で表されます。値が小さいほど、薬剤がその部位に強く結合します。 | ||||
PCPは、イオンチャネル型グルタミン酸受容体であるNMDA受容体への主な作用でよく知られています。[ 46 ] [ 43 ]そのため、PCPは非競合的NMDA受容体拮抗薬です。PCP、ケタミン、および関連解離剤の効果におけるNMDAR拮抗作用の役割は、1980年代初頭にDavid Lodge [ 47 ]と同僚によって初めて発表されました。[ 48 ]その他のNMDA受容体拮抗薬には、ケタミン、[ 49 ]チレタミン、[ 50 ]デキストロメトルファン、[ 51 ]亜酸化窒素、ジゾシルピン(MK-801)などがあります。
研究によると、PCPはニコチン性アセチルコリン受容体(nAChR)を阻害するなど、様々なメカニズムで作用することが示されています。PCP類似体は、nACh受容体[ 52 ]とNMDA受容体[ 53 ]に対して様々な効力を示します。シナプス前nAChRとNMDA受容体の相互作用は、グルタミン酸作動性シナプスのシナプス後成熟に影響を及ぼし、その結果、脳のシナプス発達と可塑性に影響を与えることが研究で示されています。[ 54 ]これらの影響は、海馬[ 55 ]や小脳[ 56 ]などの特定の脳領域における興奮性グルタミン酸活動の抑制につながる可能性があり、長期使用の影響の1つとして記憶喪失につながる可能性があります。小脳への急性影響は、中毒時の血圧、呼吸数、脈拍数の変化、および筋肉協調運動の喪失として現れます。[ 8 ]
PCPはケタミンと同様に、ラット脳ホモゲネート中で強力なドーパミンD2高受容体部分作動薬として作用し[ 43 ]、ヒトクローンD2高受容体にも親和性を示す[ 57 ]。この作用はPCP中毒の他の精神病的特徴と関連している可能性があり、これはPCP精神病の治療におけるD2受容体拮抗薬(ハロペリドールなど)の有効性によって証明されている。[ 58 ]
NMDA受容体との相互作用が十分に研究されていることに加えて、PCPはドーパミンの再取り込みを阻害することも示されており、それによって細胞外ドーパミン濃度が上昇し、ドーパミン作動性神経伝達が増加する。[ 59 ]しかし、PCPはドーパミントランスポーター(DAT)を含むヒトのモノアミントランスポーターに対する親和性がほとんどない。[ 38 ]代わりに、モノアミン再取り込みの阻害は、モノアミントランスポーターのアロステリック部位との相互作用によって媒介されている可能性がある。[ 38 ] PCPは、モノアミン再取り込み阻害に関連する十分に特徴付けられていない部位であるPCP部位2(Ki = 154 nM)の高親和性リガンドであることは注目に値する。[ 39 ]
ラットの研究では、PCPがオピオイド受容体(エンドルフィンとエンケファリン)と間接的に相互作用して鎮痛作用を発揮することが示されている。[ 60 ]
結合試験では、神経伝達物質受容体およびトランスポーターを含む 56 部位で PCP を評価し、NMDA 受容体のジゾシルピン(MK-801) 部位 (K i = 59 nM)、σ 2受容体( PC12 ) (K i = 136 nM)、およびセロトニントランスポーター(K i = 2,234 nM)を除くすべての部位でPCPの Ki 値が 10,000 nM を超えることが判明しました。[ 38 ]この研究では、特に D 2 受容体、オピオイド受容体、σ 1 受容体、およびドーパミンとノルエピネフリンのトランスポーターで Ki値が10,000 nMを超えることがわかりました。[ 38 ]これらの結果は、PCPが NMDAR および σ 2受容体の高度に選択的なリガンドであることを示唆しています。[ 38 ]しかし、PCPはモノアミントランスポーターのアロステリック部位と相互作用して、モノアミンの再取り込みを阻害する可能性がある。[ 38 ]
作用機序
フェンシクリジンは、NMDA受容体の活動を阻害して、心肺抑制を引き起こすことなく麻酔と鎮痛を引き起こす非競合的NMDA受容体拮抗薬である。[ 61 ] [ 17 ] NMDAは脳内の興奮性受容体で、正常に活性化されると受容体はイオンチャネルとして機能し、チャネルを通じて正イオンが流入して神経細胞の脱分極を引き起こす。フェンシクリジンは、イオンチャネル内にある特定のPCP結合部位に結合することにより、NMDA受容体を阻害する。[ 62 ] PCP結合部位はマグネシウム阻害部位の近くにあるため、同様の阻害効果を説明できる可能性がある。[ 63 ] PCP部位での結合は、受容体内の2つの非共有結合性相互作用、水素結合と疎水性相互作用によって媒介される。[ 64 ]結合はイオンチャネルのゲーティング機構によっても制御される。 PCP部位はイオンチャネル内に位置しているため、グリシンなどの共作動薬が結合してチャネルを開き、PCPが侵入してPCP部位に結合し、チャネルを遮断する必要がある。[ 65 ]
神経毒性
いくつかの研究では、PCPは他のNMDA受容体拮抗薬と同様に、ラットでオルニー病変と呼ばれる一種の脳障害を引き起こす可能性があることがわかっています。[ 66 ] [ 67 ]ラットで実施された研究では、NMDA受容体拮抗薬ジゾシルピンの高用量がラットの脳の特定の領域に可逆的な空胞形成を引き起こしました。オルニー病変の研究はすべて非ヒト動物でのみ実施されており、人間には当てはまらない可能性があります。フランク・シャープによる未発表の研究では、構造が類似した薬物であるNMDA拮抗薬ケタミンは、娯楽用量をはるかに超えても損傷を示さなかったと報告されていますが、[ 68 ]この研究は発表されていないため、その妥当性は議論の余地があります。
PCP はラットの脳内のN -アセチルアスパラギン酸およびN -アセチルアスパルチルグルタミン酸のレベルに統合失調症様の変化を引き起こすことも示されており、これは生きたラットおよび脳組織の剖検検査の両方で検出されます。 [ 69 ]また、ヒトでは統合失調症に似た症状を引き起こします。[ 70 ] PCP は統合失調症に似た症状を引き起こしただけでなく、視床皮質経路(デルタ波の増加、アルファ波の減少)および海馬(シータ波の増加)で統合失調症に似た脳波の変化も引き起こしました。[ 71 ] PCPによって誘発されるドーパミン放出の増加は、統合失調症の NMDA 仮説とドーパミン仮説を結び付ける可能性があります。[ 72 ]
薬物動態学

PCPは水溶性と脂溶性の両方の性質を持つため、体内に速やかに分布する。[ 63 ] PCPはPCHP、PPC、PCAAに代謝される。この薬物は、肝臓における初回通過時に酸化的水酸化によって90%代謝される。代謝物はグルクロン酸抱合され、尿中に排泄される。摂取されたPCPの9%は未変化体として排泄される。[ 17 ]
喫煙すると、化合物の一部は熱によって1-フェニルシクロヘキセン(PC) とピペリジンに分解されます。
PCPの効果が現れるまでの時間は投与経路によって異なります。吸入した場合の作用発現は2~5分ですが、経口摂取した場合は15~60分かかる場合があります。[ 17 ]
化学
PCP はアリールシクロヘキシルアミンです。
類似品

1970年代から1980年代にかけて、主にアメリカ合衆国で、30種類未満のPCP類似体がストリートドラッグとして使用されていたと報告されています。 [ 48 ]これらの化合物のうち、ロリシクリジン(PCPy)、エチシクリジン(PCE)、テノシクリジン(TCP)など、広く使用されていたのはごくわずかです。[ 48 ]あまり一般的ではない類似体には、3-HO-PCP、3-MeO-PCMo、3-MeO-PCPなどがあります。
PCP様活性に必要な一般化された構造モチーフは、PCP誘導体の構造活性相関研究から導き出された。これらの誘導体はすべて、PCP自体と精神活性作用の一部を共有している可能性が高いが、個々の薬物とその置換基に応じて、様々な効力と、麻酔作用、解離作用、および覚醒作用の様々な組み合わせが知られている。米国では、これらの化合物はすべて、連邦類似物質法に基づきPCPの規制物質類似体とみなされ、したがって人体への消費目的で販売された場合は違法薬物となる。[ 73 ] [ 74 ]
歴史
フェンシクリジンは、1926年にアーサー・ケッツと彼の弟子パウル・メルケルによって、1-ピペリジノシクロヘキサンカルボニトリルのグリニャール反応の生成物として最初に発見されました。 [ 75 ]
1956年に化学者H・ビクター・マドックスによって再び合成され、現在はファイザーの子会社である製薬会社パーク・デイビスによって麻酔薬として市場に投入された。[ 71 ] [ 10 ] [ 76 ] [ 75 ] [ 77 ] 1965年に米国では副作用率の高さから人間への使用が禁止され、1978年には動物への使用が禁止された。[ 1 ] [ 10 ] [ 78 ]さらに、ケタミンが発見され、麻酔薬としての忍容性が高まった。[ 78 ]
PCPは米国ではスケジュールII薬物に分類されています。 [ 1 ] PCPの誘導体は娯楽目的や非医療目的で販売されています。[ 48 ]
社会と文化
規制
PCPは米国ではスケジュールII物質です。PCPの行政規制物質コード番号(ACSCN)は7471です。[ 79 ] 2014年の製造割当量は19グラム(0.67オンス)でした。[ 80 ]カナダでは規制薬物・物質法でスケジュールI、オランダではアヘン法でリストI 、英国ではクラスA物質に指定されています。[ 81 ]
使用頻度
PCPは1960年代にアメリカの主要都市で娯楽用薬物として登場し始めました。 [ 7 ] 1978年、『ピープル』誌とテレビニュース番組「60 Minutes 」のマイク・ウォレスは、PCPを「アメリカ最大の薬物問題」と呼びました。娯楽目的でのPCPの使用は比較的少なかったものの、1980年代に入ると大幅に減少し始めました。調査によると、PCPを少なくとも一度は試したことがあると認めた高校生の数は、1979年の13%から1990年には3%未満に減少しました。[ 18 ] : 46–49
文化的な描写
ジャン=ミシェル・バスキアは1982年の絵画『ダストヘッズ』で2人のエンジェルダスト使用者を描いた。[ 82 ]
北条司の1985年の漫画『シティーハンター』には、エンジェルダストという薬物が登場するが、これはおそらくPCPのストリートネームに由来すると思われる。2023年のアニメ映画『シティーハンター エンジェルダスト』では、エンジェルダストはより直接的にファンタジーの世界に足を踏み入れた。バイオテクノロジー企業が開発した、凶暴化させる性質を持つ超人兵士を生み出すためのSFナノマシン血清として描かれており、現実世界のPCPを回避している。[ 83 ]
1997年の映画『タイタニック』の撮影現場では、1日で80人以上のクルーが体調を崩しました。数時間にわたって多数の救急車が現場に到着し、映画業界のスタッフを次々と運び去りました。後に、誰かが残酷ないたずらをし、ロブスタービスクにPCPを混入したことが判明しました。犯人は特定されていません。
参考文献
- ^ a b c d e「PCP Fast Facts」 . justice.gov . National Drug Intelligence Center . 2003年. 2021年8月14日時点のオリジナルよりアーカイブ。 2018年2月19日閲覧。
- ^ a b Stobo JD, Traill TA, Hellmann DB, Ladenson PW, Petty BG (1996). 『医学の原理と実践』 McGraw Hill Professional. p. 933. ISBN 978-0-07-138365-3– Googleブックス経由。
乱用リスクが高い
- ^ a b c d Malenka RC, Nestler EJ, Hyman SE (2009). 「第15章 強化と嗜癖性障害」. Sydor A, Brown RY (編). 『分子神経薬理学:臨床神経科学の基礎』(第2版). ニューヨーク: McGraw-Hill Medical. pp. 374– 375. ISBN 978-0-07-148127-4。
- ^ a b c d e f g Giannini AJ (1998). 「第35章 フェンシクリジン」 . Tarter RE, Ammerman R, Ott PJ (編).薬物乱用ハンドブック:神経行動薬理学. ニューヨーク: Plenum Publishing Corporation . pp. 579– 587. ISBN 978-1-4757-2913-9。
- ^ a b c「 NIDA InfoFacts: 幻覚剤- LSD、ペヨーテ、シロシビン、PCP」 drugabuse.gov国立薬物乱用研究所2018年2月19日閲覧。
- ^ a b Riviello RJ (2010). 『法医救急医学マニュアル:臨床医のためのガイド』マサチューセッツ州サドベリー:ジョーンズ・アンド・バートレット出版社. pp. 41– 42. ISBN 978-0-7637-4462-5– Google ブックス経由。
- ^ a b c d e Bush DM (2013). 「フェンシクリジン(PCP)使用に伴う救急外来受診」CBHSQ報告書. ロックビル、メリーランド州:薬物乱用・精神保健サービス局. PMID 27656747.
PCPは敵対的な行動につながり、極端な暴力につながる可能性がある
。 - ^ a b c「幻覚剤」国立薬物乱用研究所2016年1月2018年2月20日閲覧。
- ^ a bマリオンNE、オリバーWM(2014年)『アメリカ社会における薬物:歴史、政治、文化、法の百科事典』 ABC-CLIO、p.732、ISBN 978-1-61069-596-1– Google ブックス経由。
- ^ a b c Zedeck BE, Zedeck MS (2007).法医学薬理学. Infobase Publishing. p. 97. ISBN 978-1-4381-0382-2。
- ^ "PCP" . ginad.org . 2018年9月10日時点のオリジナルよりアーカイブ。2018年2月20日閲覧。
- ^ "PCP" . cesar.umd.edu . 2010年3月12日時点のオリジナルよりアーカイブ。2018年2月20日閲覧。
- ^ 「幻覚剤」 . drugabuse.gov . 国立薬物乱用研究所. 2020年6月3日時点のオリジナルよりアーカイブ。 2018年2月20日閲覧。
- ^ Millan MJ, Brocco M, Gobert A, Joly F, Bervoets K, Rivet J, et al. (1999年12月). 「フェンサイクリジンとアンフェタミンの抗精神病薬に対する作用機序と感受性の対照:ラットにおけるPCP誘発性運動における側坐核5-HT2A受容体の重要性」.ヨーロッパ神経科学ジャーナル. 11 (12): 4419–32 . doi : 10.1046 / j.1460-9568.1999.00858.x . PMID 10594669. S2CID 43150509 .
- ^ a bディアス、ジェイミー. 薬物は行動にどのような影響を与えるか. イングルウッド・クリフス:プレンティス・ホール、1996年.
- ^ Chudler EM. 「子供のための神経科学 – PCP」 . Neuroscience for Kids . 2011年1月26日閲覧。
- ^ a b c d Bey T, Patel A (2007年2月). 「フェンシクリジン中毒と有害作用:違法薬物の臨床的・薬理学的レビュー」 .カリフォルニア救急医学ジャーナル. 8 (1): 9– 14. PMC 2859735. PMID 20440387 .
- ^ a b c dインシャルディ JA (1992)。麻薬戦争 II。メイフィールド出版社。ISBN 978-1-55934-016-8。
- ^ a b Morgan JP, Kagan D (1980年7月). 「アメリカの塵化:大衆メディアにおけるフェンシクリジン(PCP)のイメージ」Journal of Psychedelic Drugs . 12 ( 3–4 ): 195– 204. doi : 10.1080/02791072.1980.10471426 . PMID 7431414 .
- ^ Brecher M, Wang BW, Wong H, Morgan JP (1988年12月). 「フェンシクリジンと暴力:臨床的および法的問題」. Journal of Clinical Psychopharmacology . 8 (6): 397– 401. doi : 10.1097/ 00004714-198812000-00003 . PMID 3069880. S2CID 33659160 .
- ^ Wish ED (1986). 「PCPと犯罪:単なる違法薬物の一つか?」NIDA研究モノグラフ. 64 : 174–89 . PMID 3086733 .
- ^ Uchida M, Hida H, Mori K, Yoshimi A, Kitagaki S, Yamada K, et al. (2019年8月). 「フェンサイクリジン反復投与マウスにおける情緒および認知異常におけるグリア型グルタミン酸トランスポーター(GLAST)の機能的役割」 . Eur Neuropsychopharmacol . 29 (8): 918–24 . doi : 10.1016/j.euroneuro.2019.06.005 . PMID 31303267. S2CID 195887087 .
- ^ Luisada PV (1978年8月). Petersen RC, Stillman RC (編). 「フェンサイクリジン精神病:現象学と治療」(PDF) . NIDA研究モノグラフ(21).国立薬物乱用研究所: 241–253 . PMID 101872 .
- ^ Pender JW (1972年10月). 「解離性麻酔」 .カリフォルニア医学. 117 (4): 46– 47. PMC 1518731. PMID 18730832 .
- ^ Giannini AJ (1997). 『薬物乱用』(第2版)ロサンゼルス: Practice Management Information Corp. p. 126. ISBN 978-1-57066-053-5。
{{cite book}}: CS1 maint: 発行者の所在地 (リンク) - ^ Nestler EJ (2008年10月12日). 「レビュー. 依存症の転写メカニズム:DeltaFosBの役割」 . Philos. Trans. R. Soc. Lond. B Biol. Sci . 363 ( 1507): 3245– 3255. doi : 10.1098/rstb.2008.0067 . PMC 2607320. PMID 18640924 . Nestler EJ (2008年10月). 「表1:慢性投与後に側坐核でΔFosBを誘導することが知られている乱用薬物」 . Philos. Trans. R. Soc. Lond. B Biol. Sci . 363 ( 1507): 3245–55 . doi : 10.1098/rstb.2008.0067 . PMC 2607320. PMID 18640924 .
- ^野田雄一、鍋島毅(1998年9月)「フェンサイクリジン誘発性場所嫌悪および好意の神経メカニズム:条件付け場所嗜好課題における」実験・臨床薬理学の方法と知見20 ( 7): 607–11 . doi : 10.1358/mf.1998.20.7.485726 . PMID 9819806 .
- ^ Murrie B, Lappin J, Large M, Sara G (2020年4月). 「物質誘発性精神病、短期精神病、非定型精神病から統合失調症への移行:系統的レビューとメタアナリシス」 .統合失調症速報. 46 (3): 505– 516. doi : 10.1093/schbul/sbz102 . PMC 7147575. PMID 31618428 .
- ^ a b c d Bertron JL, Seto M, Lindsley CW (2018年10月). 「化学神経科学におけるDARK Classics: フェンシクリジン(PCP)」. ACS Chemical Neuroscience . 9 (10): 2459– 2474. doi : 10.1021/acschemneuro.8b00266 . PMID 29953199. S2CID 49603581 .
- ^ 「フライ・ファスト・ファクト」国立薬物情報センター。2021年4月17日時点のオリジナルよりアーカイブ。2017年1月15日閲覧。
- ^ a b c d Helman RS, Habal R (2008年10月6日). 「フェンシクリジンの毒性」 . eMedicine .2008年11月3日に取得。
- ^ a b c d Olmedo R (2002). 「第69章 フェンシクリジンとケタミン」ゴールドフランクLR、フロメンバウムNE、ルーウィンNA、ハウランドMA、ホフマンRS、ネルソンLS(編)『ゴールドフランクの毒性緊急事態』 ニューヨーク:マグロウヒルpp. 1034– 1041. ISBN 978-0-07-136001-2。
- ^ a b c Milhorn HT (1991年4月). 「フェンサイクリジン中毒の診断と管理」. American Family Physician . 43 (4): 1293–302 . PMID 2008817 .
- ^ Giannini AJ, Price WA (1985). 「PCP:急性中毒の管理」. Medical Times . 113 (9): 43–49 .
- ^ Giannini AJ, Eighan MS, Loiselle RH, Giannini MC (1984年4月). 「フェンサイクリジン精神病の治療におけるハロペリドールとクロルプロマジンの比較」. Journal of Clinical Pharmacology . 24 (4): 202–4 . doi : 10.1002 / j.1552-4604.1984.tb01831.x . PMID 6725621. S2CID 42278510 .
- ^ Roth BL、Driscol J. 「PDSP Kiデータベース」。向精神薬スクリーニングプログラム(PDSP)。ノースカロライナ大学チャペルヒル校および米国国立精神衛生研究所。2017年8月14日閲覧。
- ^ Berton JL, Seto M, Lindsley CW (2018年6月). 「化学神経科学におけるDARK Classics: フェンシクリジン(PCP)」. ACS Chem Neurosci . 9 (10): 2459– 2474. doi : 10.1021/acschemneuro.8b00266 . PMID 29953199 . S2CID 49603581 .
- ^ a b c d e f g h i j k l m n o p q r Roth BL, Gibbons S, Arunotayanun W, Huang XP, Setola V, Treble R, et al. (2013). 「ケタミン類似体メトキセタミンおよびフェンサイクリジンの3-および4-メトキシ類似体は、グルタミン酸NMDA受容体に対する高親和性かつ選択的なリガンドである」 . PLOS ONE . 8 (3) e59334. Bibcode : 2013PLoSO...859334R . doi : 10.1371/journal.pone.0059334 . PMC 3602154. PMID 23527166 .
- ^ a b c Rothman RB (1994). 「PCPサイト2:高親和性MK-801非感受性フェンサイクリジン結合部位」 . Neurotoxicol Teratol . 16 (4): 343– 53. Bibcode : 1994NTxT...16..343R . doi : 10.1016/0892-0362(94)90022-1 . PMID 7968938 .
- ^ Frohlich J, Van Horn JD (2014). 「統合失調症におけるケタミンモデルのレビュー」 . J. Psychopharmacol. (オックスフォード) . 28 (4): 287– 302. doi : 10.1177/0269881113512909 . PMC 4133098 . PMID 24257811 .
- ^ Seeman P, Guan HC (2008). 「フェンサイクリジンとグルタミン酸作動薬LY379268はドーパミンD2High受容体を刺激する:統合失調症におけるD2の基盤」Synapse . 62 (11): 819–28 . doi : 10.1002/syn.20561 . PMID 18720422 . S2CID 206519749 .
- ^ a b Kapur S, Seeman P (2002). 「NMDA受容体拮抗薬ケタミンとPCPはドーパミンD(2)受容体とセロトニン5-HT(2)受容体に直接作用する:統合失調症モデルへの示唆」 Mol . Psychiatry . 7 (8): 837–44 . doi : 10.1038/sj.mp.4001093 . PMID 12232776 .
- ^ a b c Seeman P, Guan HC, Hirbec H (2009). 「フェンシクリジン、リゼルグ酸ジエチルアミド、サルビノリンA、モダフィニルによるドーパミンD2High受容体の刺激」Synapse . 63 (8): 698– 704. doi : 10.1002/syn.20647 . PMID 19391150 . S2CID 17758902 .
- ^ Rabin RA, Doat M, Winter JC (2000). 「フェンサイクリジンの精神異常作用におけるセロトニン5-HT2A受容体の役割」 . Int. J. Neuropsychopharmacol . 3 (4) S1461145700002091: 333– 338. doi : 10.1017/S1461145700002091 . PMID 11343613 .
- ^ a b c d Goodman CB, Thomas DN, Pert A, Emilien B, Cadet JL, Carroll FI, et al. (1994). 「RTI-4793-14、モルモット脳の(+)-MK801非感受性[3H]1-]1-(2-チエニル)シクロヘキシル]ピペリジン結合部位(PCP部位2)に対する高親和性と選択性を有する新規リガンド」 Synapse . 16 ( 1): 59– 65. doi : 10.1002/syn.890160107 . PMID 8134901 . S2CID 19829696 .
- ^ Large CH, Bison S, Sartori I, Read KD, Gozzi A, Quarta D, et al. (2011年7月). 「ラットにおけるフェンサイクリジン誘発性認知機能障害の予防におけるナトリウムチャネル遮断薬の有効性:統合失調症の新規治療法への可能性」. The Journal of Pharmacology and Experimental Therapeutics . 338 (1): 100– 113. doi : 10.1124 / jpet.110.178475 . PMID 21487071. S2CID 1862326 .
- ^ Anis NA, Berry SC, Burton NR, D. Lodge (1983). 「解離性麻酔薬ケタミンとフェンサイクリジンは、N-メチルアスパラギン酸による哺乳類中枢ニューロンの興奮を選択的に減少させる」 . British Journal of Pharmacology . 79 (2): 565– 575. doi : 10.1111/j.1476-5381.1983.tb11031.x . PMC 2044888. PMID 6317114 .
- ^ a b c d Morris H, Wallach J (2014). 「PCPからMXEへ:解離性薬物の非医療的使用に関する包括的レビュー」. Drug Testing and Analysis . 6 ( 7–8 ): 614– 632. doi : 10.1002/dta.1620 . PMID 24678061 .
- ^ Caddy C, Giaroli G, White TP, Shergill SS, Tracy DK (2014年4月). 「グルタミン酸作動性抗うつ薬のプロトタイプとしてのケタミン:薬力学的作用、および有効性の系統的レビューとメタアナリシス」 . Therapeutic Advances in Psychopharmacology . 4 ( 2): 75– 99. doi : 10.1177/2045125313507739 . PMC 3952483. PMID 24688759 .
- ^ Klockgether T, Turski L, Schwarz M, Sontag KH, Lehmann J (1988年10月). 「新規非競合性N-メチル-D-アスパラギン酸(NMDA)拮抗薬チレタミンの逆説的けいれん作用」. Brain Research . 461 (2): 343–8 . doi : 10.1016 / 0006-8993(88)90265-X . PMID 2846121. S2CID 41671395 .
- ^ Burns JM, Boyer EW (2013). 「鎮咳薬と薬物乱用」 .薬物乱用とリハビリテーション. 4 : 75–82 . doi : 10.2147/SAR.S36761 . PMC 3931656. PMID 24648790 .
- ^ Aguayo LG, Warnick JE, Maayani S, Glick SD, Weinstein H, Albuquerque EX (1982年5月). 「フェンシクリジンの作用部位. IV. フェンシクリジンとその類似体の電気的興奮性膜のイオンチャネルおよびニコチン性受容体に対する相互作用:行動への影響」. Molecular Pharmacology . 21 (3): 637– 647. doi : 10.1016/S0026-895X(25)14927-4 . PMID 6287200 .
- ^ザラントネッロ P、ベッティーニ E、パイオ A、シモンチェッリ C、テレニ S、カルドゥッロ F (2011 年 4 月)。 「NMDA受容体アンタゴニストとしてのケタミンとフェンシクリジンの新規類似体」。生物有機および医薬化学に関するレター。21 (7): 2059–63 .土井: 10.1016/j.bmcl.2011.02.009。PMID 21334205。
- ^ Lin H, Vicini S, Hsu FC, Doshi S, Takano H, Coulter DA, et al. (2010年9月). 「軸索α7ニコチン性ACh受容体はシナプス前NMDA受容体の発現とグルタミン酸作動性シナプス前ボタンの構造可塑性を制御する」 . Proceedings of the National Academy of Sciences of the United States of America . 107 (38): 16661–6 . Bibcode : 2010PNAS..10716661L . doi : 10.1073/pnas.1007397107 . PMC 2944730. PMID 20817852 .
- ^ Fisher JL, Dani JA (2000年10月). 「海馬培養におけるニコチン性受容体はシナプスグルタミン酸電流を増加させ、NMDA受容体成分を減少させる」. Neuropharmacology . 39 ( 13): 2756–69 . doi : 10.1016/s0028-3908(00)00102-7 . PMID 11044745. S2CID 42066117 .
- ^ Prestori F, Bonardi C, Mapelli L, Lombardo P, Goselink R, De Stefano ME, et al. (2013). 「小脳入力段階におけるニコチン性アセチルコリン受容体による長期増強のゲーティング」 . PLOS ONE . 8 (5) e64828. Bibcode : 2013PLoSO...864828P . doi : 10.1371/journal.pone.0064828 . PMC 3669396. PMID 23741401 .
- ^ Seeman P, Ko F, Tallerico T (2005年9月). 「PCP、LSD、ケタミン精神異常薬の作用に対するドーパミン受容体の寄与」 .分子精神医学. 10 (9): 877– 883. doi : 10.1038/sj.mp.4001682 . PMID 15852061 .
- ^ Giannini AJ, Nageotte C, Loiselle RH, Malone DA, Price WA (1984). 「フェンサイクリジン精神病の治療におけるクロルプロマジン、ハロペリドール、ピモジドの比較:DA-2受容体の特異性」. Journal of Toxicology. Clinical Toxicology . 22 (6): 573–9 . doi : 10.3109/15563658408992586 . PMID 6535849 .
- ^ Rothman RB, Reid AA, Monn JA, Jacobson AE, Rice KC (1989年12月). 「精神異常誘発薬フェンサイクリジンはモルモット脳内の2つの高親和性結合部位を標識する:N-メチル-D-アスパラギン酸共役型およびドーパミン再取り込みキャリア関連フェンサイクリジン結合部位の証拠」. Molecular Pharmacology . 36 (6): 887– 896. doi : 10.1016/S0026-895X(25)09703-2 . PMID 2557536 .
- ^ Castellani S, Giannini AJ, Adams PM (1982). 「ラットにおけるフェンサイクリジン誘発行動に対するナロキソン、メテンケファリン、モルヒネの効果」Psychopharmacology . 78 ( 1): 76– 80. doi : 10.1007/BF00470593 . PMID 6815700. S2CID 21996319 .
- ^ 「フェンシクリジン」 www.drugbank.ca 2019年1月28日閲覧。
- ^ Martin D, Lodge D (1988年10月). 「フェンシクリジン受容体とN-メチル-D-アスパラギン酸拮抗作用:電気生理学的データと既知の行動との相関」.薬理学、生化学、行動. 31 (2): 279– 286. doi : 10.1016/0091-3057(88)90346-2 . PMID 2854262. S2CID 12247783 .
- ^ a b Kohrs R, Durieux ME (1998年11月). 「ケタミン:古い薬に新しい技を教える」 .麻酔と鎮痛. 87 (5): 1186– 1193. doi : 10.1097/00000539-199811000-00039 . PMID 9806706 .
- ^ Kroemer RT, Koutsilieri E, Hecht P, Liedl KR, Riederer P, Kornhuber J (1998年1月). 「フェンシクリジン結合部位におけるN-メチル-D-アスパラギン酸受容体の遮断に必要な構造の定量分析」. Journal of Medicinal Chemistry . 41 (3): 393– 400. doi : 10.1021/jm9704412 . PMID 9464369 .
- ^ Nadler V, Kloog Y, Sokolovsky M (1990年3月). 「非競合的遮断薬(フェンサイクリジン様薬物)のNMDA受容体への結合における特徴的な構造要件」. European Journal of Pharmacology . 188 ( 2–3 ): 97–104 . doi : 10.1016/0922-4106(90)90044-X . PMID 2156715 .
- ^ Olney JW, Labruyere J, Price MT (1989年6月). 「フェンサイクリジンおよび関連薬剤による大脳皮質ニューロンの病理学的変化」. Science . 244 (4910): 1360–1362 . Bibcode : 1989Sci...244.1360O . doi : 10.1126/science.2660263 . PMID 2660263 .
- ^ Hargreaves RJ, Hill RG, Iversen LL (1994). 「神経保護作用を持つNMDA拮抗薬:皮質神経形態への有害作用の可能性をめぐる論争」. Brain Edema IX . Acta Neurochirurgica. Supplementum. Vol. 60. pp. 15– 19. doi : 10.1007/978-3-7091-9334-1_4 . ISBN 978-3-7091-9336-5. PMID 7976530 .
- ^ヤンセン、カール『ケタミン:夢と現実』MAPS、2004年、 ISBN 0-9660019-7-4
- ^ Reynolds LM, Cochran SM, Morris BJ, Pratt JA, Reynolds GP (2005年3月). 「フェンサイクリジンの慢性投与はラット脳のN-アセチルアスパラギン酸およびN-アセチルアスパルチルグルタミン酸に統合失調症様変化を誘発する」.統合失調症研究. 73 ( 2–3 ): 147– 152. doi : 10.1016/j.schres.2004.02.003 . PMID 15653257. S2CID 1651693 .
- ^ Murray JB (2002年5月). 「フェンサイクリジン(PCP):危険な薬物だが、統合失調症研究には有用」. The Journal of Psychology . 136 (3): 319– 327. doi : 10.1080/00223980209604159 . PMID 12206280. S2CID 20334137 .
- ^ a b Lodge D, Mercier MS (2015年9月). 「ケタミンとフェンサイクリジン:良い点、悪い点、そして予想外の点」 . British Journal of Pharmacology . 172 (17): 4254– 4276. doi : 10.1111/bph.13222 . PMC 4556466. PMID 26075331 .
- ^ Javitt DC, Zukin SR, Heresco-Levy U, Umbricht D (2012年9月). 「天使が道を示してくれた?統合失調症のPCP/NMDAモデルの病因論的および治療的意義」 .統合失調症速報. 38 (5): 958– 966. doi : 10.1093/schbul/sbs069 . PMC 3446214. PMID 22987851 .
- ^ Itzhak Y, Kalir A, Weissman BA, Cohen S (1981年5月). 「フェンサイクリジン由来の新規鎮痛薬」. Journal of Medicinal Chemistry . 24 (5): 496–9 . doi : 10.1021/jm00137a004 . PMID 7241506 .
- ^ Chaudieu I, Vignon J, Chicheportiche M, Kamenka JM, Trouiller G, Chicheportiche R (1989年3月). 「PCP類似体によるフェンサイクリジン結合およびドーパミン取り込み阻害における芳香族基の役割」.薬理学生化学および行動. 32 (3): 699– 705. doi : 10.1016/0091-3057(89) 90020-8 . PMID 2544905. S2CID 7672918 .
- ^ a bコッツ A、メルケル P (1926 年 5 月)。 「Zur Kenntnis ヒドロアロマティッシャー アルカミン」。Journal für Praktische Chemie (ドイツ語)。113 (1): 49–76 .土井: 10.1002/prac.19261130107。ISSN 0021-8383。
- ^ Bunney Jr WE, Hippius H, Laakmann G, Schmauß M (2012). Neuropsychopharmacology: Proceedings of the XVIth CINP Congress, Munich, August, 15-19, 1988 . Springer Science & Business Media. p. 717. ISBN 978-3-642-74034-3– Google ブックス経由。
- ^ Lindgren JE, Holmstedt B (1983). 「生物学的試料中のフェンシクリジンおよびその代謝物の分析ガイド」.食品、医薬品、化学物質の使用、誤用、乱用における毒性学. 毒性学アーカイブ. 第6巻. ベルリン、ハイデルベルク: Springer Berlin Heidelberg. pp. 61– 73. doi : 10.1007/978-3-642-69083-9_10 . ISBN 978-3-540-12392-7. ISSN 0171-9750 . PMID 6578750 .
- ^ a b Tasman A, Kay J, Lieberman JA, First MB, Riba M (2015).精神医学, 2巻セット. John Wiley & Sons. p. 4943. ISBN 978-1-118-75336-1– Google ブックス経由。
- ^ 「規制物質」(PDF)deadiversion.usdoj.gov .米国麻薬取締局(Drug Enforcement Administration)2014年3月12日。2014年4月17日時点のオリジナルよりアーカイブ(PDF) 。 2014年6月15日閲覧。
- ^ 「スケジュールIおよびII規制物質の総生産割当量の設定と、リストI化学物質のエフェドリン、プソイドエフェドリン、フェニルプロパノールアミンの2014年における年間需要評価の設定」deadiversion.usdoj.gov。米国麻薬取締局。2013年8月30日。2014年4月17日時点のオリジナルよりアーカイブ。 2014年6月15日閲覧。
- ^ 「1971年薬物乱用防止法(修正)1979年命令」legislation.gov.uk。2016年1月31日閲覧。
- ^ Nag A (2013年4月11日). 「クリスティーズ・イブニングオークション、ジャン=ミシェル・バスキアの大作絵画を出品」 .エコノミック・タイムズ. 2020年9月26日閲覧。
- ^ 「新作アニメ『シティーハンター』予告編でキャスト、主題歌、9月8日公開が明らかに」 Anime News Network . 2024年6月28日. 2024年6月28日閲覧。
外部リンク
- Erowid.org – PCP情報
- 国立薬物乱用研究所 InfoFacts: PCP (フェンサイクリジン) 2012年1月6日アーカイブ- Wayback Machine
- フェンシクリジンに関する薬物と人間のパフォーマンスに関するファクトシート
- フェンシクリジンとケタミン:ストリートからの視点 - PCPの使用と効果に関する1981年の記事。 2019年1月21日にWayback Machineにアーカイブ。
- 「フェンシクリジン」 .薬物情報ポータル. 米国国立医学図書館. 2021年5月7日時点のオリジナルよりアーカイブ。

