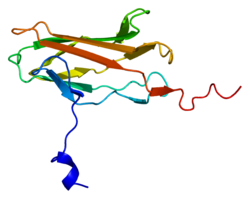
ランクス2

RUNX2(Runt関連転写因子2 )は、コア結合因子サブユニットα-1(CBF-α-1)としても知られ、ヒトではRUNX2遺伝子によってコードされるタンパク質です。RUNX2は、骨芽細胞の分化に関連する重要な転写因子です。
Runx2 は、骨芽細胞および内皮細胞において、細胞周期の開始と終了において細胞増殖を調節する役割を果たしていることも示唆されている。Runx2 は、 G1 期での細胞周期進行に影響を及ぼすことによって、前骨芽細胞の増殖を抑制する。[ 6 ]骨芽細胞では、 Runx2 のレベルはG1期で最高であり、 S 期、G2期、およびM 期で最低である。[ 5 ] Runx2 が果たす包括的な細胞周期調節メカニズムはまだ不明であるが、細胞周期全体にわたる Runx2 の活性とレベルの変化が、細胞周期の開始と終了、および細胞周期の進行に寄与することは一般的に認められている。これらの機能は、異常な細胞増殖制御に起因する可能性がある骨癌、特に骨肉腫の発生について議論する際に特に重要である。
関数
骨芽細胞の分化
このタンパク質は転写因子RUNXファミリーに属し、Runt DNA結合ドメインを有する。骨芽細胞の分化と骨格形成に必須である。骨格遺伝子発現に関与する核酸および調節因子の足場として機能する。このタンパク質は単量体として、あるいはより親和性の高いヘテロ二量体複合体のサブユニットとしてDNAに結合することができる。異なるタンパク質アイソフォームをコードする遺伝子の転写バリアントは、代替プロモーターおよび選択的スプライシングの利用によって生じる。
Runx2タンパク質の細胞内動態も、適切な骨芽細胞分化に重要です。Runx2タンパク質は前骨芽細胞で検出され、その発現は未熟骨芽細胞では亢進し、成熟骨芽細胞では低下します。Runx2は骨芽細胞への分化決定に必要な最初の転写因子であり、次いでSp7とWntシグナル伝達が重要です。Runx2は、多能性間葉系細胞から未熟骨芽細胞への分化を誘導するとともに、骨芽細胞分化を維持するいくつかの重要な下流タンパク質と骨マトリックス遺伝子の発現を活性化します。
DNA結合活性のノックアウトは骨芽細胞への分化を阻害する。このため、Runx2はしばしば骨のマスターレギュレーターと呼ばれる。[ 7 ]
細胞周期の調節
Runx2は骨芽細胞分化のマスターレギュレーターであることに加え、細胞周期制御においても複数の役割を果たすことが示されています。これは、Runx2がc-MybやC/EBP [ 5 ]、p53 [ 7 ]といった多くの細胞増殖遺伝子と転写レベルで相互作用するという事実に一部起因しています。これらの機能は骨芽細胞の増殖と維持に極めて重要です。これは、細胞周期全体を通してRunx2の分解と転写活性の制御による変動レベルを介して制御されることが多いです。
細胞内のRunx2レベルの変動は、細胞周期のダイナミクスに寄与しています。MC3T3 -E1骨芽細胞株では、Runx2レベルはG1期に最大となり、G2期、S期、有糸分裂期に最小となります。[ 5 ]さらに、Runx2の変動はG1期関連の抗増殖機能にも寄与しています。[ 8 ]また、Runx2レベルの低下は、増殖・分化中の骨芽細胞の細胞周期からの離脱につながり、Runx2はこのメカニズムを介して骨芽細胞の最終段階を媒介する役割を果たしているという説もあります。[ 9 ]現在の研究では、Runx2レベルが様々な機能を果たしていると仮定されています。
さらに、Runx2は、直接的なタンパク質リン酸化を介して細胞周期依存的なダイナミクスを促進するいくつかのキナーゼと相互作用することが示されている。さらに、Runx2は造血細胞においてサイクリンD2、D3、およびCDK阻害因子p21(cip1)の遺伝子発現を制御する。分子レベルでは、Runxは有糸分裂中にcdc2のパートナーであるサイクリンB1と会合することが示されている。[ 10 ] Runx2のリン酸化状態は、DNA結合活性にも影響する。Runx2のDNA結合活性は細胞増殖と相関しており、これはRunx2のリン酸化がRunx2を介した細胞増殖および細胞周期制御にも関連している可能性を示唆している。これを裏付けるように、Runxはcdc2キナーゼによってSer451でリン酸化され、G2期およびM期の制御を介して細胞周期の進行を促進することが指摘されている。[ 10 ]

病理学
鎖骨頭蓋異形成症
Runx2の変異は、鎖骨頭蓋骨異骨症という疾患と関連しています。ある研究では、この表現型はRunx2の発現量不足が一因であると提唱されています。Runx2は細胞周期からの離脱を促進するため、Runx2の発現量不足は、鎖骨頭蓋骨異骨症患者に観察される骨芽細胞の増殖増加と関連しています。[ 11 ]
骨肉腫
Runx2 の変異体は骨肉腫の表現型と関連付けられている。[ 5 ]現在の研究では、これは部分的に Runx2 が細胞周期を緩和する役割を果たしているためであると示唆されている。[ 6 ] Runx2 は、 G1で細胞周期の進行を停止することにより、骨芽細胞の腫瘍抑制因子としての役割を果たしている。[ 5 ]正常な骨芽細胞株 MC3T3-E1 と比較すると、骨肉腫 ROS および SaOS 細胞株の Runx2 の振動は、正常な骨芽細胞の Runx2 レベルの振動と比較すると異常であり、これは Runx2 レベルの調節異常が細胞周期から逃れることができず異常な細胞増殖に寄与していることを示唆している。分子論的には、 MG132によるプロテアソーム阻害はMC3T3細胞のG1後期およびS期のRunx2タンパク質レベルを安定化できるが、骨肉腫細胞では安定化できず、結果として癌性の表現型につながると提案されている。[ 6 ] [ 5 ]
調節と補因子
Runx2 は骨芽細胞分化のマスター転写因子としての役割を担っているため、その調節は細胞内の他のプロセスと複雑に関連しています。
Twist、Mshホメオボックス2(Msx2)、および前骨髄球性白血病ジンクフィンガータンパク質(PLZF)はRunx2の上流で作用します。Osterix (Osx)はRunx2の下流で作用し、正常な骨芽細胞分化のマーカーとして機能します。ジンクフィンガータンパク質521(ZFP521)と活性化転写因子4(ATF4)はRunx2の補因子です。[ 12 ]転写共調節因子であるWWTR1(TAZ)がRunx2に結合すると、転写が促進されます。
さらに、増殖中の軟骨細胞では、Runx2は細胞周期の一部としてCyclinD1/CDK4によって阻害される。 [ 13 ]
相互作用
RUNX2 は以下と相互作用することが示されています。
- AR [ 14 ]
- ER-α [ 15 ]
- C-Fos、[ 16 ] [ 17 ]
- C-jun、[ 16 ] [ 17 ]
- HDAC3 , [ 18 ]
- MYST4 , [ 19 ]
- SMAD1 [ 20 ] [ 21 ]
- SMAD3、[ 20 ] [ 21 ]および
- スタブ1 . [ 22 ]
そして
miR-133とCyclinD1/CDK4はRunx2を直接阻害する。[ 24 ] [ 13 ]
参照
参考文献
- ^ a b c GRCh38: Ensemblリリース89: ENSG00000124813 – Ensembl、2017年5月
- ^ a b c GRCm38: Ensemblリリース89: ENSMUSG00000039153 – Ensembl、2017年5月
- ^ 「ヒトPubMedリファレンス:」。米国国立医学図書館、国立生物工学情報センター。
- ^ 「マウスPubMedリファレンス:」。米国国立医学図書館、国立生物工学情報センター。
- ^ a b c d e f g San Martin IA、Varela N、Gaete M、Villegas K、Osorio M、Tapia JC、他。 (2009 年 12 月)。「骨肉腫細胞における骨芽細胞関連ヘテロ二量体転写因子Runx2-Cbfbetaの細胞周期制御の障害」。細胞生理学ジャーナル。221 (3): 560–71 .土井: 10.1002/jcp.21894。PMC 3066433。PMID 19739101。
- ^ a b c Lucero CM, Vega OA, Osorio MM, Tapia JC, Antonelli M, Stein GS, et al. (2013年4月). 「がん関連転写因子Runx2はヒト骨肉腫細胞株における細胞増殖を制御する」 . Journal of Cellular Physiology . 228 (4): 714–23 . doi : 10.1002 / jcp.24218 . PMC 3593672. PMID 22949168 .
- ^ a b Wysokinski D, Pawlowska E, Blasiak J (2015年5月). 「RUNX2:DNA損傷応答に関与する可能性のある骨成長制御因子」. DNA and Cell Biology . 34 (5): 305–15 . doi : 10.1089/dna.2014.2688 . PMID 25555110 .
- ^ Galindo M, Pratap J, Young DW, Hovhannisyan H, Im HJ, Choi JY, et al. (2005年5月). 「Runx2の骨特異的発現は細胞周期中に振動し、骨芽細胞におけるG1期関連の抗増殖機能をサポートする」 . The Journal of Biological Chemistry . 280 (21): 20274–85 . doi : 10.1074/jbc.M413665200 . PMC 2895256. PMID 15781466 .
- ^ Pratap J, Galindo M, Zaidi SK, Vradii D, Bhat BM, Robinson JA, et al. (2003年9月). 「前骨芽細胞の増殖拡大におけるRunx2の細胞増殖制御役割」. Cancer Research . 63 (17): 5357–62 . PMID 14500368 .
- ^ a b Qiao M, Shapiro P, Fosbrink M, Rus H, Kumar R, Passaniti A (2006年3月). 「cdc2によるRUNX2転写因子の細胞周期依存性リン酸化は内皮細胞の増殖を制御する」 . The Journal of Biological Chemistry . 281 (11): 7118–28 . doi : 10.1074/jbc.M508162200 . PMID 16407259 .
- ^ Lou Y, Javed A, Hussain S, Colby J, Frederick D, Pratap J, et al. (2009年2月). 「鎖骨頭蓋異形成症の表現型におけるRunx2閾値」 . Human Molecular Genetics . 18 (3): 556–68 . doi : 10.1093 / hmg/ddn383 . PMC 2638795. PMID 19028669 .
- ^ジンキンス JR (1987)。 「大容量全円柱状腰椎脊髄造影」。神経放射線学。29 (4): 371–373 .土井: 10.1007/bf00348917。PMID 3627420。S2CID 20760228。
- ^ a b Berti M, Buso G, Colautti P, Moschini G, Stlevano BM, Tregnaghi C (1977年8月). 「プロトン誘起X線発光法による血清中のセレンの定量」.分析化学. 49 (9): 1313–5 . Bibcode : 1977AnaCh..49.1313B . doi : 10.1021/ac50017a008 . PMID 883617 .
- ^ Baniwal SK, Khalid O, Sir D, Buchanan G, Coetzee GA, Frenkel B (2009年8月). 「骨芽細胞および前立腺癌細胞におけるアンドロゲン受容体(AR)によるRunx2の抑制:ARはRunx2に結合し、DNAへのリクルートを阻害する」 . Molecular Endocrinology . 23 (8): 1203–14 . doi : 10.1210 / me.2008-0470 . PMC 2718746. PMID 19389811 .
- ^ Khalid O, Baniwal SK, Purcell DJ, Leclerc N, Gabet Y, Stallcup MR, et al. (2008年12月). 「エストロゲン受容体αによるRunx2活性の調節:骨粗鬆症および乳がんへの影響」 .内分泌学. 149 (12): 5984–95 . doi : 10.1210 / en.2008-0680 . PMC 2613062. PMID 18755791 .
- ^ a b Hess J, Porte D, Munz C, Angel P (2001年6月). 「AP-1とCbfa/runtは物理的に相互作用し、骨芽細胞における副甲状腺ホルモン依存性MMP13の発現を、新規骨芽細胞特異的エレメント2/AP-1複合エレメントを介して制御する」 . The Journal of Biological Chemistry . 276 (23): 20029–38 . doi : 10.1074/jbc.M010601200 . PMID 11274169 .
- ^ a b D'Alonzo RC, Selvamurugan N, Karsenty G, Partridge NC (2002年1月). 「コラーゲナーゼ3プロモーター活性化における活性化タンパク質1因子c-Fosおよびc-JunとCbfa1の物理的相互作用」 . The Journal of Biological Chemistry . 277 (1): 816–22 . doi : 10.1074/jbc.M107082200 . PMID 11641401 .
- ^ Schroeder TM, Kahler RA, Li X, Westendorf JJ (2004年10月). 「ヒストン脱アセチル化酵素3はrunx2と相互作用してオステオカルシンプロモーターを抑制し、骨芽細胞分化を制御する」 . The Journal of Biological Chemistry . 279 (40): 41998– 2007. doi : 10.1074/jbc.M403702200 . PMID 15292260 .
- ^ Pelletier N, Champagne N, Stifani S, Yang XJ (2002年4月). 「MOZおよびMORFヒストンアセチルトランスフェラーゼはRuntドメイン転写因子Runx2と相互作用する」. Oncogene . 21 (17): 2729–40 . doi : 10.1038/sj.onc.1205367 . PMID 11965546 .
- ^ a b Zhang YW, Yasui N, Ito K, Huang G, Fujii M, Hanai J, et al. (2000年9月). 「RUNX2/PEBP2alpha A/CBFA1変異は鎖骨頭蓋骨異形成症におけるトランス活性化とSmad相互作用を阻害する」 . Proceedings of the National Academy of Sciences of the United States of America . 97 (19): 10549–54 . Bibcode : 2000PNAS...9710549Z . doi : 10.1073 / pnas.180309597 . PMC 27062. PMID 10962029 .
- ^ a b Hanai J, Chen LF, Kanno T, Ohtani-Fujita N, Kim WY, Guo WH, et al. (1999年10月). 「PEBP2/CBFとSmadの相互作用および機能的協力。免疫グロブリン生殖細胞系列Calphaプロモーターの相乗的誘導」 . The Journal of Biological Chemistry . 274 (44): 31577–82 . doi : 10.1074/jbc.274.44.31577 . PMID 10531362 .
- ^ Li X, Huang M, Zheng H, Wang Y, Ren F, Shang Y, et al. (2008年6月). 「CHIPはRunx2の分解を促進し、骨芽細胞分化を負に制御する」 . The Journal of Cell Biology . 181 (6): 959–72 . doi : 10.1083/jcb.200711044 . PMC 2426947. PMID 18541707 .
- ^高畑裕也、萩野博、木村亜、漆崎真、小林S、若森一、他(2021年10月)。「Smoc1 と Smoc2 は Runx2 の下流分子として骨形成を制御します。 」コミュニケーション生物学。4 (1199) 1199.土井: 10.1038/s42003-021-02717-7。PMC 8526618。PMID 34667264。
- ^ Li Z, Hassan MQ, Volinia S, van Wijnen AJ, Stein JL, Croce CM, 他 (2008年9月). 「BMP2誘導性骨芽細胞系譜コミットメントプログラムにおけるマイクロRNAシグネチャー」 . Proceedings of the National Academy of Sciences of the United States of America . 105 (37): 13906–11 . Bibcode : 2008PNAS..10513906L . doi : 10.1073 / pnas.0804438105 . PMC 2544552. PMID 18784367 .
さらに読む
- Otto F, Kanegane H, Mundlos S (2002年3月). 「鎖骨頭蓋異形成症患者におけるRUNX2遺伝子の変異」 . Human Mutation . 19 (3): 209–16 . doi : 10.1002/humu.10043 . PMID 11857736. S2CID 2578591 .
- 小森 剛志 (2002年3月). 「骨芽細胞分化制御に必須な転写因子Cbfa1/Runx2」.日本臨床. 日本臨床医学会誌. 60 (Suppl 3): 91–7 . PMID 11979975 .
- Stock M, Otto F (2005年6月) . 「RUNX2アイソフォーム発現の制御:プロモーターとエンハンサーの役割」. Journal of Cellular Biochemistry . 95 (3): 506–17 . doi : 10.1002/jcb.20471 . PMID 15838892. S2CID 29657025 .
- Blyth K, Cameron ER, Neil JC (2005年5月). 「RUNX遺伝子:がんにおける機能獲得または喪失」. Nature Reviews. Cancer . 5 (5): 376–87 . doi : 10.1038/nrc1607 . PMID 15864279. S2CID 335980 .
- Schroeder TM, Jensen ED, Westendorf JJ (2005年9月). 「Runx2:発達期および成熟期の骨芽細胞における遺伝子転写のマスターオーガナイザー」 .出生異常研究. パートC, Embryo Today . 75 (3): 213–25 . doi : 10.1002/bdrc.20043 . PMID 16187316 .
- Frenkel B, Hong A, Baniwal SK, Coetzee GA, Ohlsson C, Khalid O, et al. (2010年8月). 「性ステロイドによる成人の骨代謝調節」 . Journal of Cellular Physiology . 224 (2): 305–10 . doi : 10.1002/jcp.22159 . PMC 5770230. PMID 20432458 .
外部リンク
- GeneReviews/NCBI/NIH/UWの鎖骨頭蓋異形成症に関するエントリ
- 米国国立医学図書館の医学主題標目表(MeSH)におけるRunx2+タンパク質