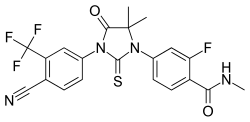
エンザルタミド
 | |
| 臨床データ | |
|---|---|
| 商号 | ザンディ |
| その他の名前 | MDV-3100; ASP-9785 |
| AHFS / Drugs.com | モノグラフ |
| メドラインプラス | a612033 |
| ライセンスデータ | |
| 妊娠カテゴリー |
|
| 投与経路 | 経口摂取[ 2 ] [ 3 ] |
| 薬物クラス | 非ステロイド性抗アンドロゲン |
| ATCコード | |
| 法的地位 | |
| 法的地位 | |
| 薬物動態データ | |
| バイオアベイラビリティ | ラット:89.7% [ 8 ]ヒト:不明(ただし、排泄物からの回収に基づくと少なくとも84.6%)[ 9 ] [ 3 ] |
| タンパク質結合 | エンザルタミド:97~98%(主にアルブミンに対して)[ 2 ] NDME:95%[ 2 ] |
| 代謝 | 肝臓(主にCYP2C8とCYP3A4)[ 2 ] |
| 代謝物 | • NDMEツールチップ N-デスメチレンザルタミド(活性)[ 2 ] [ 3 ] • カルボン酸誘導体代謝物(不活性)[ 3 ] |
| 消失半減期 | エンザルタミド:5.8日(範囲2.8~10.2日)[ 2 ] NDME:7.8~8.6日[ 2 ] |
| 排泄 | 尿:71.0% [ 3 ]胆汁:13.6% [ 3 ]便:0.39% [ 3 ] |
| 識別子 | |
| |
| CAS番号 | |
| PubChem CID | |
| IUPHAR/BPS | |
| ドラッグバンク | |
| ケムスパイダー | |
| ユニイ | |
| ケッグ | |
| チェビ |
|
| チェムブル | |
| CompToxダッシュボード(EPA) | |
| ECHA 情報カード | 100.231.722 |
| 化学および物理データ | |
| 式 | C 21 H 16 F 4 N 4 O 2 S |
| モル質量 | 464.44 g·mol −1 |
| 3Dモデル(JSmol) | |
| |
| |
エンザルタミドは、 Xtandiというブランド名で販売されており、前立腺がんの治療に使用される非ステロイド性抗アンドロゲン( NSAA)薬です。[ 2 ] [ 10 ]転移性去勢抵抗性前立腺がん(mCRPC)[ 2 ] 、非転移性去勢抵抗性前立腺がん[ 2 ]、転移性去勢感受性前立腺がん(mCSPC)[ 11 ]の治療において、去勢と併用して使用されます。 [ 2 ]経口投与されます。
去勢手術にエンザルタミドを追加した場合の副作用には、無力症、腰痛、下痢、関節痛、ほてりなどがあります。[ 2 ]まれに、発作を引き起こす可能性があります。[ 2 ]薬物相互作用の可能性が高いです。[ 2 ]エンザルタミドは抗アンドロゲン薬であり、テストステロンやジヒドロテストステロンなどのアンドロゲンの生物学的標的であるアンドロゲン受容体の拮抗薬として作用します。[ 2 ]そうすることで、前立腺や体の他の部分でこれらのホルモンの作用を阻害します。 [ 2 ]
エンザルタミドは2006年に初めて記載され、2012年に前立腺癌の治療薬として導入されました。[ 12 ] [ 13 ] [ 14 ]これは導入された最初の第二世代NSAAでした。 [ 15 ]エンザルタミドは、世界保健機関の必須医薬品リストに掲載されている治療代替薬です。[ 16 ]
医療用途
エンザルタミドは、去勢抵抗性前立腺がん、転移性去勢感受性前立腺がん、および転移リスクの高い生化学的再発を伴う非転移性去勢感受性前立腺がんの治療に適応があります。 [ 2 ]
前立腺がん
エンザルタミドは、特にPSA倍加時間が6ヶ月以下の高リスク非転移性去勢抵抗性前立腺がん患者において、全生存率を延長させる効果的な治療法であるという十分な証拠がある。 [ 17 ]
その他の用途
エンザルタミドは、トランスジェンダー女性の女性化ホルモン療法における抗アンドロゲンとして使用することができる。[ 18 ] [ 19 ]
利用可能なフォーム
エンザルタミドはカプセルまたは錠剤として提供されます。[ 2 ]
禁忌
エンザルタミドは妊娠中の女性には禁忌である。[ 2 ]胎児に害を及ぼす可能性がある。[ 2 ]
副作用
臨床試験で確認されたエンザルタミドの主な副作用には、女性化乳房、乳房の痛みや圧痛、疲労、下痢、ほてり、頭痛、性機能障害、そして頻度は低いものの発作などがある。[ 20 ] [ 21 ] [ 22 ] [ 23 ]臨床試験で報告されたその他の「一般的な」副作用には、好中球減少症、幻視、不安、認知障害、記憶障害、高血圧、皮膚の乾燥、掻痒などがある。[ 24 ]エンザルタミド単独療法は、性機能と性行為に中程度の悪影響を与えると考えられており、GnRHアナログよりも大幅に少ないが、ビカルタミドなどの他のNSAAと同程度である。[ 25 ]
中枢性副作用
臨床試験では、エンザルタミドを投与された患者の約1%に発作が認められている。[ 20 ] [ 22 ]これは、エンザルタミドが血液脳関門を通過し、 [ 26 ] [ 27 ]中枢神経系のGABA A受容体にオフターゲット結合して阻害するためと考えられている(試験管内試験ではGABA A受容体を阻害することが分かっている(IC 50ツールチップの半最大阻害濃度エンザルタミドは、GABA A受容体に対する GABA A 受容体阻害薬として知られています(例えば、エンザルタミドは、GABA A 受容体に対する GABA A 受容体阻害薬として知られています(例えば、エンザルタミドは、GABA A 受容体に対する GABA A 受容体阻害薬として知られています)。[ 29 ] [ 30 ] [31] エンザルタミドは、GABA A受容体に対するGABA A受容体阻害薬として知られています(例えば、エンザルタミドは、GABA A 受容体に対する GABA A 受容体阻害薬として知られています)。[20] [ 22 ]発作に加えて、臨床試験でエンザルタミド投与時に観察された他の GABA A 受容体関連の副作用としては、不安、不眠、めまい、知覚異常、頭痛などがあります。[30] 発作閾値を下げる能力があるため、発作性疾患や脳損傷の既往歴がある患者は、エンザルタミド投与中は注意深く監視する必要があります。[ 31 ] NSAA誘発性発作はベンゾジアゼピン治療に反応し、エンザルタミドによる GABA A受容体阻害はこれらの薬剤で治療できることが示唆されています。 [ 28 ]用量範囲試験では、エンザルタミド 240 mg/日以上の用量で重度の疲労が観察されました。 [ 32 ] [ 33 ]
まれな副作用
エンザルタミド治療による可逆性後脳症症候群(PRES)の症例報告が1件ある。[ 34 ]この副作用の作用機序は不明であるが、エンザルタミドによるGABAA受容体の阻害の結果であると提案されている。[ 34 ]
過剰摂取
エンザルタミドは過剰摂取すると発作を引き起こす可能性がある。[ 2 ]
相互作用
エンザルタミドは、 CYP3A4、CYP2C9、CYP2C19を含む複数のシトクロムP450酵素の中程度から強力な誘導剤であるため、臨床的に関連する薬物相互作用を引き起こす可能性が高い。[ 2 ]エンザルタミドの血中濃度は、 CYP2C8およびCYP3A4の阻害剤や誘導剤によって変化する可能性があるため、可能な限り避けるべきである。[ 35 ]
ERに対するエンザルタミドの臨床試験ではツールチップのエストロゲン受容体女性の乳がん患者において、エンザルタミドはアロマターゼ阻害剤アナストロゾールとエキセメスタンの血清濃度をそれぞれ90%と50%低下させ、その効果を減弱させる可能性があることが判明した。 [ 36 ]
薬理学
薬力学
エンザルタミドは、テストステロンやジヒドロテストステロン(DHT)などのアンドロゲンの生物学的標的であるアンドロゲン受容体(AR)の選択的サイレントアンタゴニストとして作用します。第一世代のNSAAであるビカルタミドとは異なり、エンザルタミドはARの細胞核への移行を促進せず、さらにARとデオキシリボ核酸(DNA)の結合、およびARとコアクチベータータンパク質の結合を阻害します。[ 37 ]そのため、エンザルタミドはアンタゴニストであるだけでなく、ARシグナル伝達阻害剤としても知られています。[ 20 ]この薬剤は、フルタミドやビカルタミドなどのいわゆる「第一世代」NSAAと比較して、抗アンドロゲン剤としての効力が大幅に向上しているため、「第二世代」NSAAと呼ばれています。この薬剤のARに対する親和性は、前立腺におけるARの内因性リガンドであるDHTのわずか2倍です。[ 38 ]
進行性前立腺がん患者に見られるように、高レベルのARを発現するように設計されたLNCaP細胞(前立腺がん細胞株)をエンザルタミドで処理すると、アンドロゲン依存性遺伝子PSAおよびTMPRSS2の発現は、発現がアップレギュレーションされたビカルタミドとは対照的に、ダウンレギュレーションされた。[ 37 ] ARを過剰発現するVCaP細胞では、エンザルタミドはアポトーシスを誘導したが、ビカルタミドは誘導しなかった。[ 37 ]さらに、エンザルタミドはW741C変異体ARのアンタゴニストとして作用するが、W741C変異体に結合した場合、純粋なアゴニストとして作用するビカルタミドとは対照的である。[ 37 ]
前立腺癌患者におけるエンザルタミドの用量範囲試験が実施されている。 [ 33 ]
ホルモンレベルの変化
エンザルタミド単独療法を1日160 mg投与すると、血中テストステロン濃度が114.3%、ジヒドロテストステロン(DHT)濃度が51.7%、エストラジオール濃度が71.7%、性ホルモン結合グロブリン(SHBG)濃度が100.6%、デヒドロエピアンドロステロン(DHEA)濃度が9.6%、アンドロステンジオン濃度が51.1%、黄体形成ホルモン(LH)濃度が184.7%、卵胞刺激ホルモン(FSH)濃度が47.0%、プロラクチン濃度が16.8%上昇することが分かっています。[ 25 ] [ 39 ]これらのホルモン濃度の変化は、高用量ビカルタミド単独療法での変化と同様です。[ 25 ] [ 39 ]前立腺特異抗原(PSA)レベルの最大減少率の中央値は99.6%であった。[ 25 ]
他の抗アンドロゲンとの比較
エンザルタミドはビカルタミドと比較してアンドロゲン受容体(AR)に対する結合親和性が約8倍高い。[ 37 ] [ 40 ]ある研究では、IC 50ツールチップの半最大阻害濃度LNCaP細胞株のARにおけるエンザルタミドのIC 50値は21 nM、ビカルタミドのIC 50値は160 nM(7.6倍の差)であった[ 41 ] 。一方、別の研究では、IC 50値はそれぞれ36 nMと159 nM(4.4倍の差)であった[ 42 ] 。それに応じて、臨床所見は、エンザルタミドが、ビカルタミド、フルタミド、ニルタミドなどの第一世代NSAAと比較して、はるかに強力で効果的な抗アンドロゲンであることを示唆している。[ 25 ] [ 39 ]また、第一世代NSAAとは異なり、臨床試験ではエンザルタミド治療に関連した肝毒性や肝酵素の上昇の証拠は得られていない。 [ 43 ] [ 44 ]
前立腺がんにおける耐性メカニズム
エンザルタミドは一定期間のみ有効であり、その後は癌の増殖を抑制できなくなります。エンザルタミドに対する耐性のメカニズムについては、現在精力的に研究されています。[ 45 ]現在、いくつかのメカニズムが発見されています。
- AR変異[ 46 ] [ 47 ]
- ARスプライスバリアント[ 48 ]
- グルココルチコイド受容体バイパス[ 49 ]
- 解糖系のフラックスの増加[ 50 ]
- オートファジーを介した耐性[ 51 ]
- Wntシグナル伝達の活性化[ 52 ]
- AKR1C3酵素を介した腫瘍内アンドロゲン生合成の増加[ 53 ]
- インターロイキン6シグナル伝達を介した耐性[ 54 ]
シトクロムP450の調節
エンザルタミドは、 CYP3A4酵素の強力な誘導剤であり、 CYP2C9およびCYP2C19の中程度の誘導剤であると報告されており、これらの酵素によって代謝される薬物の循環濃度に影響を及ぼす可能性がある。[ 55 ] [ 35 ]
薬物動態学
エンザルタミドのヒトにおける生物学的利用能は不明であるが、排泄試験において尿および胆汁から回収された量に基づくと少なくとも 84.6% である。 [ 9 ] [ 3 ]同様に、ラットにおけるエンザルタミドの生物学的利用能は 89.7% である。[ 8 ]エンザルタミドの定常状態濃度は、治療開始後 28 日以内に達成される。[ 41 ]エンザルタミドの血漿タンパク質結合率は97~98% であるが、主な代謝物であるN-デスメチルエンザルタミド(NDME)のそれは95% である。[ 2 ]エンザルタミドは主にアルブミンに結合します。[ 2 ]この薬は肝臓で主にシトクロム P450酵素CYP2C8およびCYP3A4によって代謝されます。[ 2 ] [ 35 ]エンザルタミドの消失半減期は平均5.8日と長く、範囲は2.8~10.2日です。[ 2 ] NDMEの消失半減期はさらに長く、約7.8~8.6日です。[ 2 ]エンザルタミドは尿中に71.0% 、胆汁中に13.6% 、糞便中に0.39%が排泄されます。[ 3 ]
化学
エンザルタミドは合成ジアリールチオヒダントイン誘導体であり、構造的にはフルタミド、ニルタミド、ビカルタミドなどの以前の第一世代NSAA、およびアパルタミドやプロキサルタミドなどの新しい第二世代NSAAに関連しています。[ 56 ]
歴史
エンザルタミドは、カリフォルニア大学ロサンゼルス校のチャールズ・ソーヤーズとマイケル・ユングによって発見されました。[ 57 ] [ 58 ] [ 59 ]彼らと同僚は、ニルタミドの類似体であるRU-59063のチオヒダントイン誘導体約200種を合成し、ヒト前立腺癌細胞でのAR拮抗作用を評価し、エンザルタミドとRD-162をリード化合物として特定しました。[ 37 ] [ 59 ]これらの化合物は2006年に特許を取得し、2007年に説明されました。[ 12 ]エンザルタミドは、前立腺癌の治療薬としてメディベーション社によって開発され、販売されました。[ 60 ]米国では2012年8月にmCRPCの治療薬として米国食品医薬品局(FDA)に承認され、2018年7月には非転移性去勢抵抗性前立腺がんの治療薬としても承認された。 [ 20 ] [ 61 ]エンザルタミドは、 1995年に第一世代のNSAAであるビカルタミドが導入されて以来、15年以上ぶりに前立腺がんの治療薬として承認された新しいAR拮抗薬である。[ 62 ]これは、導入された最初の第二世代NSAAであった。[ 15 ]
2018年7月、FDAは去勢抵抗性前立腺がん患者の治療薬としてエンザルタミドを承認した。[ 63 ]この承認により適応が拡大され、非転移性去勢抵抗性前立腺がんと転移性去勢抵抗性前立腺がんの両方の患者が含まれるようになった。[ 63 ]エンザルタミドは以前にも転移性去勢抵抗性前立腺がん患者の治療薬として承認されていた。[ 63 ]
2019年12月、FDAは転移性去勢感受性前立腺がん(mCSPC)の患者の治療薬としてエンザルタミドを承認した。[ 11 ]エンザルタミドは、以前には去勢抵抗性前立腺がんの患者の治療薬として承認されていた。[ 11 ]
2023年6月、FDAは、相同組換え修復(HRR)遺伝子変異を有する転移性去勢抵抗性前立腺癌(mCRPC)患者の治療薬として、エンザルタミドとの併用でタラゾパリブを承認した。[ 64 ]
2023年11月、FDAは、転移リスクの高い生化学的再発を伴う非転移性去勢感受性前立腺がん(高リスクBCR)の患者の治療薬としてエンザルタミドを承認した。[ 65 ]有効性は、高リスクBCRを伴うnmCSPC患者1068人を対象としたランダム化比較臨床試験であるEMBARK(NCT02319837)で評価された。[ 65 ]すべての患者は、以前に根治的前立腺摘除術および/または治癒目的の放射線療法による根治的治療を受けており、PSA倍加時間≦9か月であり、登録時に救済放射線療法の対象ではなかった。[ 65 ]患者は、盲検化エンザルタミド160 mgを1日1回+ロイプロレリンを投与する群、非盲検化単剤エンザルタミド160 mgを1日1回+ロイプロレリンを投与する群、または盲検化プラセボを1日1回+ロイプロレリンを投与する群に1:1:1で無作為に割り付けられた。[ 65 ]この申請は優先審査およびファストトラック指定を受けた。[ 65 ]
社会と文化
法的地位
2024年6月、欧州医薬品庁のヒト用医薬品委員会は、前立腺がんの治療を目的とした医薬品エンザルタミド・ビアトリスの販売承認を付与することを推奨する肯定的な意見を採択した。[ 66 ] [ 67 ]この医薬品の申請者はビアトリス社である。[ 66 ]エンザルタミド・ビアトリスは、イクスタンジのジェネリック医薬品である。[ 66 ]
経済
ファイザーは、2023年にXtandiの収益が11億9100万米ドルになると報告した。[ 68 ]
研究
乳癌
研究によると、エンザルタミドは女性の特定の種類の乳がんの治療に効果がある可能性があることが示唆されています。 [ 69 ] [ 70 ]第II相臨床試験では、トリプルネガティブ、AR陽性乳がんの治療薬として試験されています。[ 71 ] [ 72 ]
多毛症
エンザルタミドは、多嚢胞性卵巣症候群の女性の多毛症および高アンドロゲン血症の潜在的な治療薬として示唆されている。[ 73 ] [ 74 ]
参照
参考文献
- ^ 「妊娠中のエンザルタミド(ザンジ)の使用」 Drugs.com 、 2018年9月4日。2019年12月22日時点のオリジナルよりアーカイブ。 2019年12月21日閲覧。
- ^ a b c d e f g h i j k l m n o p q r s t u v w x y z aa ab 「 Xtandi-エンザルタミドカプセル;Xtandi-エンザルタミド錠」 DailyMed 、 2023年11月20日。 2024年3月9日閲覧。
- ^ a b c d e f g h i Gibbons JA、Ouatas T、Krauwinkel W、Ohtsu Y、van der Walt JS、Beddo V、他。 (2015年)。「エンザルタミドの臨床薬物動態研究」。クリン・ファーマキネット。54 (10): 1043–55 .土井: 10.1007/s40262-015-0271-5。PMC 4580721。PMID 25917876。
- ^ 「処方薬:オーストラリアにおける新規化学物質の登録、2014年」。オーストラリア医薬品行政局(TGA)。2022年6月21日。 2023年4月10日時点のオリジナルよりアーカイブ。 2023年4月10日閲覧。
- ^ 「Xtandi (Astellas Pharma Australia Pty Ltd)」オーストラリア医薬品行政局 (TGA) 2025年3月13日. 2025年3月24日閲覧。
- ^ 「製品モノグラフのブランドセーフティアップデート」カナダ保健省、2024年2月。 2024年3月24日閲覧。
- ^ 「Xtandi EPAR」 .欧州医薬品庁(EMA) . 2013年6月21日. 2024年6月4日閲覧。
- ^ a b Kim TH, Jeong JW, Song JH, Lee KR, Ahn S, Ahn SH, 他 (2015年11月). 「ラットにおける抗前立腺癌薬エンザルタミドの薬物動態」Archives of Pharmacal Research . 38 (11): 2076–82 . doi : 10.1007/s12272-015-0592-9 . PMID 25956695. S2CID 26903608 .
- ^ a b Benoist GE, Hendriks RJ, Mulders PF, Gerritsen WR, Somford DM, Schalken JA, et al. (2016). 「転移性去勢抵抗性前立腺癌に使用される2つの新規経口薬:アビラテロン酢酸塩とエンザルタミドの薬物動態学的側面」 . Clin Pharmacokinet . 55 (11): 1369– 1380. doi : 10.1007/s40262-016-0403-6 . PMC 5069300. PMID 27106175 .
- ^ 「MedivationのMDV3100、ホルモン不応性前立腺がんの前臨床モデルで有効性を示す」(プレスリリース)。Medivation, Inc.、2007年2月26日。 2007年9月16日時点のオリジナルよりアーカイブ。 2009年5月10日閲覧。
- ^ a b c「FDA、転移性去勢感受性前立腺がんに対するエンザルタミドを承認」米国食品医薬品局(FDA) 2019年12月17日。2019年12月22日時点のオリジナルよりアーカイブ。 2019年12月21日閲覧。
 この記事には、パブリック ドメインであるこのソースからのテキストが組み込まれています。
この記事には、パブリック ドメインであるこのソースからのテキストが組み込まれています。 - ^ a b Sawyers, C., Jung, M., Chen, C., Ouk, S., Welsbie, D., Tran, C., ... & Yoo, D. (2006). 米国特許出願番号 11/433,829. https://patents.google.com/patent/US20070004753 [1]
- ^ 「FDA、ある種の後期前立腺がんに対する新たな治療法を承認」(プレスリリース)。米国食品医薬品局(FDA)。2012年8月31日。 2013年10月2日時点のオリジナルよりアーカイブ。 2019年12月16日閲覧。
- ^ Anna Azvolinsky (2012年9月4日). 「FDA、後期前立腺がん治療薬としてエンザルタミド(Xtandi)を承認」 CancerNetwork. 2012年9月13日時点のオリジナルよりアーカイブ。 2012年9月6日閲覧。
- ^ a b Saad F, Heinrich D (2013). 「去勢抵抗性前立腺がんに対する新たな治療法」. The Journal of Oncopathology . 1 (4): 23– 32. doi : 10.13032/tjop.2052-5931.100072 (2025年7月12日現在非アクティブ).
{{cite journal}}: CS1 maint: DOIは2025年7月時点で非アクティブです(リンク) - ^世界保健機関(2025).必須医薬品の選択と使用、2025年:WHO必須医薬品モデルリスト、第24版. ジュネーブ:世界保健機関. doi : 10.2471/B09474 . hdl : 10665/382243 .
- ^ Wenzel M, Nocera L, Collà Ruvolo C, Würnschimmel C, Tian Z, Shariat SF, et al. (2021年5月). 「高リスク非転移性去勢抵抗性前立腺癌に対するダロルタミド、アパルタミド、エンザルタミドによる治療後の全生存率および有害事象:系統的レビューおよびネットワークメタアナリシス」 . Prostate Cancer Prostatic Dis (Systematic review). 25 (2): 139– 148. doi : 10.1038/ s41391-021-00395-4 . PMC 9184262. PMID 34054128 .
- ^ Fishman SL, Paliou M, Poretsky L, Hembree WC (2019). 「トランスジェンダー成人の内分泌ケア」.トランスジェンダー医学. Contemporary Endocrinology. pp. 143– 163. doi : 10.1007/978-3-030-05683-4_8 . ISBN 978-3-030-05682-7. ISSN 2523-3785 . S2CID 86772102 .
アンドロゲン感受性前立腺がんの治療薬として開発された非ステロイド性選択的アンドロゲン受容体拮抗薬は、望ましい結果が得られなかったり、代替薬に耐えられないトランスジェンダー女性に時折使用されます [52]。フルタミド(ユーレキシン)で成功したという散発的な報告がありますが、テストステロン値の低下には酢酸シプロテロンほど効果的ではないと報告されています [12]。フルタミドとビカルタミド(カソデックス)はどちらも経口避妊薬と併用することで、多嚢胞性卵巣症候群(PCOS)の出生女性の多毛症に有意な改善を示しています [53, 54, 55, 56, 57]。トランスジェンダー患者に対するこれらの薬剤の抗アンドロゲン剤としての使用は、肝毒性の懸念から制限されています。しかし、低用量では、これらの薬剤は多毛症の治療に使用した場合、忍容性と有効性の両方が良好であることが示されている[57]。[...] 表8.2:抗アンドロゲン剤:[...] アンドロゲン受容体拮抗薬:[...] 種類:エンザルタミド。投与経路:経口。投与量:160mg/日。
- ^ Chan Swe N, Ahmed S, Eid M, Poretsky L, Gianos E, Cusano NE (2022年3月). 「性別適合ホルモン療法の心血管系および骨格系の健康への影響:文献レビュー」 . Metabol Open . 13 100173. doi : 10.1016/j.metop.2022.100173 . PMC 8907681. PMID 35282421 .
- ^ a b c d e Antonarakis ES (2013年6月). 「エンザルタミド:抗アンドロゲンの帝王」 . Translational Andrology and Urology . 2 (2): 119– 120. doi : 10.3978/j.issn.2223-4683.2012.09.04 . PMC 3785324. PMID 24076589 .
- ^ Payton S (2014年5月). 「前立腺がん:エンザルタミド、欧州の研究で優れた効果」 . Nature Reviews. Urology . 11 (5): 243. doi : 10.1038/nrurol.2014.98 . PMID 24776976. S2CID 29251381 .
- ^ a b c Golshayan AR, Antonarakis ES (2013). 「エンザルタミド:前立腺がん治療におけるその使用に関するエビデンスに基づくレビュー」 . Core Evidence . 8 : 27–35 . doi : 10.2147/CE.S34747 . PMC 3622394. PMID 23589709 .
- ^ Tombal B, Borre M, Rathenborg P, Werbrouck P, Van Poppel H, Heidenreich A, et al. (2015年11月). 「ホルモン治療未治療前立腺がんにおけるエンザルタミド単剤療法の長期的有効性と安全性:1年および2年のオープンラベル追跡調査結果」 . European Urology . 68 (5): 787–94 . doi : 10.1016/j.eururo.2015.01.027 . PMID 25687533 .
- ^ Jeffrey K Aronson (2014年3月4日). Side Effects of Drugs Annual: A worldly survey of new data in adverse drug reactions . Newnes. pp. 740–. ISBN 978-0-444-62636-3。
- ^ a b c d e Tombal B, Borre M, Rathenborg P, Werbrouck P, Van Poppel H, Heidenreich A, et al. (2014年5月). 「ホルモン未治療前立腺癌におけるエンザルタミド単剤療法:オープンラベル単群第2相試験の一次解析」. The Lancet. Oncology . 15 (6): 592– 600. doi : 10.1016/S1470-2045(14)70129-9 . PMID 24739897 .
- ^ Vogelzang NJ (2012年9月). 「エンザルタミド:転移性前立腺癌治療における大きな進歩」. The New England Journal of Medicine . 367 (13): 1256–7 . doi : 10.1056/NEJMe1209041 . PMID 23013078 .
- ^ a b Poole A, Alva A, Batten J, Agarwal N (2014年12月17日). 「転移性去勢抵抗性前立腺癌:アンドロゲンシグナル伝達阻害剤の役割」 . Dicker AP, Kelly WK, Trabulsi EJ, Zaorsky NG (編).前立腺癌:診断と管理への多分野アプローチ. Demos Medical Publishing. p. 342. ISBN 978-1-936287-59-8. 2023年1月10日時点のオリジナルよりアーカイブ。2016年1月5日閲覧。
- ^ a b Foster WR, Car BD, Shi H, Levesque PC, Obermeier MT, Gan J, et al. (2011). 「薬剤の安全性は、新規アンドロゲン受容体拮抗薬の発見と開発における障壁となっている」. The Prostate . 71 (5): 480–8 . doi : 10.1002/pros.21263 . PMID 20878947. S2CID 24620044 .
- ^ Rathkopf D, Scher HI (2013). 「去勢抵抗性前立腺癌におけるアンドロゲン受容体拮抗薬」 . Cancer Journal . 19 (1): 43–9 . doi : 10.1097/PPO.0b013e318282635a . PMC 3788593. PMID 23337756 .
- ^ジェローム Z. リット (2013 年 1 月 25 日)。Litt の薬剤噴出と反応マニュアル、第 19 版。 CRCプレス。 148ページ–。ISBN 978-1-84214-599-9. 2023年1月10日時点のオリジナルよりアーカイブ。2016年1月5日閲覧。
- ^ Tan PS, Haaland B, Montero AJ, Kyriakopoulos CE, Lopes G (2014). 「ドセタキセル投与後の転移性去勢抵抗性前立腺癌(mCRPC)に対するホルモン療法エンザルタミドとアビラテロン酢酸塩の間接比較」 . Clinical Medicine Insights: Oncology . 8 CMO.S13671: 29– 36. doi : 10.4137/CMO.S13671 . PMC 3964205. PMID 24678245 .
- ^ Labrie F (2015年1月). 「前立腺癌における精巣および局所性アンドロゲンの併用遮断:内分泌学に基づく極めて重要な医学的進歩」. J. Steroid Biochem. Mol. Biol . 145 : 144–56 . doi : 10.1016/j.jsbmb.2014.05.012 . PMID 24925260. S2CID 23102323 .
- ^ a b Scher HI, Beer TM, Higano CS, Anand A, Taplin ME, Efstathiou E, et al. (2010年4月). 「去勢抵抗性前立腺癌におけるMDV3100の抗腫瘍活性:第1-2相試験」 . Lancet . 375 (9724): 1437–46 . doi : 10.1016/S0140-6736(10)60172-9 . PMC 2948179. PMID 20398925 .
- ^ a b Crona DJ, Whang YE (2015年6月). 「去勢抵抗性前立腺癌患者におけるエンザルタミド誘発性後頭葉可逆性脳症症候群」 . Investigational New Drugs . 33 (3): 751–4 . doi : 10.1007/ s10637-014-0193-3 . PMC 4451215. PMID 25467090 .
- ^ a b c McCutcheon SB (2013). 「エンザルタミド:前立腺癌治療の武器となる新たな薬剤」 . J Adv Pract Oncol . 4 (3): 182–5 . doi : 10.6004/jadpro.2013.4.3.7 . PMC 4093421. PMID 25031999 .
- ^ Narayanan R, Coss CC, Dalton JT (2018). 「選択的アンドロゲン受容体モジュレーター(SARM)の開発」 . Mol. Cell. Endocrinol . 465 : 134–142 . doi : 10.1016/j.mce.2017.06.013 . PMC 5896569. PMID 28624515 .
- ^ a b c d e f Tran C, Ouk S, Clegg NJ, Chen Y, Watson PA, Arora V, et al. (2009年5月). 「進行性前立腺がん治療のための第二世代抗アンドロゲンの開発」 . Science . 324 ( 5928): 787–90 . Bibcode : 2009Sci...324..787T . doi : 10.1126/science.11 68175. PMC 2981508. PMID 19359544 .
- ^ Li JJ、Johnson DS(2015年12月14日)「第6章:エンザルタミド」『革新的な医薬品合成』John Wiley & Sons. p. 103. ISBN 978-1-118-82005-6。
- ^ a b c Ricci F, Buzzatti G, Rubagotti A, Boccardo F (2014年11月). 「前立腺がん治療における抗アンドロゲン療法の安全性」.医薬品安全性に関する専門家意見. 13 (11): 1483–99 . doi : 10.1517/14740338.2014.966686 . PMID 25270521. S2CID 207488100 .
- ^ Rodriguez-Vida A, Galazi M, Rudman S, Chowdhury S, Sternberg CN (2015). 「転移性去勢抵抗性前立腺癌の治療におけるエンザルタミド」 . Drug Design, Development and Therapy . 9 : 3325–39 . doi : 10.2147/DDDT.S69433 . PMC 4492664. PMID 26170619 .
- ^ a b医薬化学年次報告書エルゼビア・サイエンス 2013年9月13日 pp. 498–. ISBN 978-0-12-417151-0。
- ^ KC Balaji (2016年4月25日).泌尿器腫瘍学診療における転移性前立腺癌の管理. Springer. pp. 24– 25. ISBN 978-3-319-31341-2. 2023年1月10日時点のオリジナルよりアーカイブ。2016年10月1日閲覧。
- ^ Keating GM (2015年3月). 「エンザルタミド:化学療法未治療の転移性去勢抵抗性前立腺癌におけるその使用に関するレビュー」. Drugs & Aging . 32 (3): 243–9 . doi : 10.1007/s40266-015-0248- y . PMID 25711765. S2CID 29563345 .
- ^ Beer TM, Armstrong AJ, Rathkopf DE, Loriot Y, Sternberg CN, Higano CS, 他 (2014年7月). 「転移性前立腺癌に対する化学療法前のエンザルタミド」. The New England Journal of Medicine . 371 (5): 424–33 . doi : 10.1056/NEJMoa1405095 . PMC 4418931. PMID 24881730 .
- ^ Claessens F、Helsen C、Prekovic S、Van den Broeck T、Spans L、Van Poppel H、他。 (2014年12月)。 「前立腺がんにおけるエンザルタミド耐性の新たなメカニズム」。ネイチャーレビュー 泌尿器科。11 (12): 712–6 .土井: 10.1038/nrurol.2014.243。PMID 25224448。S2CID 13313385。
- ^ Balbas MD, Evans MJ, Hosfield DJ, Wongvipat J, Arora VK, Watson PA, et al. (2016年4月). 「合理的な薬剤設計による抗アンドロゲンに対する変異に基づく耐性の克服」 . eLife . 2 e00499. doi : 10.7554/eLife.00499 . PMC 3622181. PMID 23580326 .
- ^ Prekovic S, van Royen ME, Voet AR, Geverts B, Houtman R, Melchers D, et al. (2016年5月). 「F877LおよびT878A変異がエンザルタミドに対するアンドロゲン受容体反応に及ぼす影響」 . Molecular Cancer Therapeutics . 15 (7): 1702–12 . doi : 10.1158/1535-7163.MCT-15-0892 . PMID 27196756 .
- ^ Antonarakis ES, Lu C, Wang H, Luber B, Nakazawa M, Roeser JC, 他 (2014年9月). 「前立腺癌におけるAR-V7とエンザルタミドおよびアビラテロンに対する耐性」 . New England Journal of Medicine . 371 ( 11): 1028–38 . doi : 10.1056/NEJMoa1315815 . PMC 4201502. PMID 25184630 .
- ^ Arora VK, Schenkein E, Murali R, Subudhi SK, Wongvipat J, Balbas MD, et al. (2013年12月). 「グルココルチコイド受容体はアンドロゲン受容体遮断を回避し、抗アンドロゲンに対する抵抗性を付与する」 . Cell . 155 ( 6): 1309–22 . doi : 10.1016/j.cell.2013.11.012 . PMC 3932525. PMID 24315100 .
- ^ Cui Y, Nadiminty N, Liu C, Lou W, Schwartz CT, Gao AC (2014年6月). 「NF-κB2/p52によるグルコース代謝の上方制御が去勢抵抗性前立腺癌細胞におけるエンザルタミド耐性を媒介する」 .内分泌関連癌. 21 (3): 435–42 . doi : 10.1530/ERC-14-0107 . PMC 4021715. PMID 24659479 .
- ^ Nguyen HG, Yang JC, Kung HJ, Shi XB, Tilki D, Lara PN, et al. (2014年9月). 「オートファジーを標的とすることで、去勢抵抗性前立腺癌細胞におけるエンザルタミド耐性を克服し、異種移植モデルにおける治療反応性を向上させる」 . Oncogene . 33 ( 36): 4521–30 . doi : 10.1038/onc.2014.25 . PMC 4155805. PMID 24662833 .
- ^ Miyamoto DT, Zheng Y, Wittner BS, Lee RJ, Zhu H, Broderick KT, et al. (2015年9月). 「前立腺CTCのRNA-Seq解析は、抗アンドロゲン抵抗性における非典型的なWntシグナル伝達を示唆する」 . Science . 349 (6254): 1351–6 . Bibcode : 2015Sci...349.1351M . doi : 10.1126/science.aab0917 . PMC 4872391. PMID 26383955 .
- ^ Liu C, Lou W, Zhu Y, Yang JC, Nadiminty N, Gaikwad NW, 他 (2015年4月). 「前立腺がんにおいて、内分泌アンドロゲンとAKR1C3活性化がエンザルタミドに対する耐性を付与する」 . Cancer Research . 75 (7): 1413–22 . doi : 10.1158/0008-5472.CAN-14-3080 . PMC 4383695. PMID 25649766 .
- ^ Liu C, Zhu Y, Lou W, Cui Y, Evans CP, Gao AC (2014年2月). 「恒常活性型Stat3の阻害はLNCaP誘導性前立腺癌細胞におけるエンザルタミド耐性を回復させる」. The Prostate . 74 (2): 201–9 . doi : 10.1002/pros.22741 . PMC 4437226. PMID 24307657 .
- ^ Hamilton RJ編(2013年12月4日). Tarascon Pocket Pharmacopoeia 2014 Deluxe Lab-Coat Edition . Jones & Bartlett Publishers. pp. 336–. ISBN 978-1-284-05399-9. 2023年1月10日時点のオリジナルよりアーカイブ。2016年1月5日閲覧。
- ^ Georg F. Weber (2015年7月22日).がんの分子治療法. Springer. pp. 318–. ISBN 978-3-319-13278-5。
- ^ Borman S (2008). 「新しい前立腺がん治療薬クラス」. Chemical & Engineering News . 86 (38): 84– 87. doi : 10.1021/cen-v086n038.p084 .
- ^ Jung ME, Ouk S, Yoo D, Sawyers CL, Chen C, Tran C, 他 (2010年4月). 「去勢抵抗性前立腺癌(CRPC)に対するチオヒダントインアンドロゲン受容体拮抗薬の構造活性相関」 . Journal of Medicinal Chemistry . 53 (7): 2779–96 . doi : 10.1021/jm901488g . PM C 3180999. PMID 20218717 .
- ^ a b Liu B、Su L、Geng J、Liu J、Zhao G (2010)。 「アンドロゲン受容体を標的とする非ステロイド性抗アンドロゲン剤の開発」。ケムメドケム。5 (10): 1651–61 .土井: 10.1002/cmdc.201000259。PMID 20853390。S2CID 23228778。
- ^ 「エンザルタミド - アステラス製薬/メディベーション - AdisInsight」。2018年7月17日時点のオリジナルよりアーカイブ。 2017年11月19日閲覧。
- ^ 「FDA、前立腺がんに対するXtandiの承認を拡大」 www.healio.com . 2018年7月17日時点のオリジナルよりアーカイブ。 2018年7月17日閲覧。
- ^ Gohil K (2015年8月). 「前立腺がんにおける今後の刺激的な治療法」 . P & T. 40 ( 8): 530–1 . PMC 4517537. PMID 26236143 .
- ^ a b c「FDA、去勢抵抗性前立腺がん治療薬としてエンザルタミドを承認」米国食品医薬品局(FDA)2018年7月13日。 2024年3月9日閲覧。
 この記事には、パブリック ドメインであるこのソースからのテキストが組み込まれています。
この記事には、パブリック ドメインであるこのソースからのテキストが組み込まれています。 - ^ 「FDA、HRR遺伝子変異を伴う転移性去勢抵抗性前立腺がんにタラゾパリブとエンザルタミドの併用を承認」米国食品医薬品局(FDA )2023年6月20日。 2023年6月21日時点のオリジナルよりアーカイブ。 2024年3月9日閲覧。
 この記事には、パブリック ドメインであるこのソースからのテキストが組み込まれています。
この記事には、パブリック ドメインであるこのソースからのテキストが組み込まれています。 - ^ a b c d e「FDA、生化学的再発を伴う非転移性去勢感受性前立腺がんにエンザルタミドを承認」米国食品医薬品局(FDA) 2023年11月16日。 2023年11月17日時点のオリジナルよりアーカイブ。 2024年3月9日閲覧。
 この記事には、パブリック ドメインであるこのソースからのテキストが組み込まれています。
この記事には、パブリック ドメインであるこのソースからのテキストが組み込まれています。 - ^ a b c「エンザルタミド・ビアトリスEPAR」欧州医薬品庁2024年6月27日2024年6月29日閲覧。テキストは、欧州医薬品庁の著作権が付与されているこの情報源からコピーされました。出典を明記すれば、複製は許可されます。
- ^ 「2024年6月24~27日に開催されたヒト用医薬品委員会(CHMP)の会議ハイライト」。欧州医薬品庁。2024年6月28日。 2024年7月12日時点のオリジナルよりアーカイブ。 2024年7月12日閲覧。
- ^ 「ファイザーの年次報告」。ファイザー2023年度年次報告書。2023年12月31日。 2024年12月30日閲覧。
- ^ 「乳がんモデルにおけるエンザルタミドの前臨床評価」 。2013年2月23日時点のオリジナルよりアーカイブ。
- ^ 「メディベーションとアステラス製薬、MDV3100が乳がん細胞の増殖を阻害することを示す新たな前臨床研究結果を発表」(プレスリリース)。MarketWatch。2011年8月4日。 2011年9月25日閲覧。
- ^ Traina TA, O'Shaughnessy J, Nanda R, Schwartzberg L, Abramson V, Cortes J, et al. (2015). 「抄録 P5-19-09: アンドロゲン受容体(AR)阻害剤であるエンザルタミドの進行性AR陽性トリプルネガティブ乳がん(TNBC)に対する第2相単群試験の予備的結果」. Cancer Research . 75 (9 Supplement): P5-19-09. doi : 10.1158/1538-7445.SABCS14-P5-19-09 .
- ^ Le Du F, Eckhardt BL, Lim B, Litton JK, Moulder S, Meric-Bernstam F, et al. (2015年5月). 「トリプルネガティブ乳がんにおける個別化治療の将来は分子サブタイプに基づくのか?」 . Oncotarget . 6 ( 15): 12890– 12908. doi : 10.18632/oncotarget.3849 . PMC 4536987. PMID 25973541 .
- ^ Moretti C, Guccione L, Di Giacinto P, Simonelli I, Exacoustos C, Toscano V, et al. (2017). 「多嚢胞性卵巣症候群および重症多毛症に対する経口避妊薬とビカルタミドの併用 - 二重盲検RTC」 . J. Clin. Endocrinol. Metab . 103 (3): 824– 838. doi : 10.1210/jc.2017-01186 . PMID 29211888 .
- ^ Luque-Ramírez M, Escobar-Morreale HF (2015). 「多嚢胞性卵巣症候群におけるアンドロゲン過剰の治療標的」. Expert Opin Ther Targets . 19 (11): 1545–60 . doi : 10.1517/14728222.2015.1075511 . PMID 26549181 . S2CID 207486790 .
