染料

染料は、ある種の溶媒に溶ける色のついた物質です。対照的に、顔料はすべての溶媒に溶けないか、ほとんど溶けません。染料は溶解性が高いため、着色する物質と化学的に結合することができます。染料は通常、水溶液で塗布され、繊維上での染料の堅牢度を高めるために媒染剤が必要になる場合があります。[ 1 ]
天然染料の大部分は、根、果実、樹皮、葉、木材、菌類、地衣類などの動物以外の資源から得られます。[ 2 ]しかし、需要の高まりと技術の進歩により、現代世界で使用されている染料のほとんどは、石油化学製品などの物質から合成されています。[ 3 ]昆虫や鉱物から抽出されるものもあります。[ 4 ]
合成染料は様々な化学物質から製造されます。染料の大部分は、コスト、光学的特性(色)、そして耐久性(堅牢性、媒染性)に優れているため、この方法で製造されます。[ 1 ]染料と顔料はどちらも可視光の特定の波長のみを吸収するため、色が付いています。染料は通常、何らかの溶媒に溶けますが、顔料は不溶性です。一部の染料は、塩を加えることで不溶性になり、レーキ顔料を作ることができます。
歴史

織物の染色は新石器時代にまで遡る。歴史を通じて、人々は身近で入手可能な材料を用いて織物を染めてきた。ティリアンパープルや深紅のケルメスといった天然の無脊椎動物由来の染料のように、鮮やかで永久的な色を生み出す希少な染料は、古代および中世の世界では非常に貴重な贅沢品であった。ウォード、インディゴ、サフラン、アカネといった植物由来の染料は、アジアやヨーロッパの経済において重要な交易品であった。アジアやアフリカでは、後染め布の色の吸収を制御する防染技法を用いて模様のある織物が生産されていた。コチニールやログウッドといった新世界の染料は、スペインの宝船団によってヨーロッパにもたらされ、[ 5 ]、ヨーロッパの染料は植民者によってアメリカ大陸に運ばれた。[ 6 ]

ジョージア共和国では、3万6000年前の先史時代の洞窟で染色された亜麻繊維が発見されています。[ 7 ] [ 8 ]考古学的証拠によると、特にインドとフェニキアでは、 5000年以上前から染色が広く行われてきました。初期の染料は、動物、植物、または鉱物から得られ、ほとんど加工されていませんでした。これまでのところ、染料の最大の供給源は植物界、特に根、果実、樹皮、葉、木材であり、商業規模で使用されているのはごくわずかです。[ 9 ]
初期の工業化はスコットランドのJ・プラー・アンド・サンズ社によって行われました。 [ 10 ]最初の合成染料であるモーブは、 1856年にウィリアム・ヘンリー・パーキンによって偶然発見されました。[ 11 ] [ 12 ] [ 13 ]モーベイン(マウベイン)の発見は、合成染料、そして有機化学全般の急速な発展のきっかけとなりました。その後、フクシン(フクシン)、サフラニン(サフラニン)、インデュリン(インデュリン)といったアニリン系染料が続きました。それ以来、数千種類もの合成染料が開発されてきました。[ 14 ] [ 15 ]
1856年のモーベンの発見は、合成染料産業の発展につながりました。イギリスのマンチェスターでは、イヴァン・レビンシュタイン(レビンシュタイン社) [ 16 ] 、 チャールズ・ドレイファス(クレイトン・アニリン社)[ 16 ]、ウィリアム・クラウス(クラウス社)[ 17 ]など、多くの人々が染料製造工場を設立しました。
藤色の発見は、免疫学と化学療法の発展にもつながりました。1863年、バイエルAGの前身となる会社がドイツのヴッパータールに設立されました。1891年、パウル・エールリッヒは特定の細胞や生物が特定の染料を選択的に取り込むことを発見しました。彼は、染料が他の細胞に影響を与えないのであれば、病原性微生物を殺すのに十分な量の染料を注入できると推論しました。エールリッヒはさらに、梅毒を標的とする化合物を使用しました。これは、体内の細菌を選択的に殺すために化学物質が使用された最初の例です。彼はまた、マラリアの原因となるマラリア原虫を標的とするためにメチレンブルーを使用しました。[ 18 ]
染料の分類
_in_a_hairdresser_shop_in_Germany_(2023).jpg/440px-Shelve_with_various_hair_colours_(hair_dyes)_in_a_hairdresser_shop_in_Germany_(2023).jpg)
染料の色は、電磁スペクトルの可視領域(380~750 nm)における光の吸収によって決まります。化学構造は光吸収を決定し、多くの分類体系の基礎となっています。[ 1 ]
化学構造による分類
アントラキノン染料
この染料群の基本構造はアントラキノンです。置換基を変えることで、黄色から赤、青から緑までほぼすべての色を得ることができますが、特に赤と青のアントラキノン染料は重要です。還元により、キノンは対応する水溶性ヒドロキノンに変換され、アントラキノン染料は建染染料として使用できるようになります。適切な置換基を用いることで、アントラキノン染料は合成繊維の染色用の分散染料としても使用できます。スルホン酸基を含む水溶性アントラキノン染料は、酸性 染料または反応性染料として使用されます
アゾ染料

アゾ染料は、アリール基またはアルケニル基で置換されたアゾ基を基本構造要素として有します。複数のアゾ基を含むアゾ染料は、ビスアゾ(ジスアゾとも呼ばれます)、トリスアゾ、テトラキスアゾ、およびポリアゾ染料と呼ばれます。アリール置換基は通常、ベンゼンまたはナフタレン誘導体ですが、ピラゾールやピリドンなどの複素芳香族系も含まれる場合があります。アルケニル置換基としては、アセト酢酸の置換アニリドなどのエノール化可能な脂肪族基が用いられます。
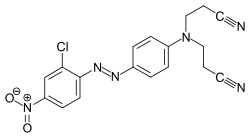
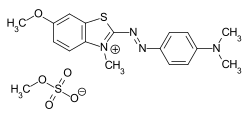
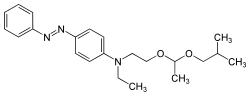
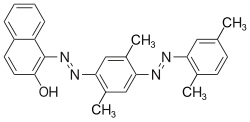
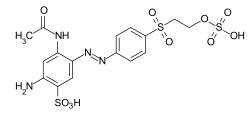
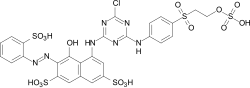
これらの染料は、芳香族アミンのジアゾ化、続いてジアゾニウム塩と電子豊富な芳香族化合物またはβ-ジカルボニル化合物とのアゾカップリング反応によって合成されます。アゾ染料は、染料の中で最も重要かつ広範なクラスであり、ほぼすべての応用分野における染料カテゴリーに含まれています(→応用技術による分類)。天然に存在するアゾ染料は知られていません。ターコイズと鮮やかな緑を除いて、ほぼすべての色はアゾ染料を用いて実現できます。アゾ基は還元剤に敏感で、分解されて染料が変色します。様々なタイプのアゾ染料の例(モノアゾ染料およびビスアゾ染料 / ベンゼン、ナフタレン残基 / ピリドン、アセトアセトアニリドカップリング成分 / 金属錯体染料):
ジオキサジン染料

ジオキサジン染料は、トリフェンジオキサジンを基本構造として含んでいます。鮮やかな色合いのこれらの染料は、優れた染色堅牢度を示し、アゾ染料とアントラキノン染料の両方の利点を兼ね備えています。ジオキサジン染料は、直接染料と反応染料として市販されています。[ 19 ]
インディゴイド染料

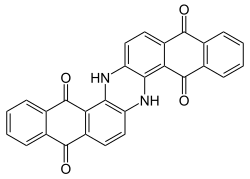
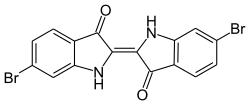
インディゴイド染料はカルボニル染料に属し、建染染料として用いられます。最も重要な染料はインディゴです。インディゴは古代から植物から抽出された天然染料で、現在でも工業的に大量に生産されており、特にジーンズの染色に用いられています。もう一つの天然染料は、古代紫(CIナチュラルバイオレット1 /ジブロミンジゴ)です。
- CI バットブルー 1(インディゴ)
- CIナチュラルバイオレット1
金属錯体染料
金属錯体染料は、金属と1つ以上の電子供与体を含む染料配位子から形成される錯化合物から構成されます。銅とクロムの化合物が主流ですが、コバルト、ニッケル、鉄の錯体も少量使用されます。配位子としては、アゾ染料、メチン染料、ホルマザン、またはフタロシアニンがよく使用されます。金属錯体染料は優れた堅牢性が特徴です。
ホルマザン染料

ホルマザン染料は構造的にアゾ染料に関連しています。基本構造はトリフェニルホルマザンです。銅、ニッケル、コバルトなどの遷移金属とキレート錯体を形成します。置換基に応じて、非錯体ホルマザンはオレンジ色から濃い赤色ですが、金属錯体ホルマザンは紫、青、または緑色です。これらは、ジアゾニウム塩とヒドラゾンのアゾカップリングによって合成されます。特に商業的に重要なのは、様々なホルマザンの青色の四座配位銅キレート錯体で、主に綿の反応染料として使用されています
- CIリアクティブブルー160
フタロシアニン染料
フタロシアニン染料は、フタロシアニン構造に基づく銅またはニッケルの金属錯体です。構造的にはポルフィリンと関連しており、アヌレン元素を共有しています。主にスルホ塩素化によって水溶性置換基を導入することで、ターコイズ色から鮮やかな緑色の染料を得ることができます。フタロシアニン染料は、優れた耐光性が特徴です
- フタロシアニン(アザ[18]アヌレン)
- CIリアクティブブルー7
メチン染料

メチン染料またはポリメチン染料は、発色団として共役二重結合を有し、2つの末端基は電子受容体Aと電子供与体Dとして機能します。これらの末端基は通常、窒素原子または酸素原子を含み、複素環の一部である場合があり、二重結合は芳香族系の一部である場合があります。1つ以上のメチン基が窒素原子に置き換えられた場合、染料はアザ類似体メチン染料と呼ばれます。これにより、異なるサブクラスが生じます
シアニン色素は、共役二重結合の両側に第三級アミノ基と第四級アンモニウム化合物が配置されています。 [ 21 ] 2つのメチン基が窒素原子に置換され、一方の末端基が複素環の一部であり、もう一方が開鎖である場合、重要なジアザヘミシアニン色素が形成されます。例:ベーシックレッド22。
スチリル染料:ポリエン骨格にフェニル環が挿入されたことで、スチレン構造要素を含む染料です。例:ディスパースイエロー31。
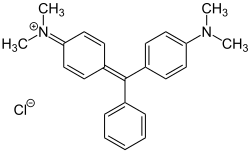
トリアリールメチン染料は、トリフェニルメタンから誘導され、少なくとも2つの芳香環に電子供与性置換基を有するため、古い文献ではトリフェニルメタン染料とも呼ばれています。例:ベーシックグリーン4(マラカイトグリーン)。 [ 22 ]
- CIベーシックレッド22
- CI ディスパースイエロー 31
- CIベーシックグリーン4(マラカイトグリーン)
ニトロ染料とニトロソ染料
ニトロ染料では、ニトロ基は芳香環上の電子供与体であるヒドロキシ基(-OH)またはアミノ基(-NH 2)に対してオルト位に位置しています。この染料群の最も古い代表例はピクリン酸(2,4,6-トリニトロフェノール)です。ヒドロキシニトロ染料はもはや商業的に重要ではありません。これは比較的小規模ですが、歴史的に重要な染料群であり、その代表例は高い耐光性と簡便な製造を特徴としています。ニトロ染料は黄色から茶色の色合いを示します。分子サイズが比較的小さいため、分散染料としてポリエステル繊維の染色に重要な用途があります。また、酸性染料や顔料染料としても使用されます。
希少なニトロソ染料は、ニトロソ基を含む芳香族化合物です。ニトロソ基のオルト位にヒドロキシ基を持つニトロソ染料は、金属錯体としてのみ使用されます。代表的なものとしては、ナフトールグリーンB(CIアシッドグリーン1)が挙げられます。 [ 23 ]
- ピクリン酸
- CIアシッドグリーン1
硫化染料
硫化染料(スルフィン染料)は、芳香族残基間にジスルフィド架橋またはオリゴスルフィド結合を含む、水に不溶性の高分子染料です。ベンゼン、ナフタレン、またはアントラセン誘導体を硫黄またはポリスルフィドと溶融して生成され、構造が明確ではありません。特に綿繊維の染色に適しています。バット染料と同様に、苛性ソーダと亜ジチオン酸塩または硫化ナトリウムを使用して水溶性の形(ロイコ化合物)に還元し、繊維に塗布してから酸化によって不溶性の形で固定します。毒物学的および生態学的理由から、クロム酸塩による酸化は、低硫化物硫化染料と硫化物を含まない還元剤にますます置き換えられています。生産コストが低いため、硫化染料は量の面で引き続き重要な役割を果たしています。色は一般に落ち着いたものですが、洗濯堅牢度と光堅牢度に優れているのが特徴です。[ 24 ]
応用技術による分類
染料の色合いは基本的に発色団によって決定されますが、適切な化学基を導入することで染料の特性を変化させ、様々な基質への染色を可能にします。このことから、染料は染色プロセスに基づいて分類されます。この分類は、染料化学における重要な標準規格であるカラーインデックスにも用いられています。カラーインデックス(CI)は、染料のクラス、色、化学的性質を示しています。10,000種類以上の染料が掲載されており、そのうち50%以上がアゾ染料です。[ 25 ]
媒染染料
この用語は媒染染色に由来し、適切な酸性染料を媒染された布地、主にウールやシルクに塗布します。染色前に、繊維は[クロム]、[鉄]、またはアルミニウムの塩で処理されます。その後の蒸煮中に、繊維上に金属水酸化物が形成されます。染色中、これらの水酸化物は(通常は特殊な)酸性染料と反応して金属錯体染料を形成します。繊維上でのこのプロセスはニス塗りに相当します。 [ 26 ]
クロム塩が使用される染料は、クロム染料と呼ばれます。染料の種類に応じて、クロム塩(通常はクロム酸塩または二クロム酸塩)は、染色前、染色中、または染色後に添加されます。したがって、前媒染、後媒染、および一浴クロム染色法が区別されます。クロム染料は優れた耐湿堅牢度で知られています。しかしながら、繊維や染色廃水の重金属汚染は、重大な生態学的懸念事項です。[ 27 ]
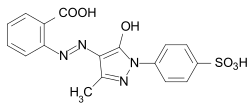
媒染染料は、カラーインデックスでは「CI媒染染料」と表記されます。例:
- CI モーダントブラック 9
- CI モーダントイエロー 8
- CI モーダントブラック 7
- CI モーダントレッド 60
- CI モーダントブルー 9
歴史的には、クロム、鉄、アルミニウム塩に加え、バナジン酸アンモニウム、タンニン酸、酸化アルミニウム、アンチモン、バリウム、鉛、コバルト、銅、マンガン、ニッケル、スズ、トルコレッドオイルをベースとした媒染剤も使用されていました。また、酒石酸アンチモンカリウムや塩化アンチモン(III)などの様々なアンチモン塩、ケイ酸ナトリウム、リン酸ナトリウム、さらには牛糞も定着剤として使用されていました。 [ 28 ]
直接染料
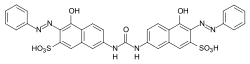
直接染料(または直接染料)は、その高い直接性により、水溶液から繊維に直接吸収されます。特にセルロース繊維に適しています。繊維への結合は、主にファンデルワールス力による物理的相互作用によって起こります。ほとんどの直接染料はアゾ染料グループに属し、特にポリアゾ染料はそうです。カラーインデックスでは、CI直接染料として指定されています。例:
- CIダイレクトブルー8
- CIダイレクトオレンジ26
- CIダイレクトイエロー9
分散染料
分散染料は水にほとんど溶けず、主に疎水性ポリエステルやセルロースアセテートの染色に使用されます。分散剤と共に細かく粉砕され、分子状に溶解した染料が染色中に繊維に拡散し、固溶体を形成します。これにより、洗濯堅牢度と耐光堅牢度に優れた染料が得られます
分散染料の大部分はアゾ染料に属します。分散染料は、特にポリエステル繊維の広範な用途と機械的特性により、非常に重要なグループに属しています。1999年の西ヨーロッパにおける総売上高は9,800万ユーロに達しました。
カラーインデックスによると、これらは「CI分散染料」と指定されています。例:
- CI ディスパースオレンジ 44
- CI ディスパースブルー 797
- CI ディスパースレッド 177
現像染料またはカップリング染料
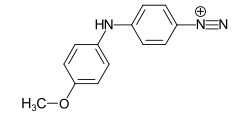
染料現像においては、水溶性カップリング成分(CIアゾイックカップリング成分)と水溶性ジアゾ成分(CIアゾイックジアゾ成分)の反応により、実質的に水に不溶性の染料が繊維上に直接生成されます。この染料クラスは主にセルロース繊維に使用され、非常に優れた湿潤堅牢度を特徴としています。染料現像において最も重要なカップリング成分はナフトールASです。
- CI アゾイックカップリング成分2(ナフトールAS)
- CI アゾイックカップリング成分35(ナフトールAS-LG)
- CI アゾイックジアゾ成分3(エヒトスカーレットソルトGG)
- CIアゾイックジアゾ成分35(バリアミンブルー塩B)
カチオン染料
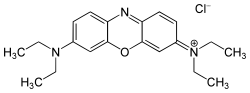
カチオン染料は、特にポリアクリロニトリル(PAN)繊維やアニオン変性ポリエステル繊維において、鮮やかで耐光性に優れた色を生み出すカチオン化合物です。繊維上の負に帯電した基とイオン結合を形成します。カチオン染料には様々な発色団を使用できますが、メチン染料では、他の発色団とは異なり、正電荷が非局在化しています
カチオン染料はカラーインデックスでは「CI塩基性染料」と指定されていますが、最近の文献ではこの染料クラスに対して「塩基性染料」という用語は一般的に使用されなくなりました。 [ 23 ]
- CIベーシックオレンジ22
- CIベーシックブルー3
- CIベーシックブルー54
- CIベーシックレッド18
バット染料
バット染料は、アルカリ溶液中で還元(バットング)することで、染色のために可溶性のジヒドロまたはロイコ塩基に変換される水不溶性顔料です。陰イオンは綿やビスコース繊維と十分な親和性を示し、吸収を可能にします。その後、染料は大気中の酸素または酸化剤による酸化によって不溶性に戻ります。染料は繊維内の分子レベルで効果的に固定され、この「繊維内の沈殿」により、非常に高い洗濯堅牢度と光堅牢度が得られます。[ 29 ]水不溶性硫化染料も同様の挙動を示します
最も重要なバット染料は藍です。インダンスレン染料も非常に重要です。
バット染料は、カラーインデックスでは「CIバット染料」と表記されます。例:
- CIバットグリーン11
- CIバットオレンジ7
- CI バットレッド 23
食品着色料
食品着色料は、加工による色の変化を補うため、または消費者の期待に応えるために食品添加物として使用されます。天然由来の着色料と合成着色料の両方が使用されています。食品着色料の使用は法律で厳しく規制されており、 EUでは2008年12月16日付の食品添加物に関する規則(EC)第1333/2008号によって規制されています。[ 30 ] E番号が付与された承認済みの添加物のみが販売可能であり、製品に表示する必要があります。[ 31 ]
食品着色料は、カラーインデックスでは「CI Food Dyes」として指定されています。
食品着色料は食品添加物に分類されるため、一部の工業用着色料よりも高い基準で製造されています。食品着色料には直接染料、媒染染料、建染染料があり、その使用は法律によって厳しく規制されています。多くはアゾ染料ですが、緑や青などの色にはアントラキノン化合物やトリフェニルメタン化合物が使用されています。天然由来の染料も使用されています。[ 32 ]
溶剤染料
カラーインデックスで「溶剤染料」と指定されている溶剤染料は、アルコール、エステル、炭化水素などの様々な有機溶剤に溶解する水不溶性染料です。原則として、溶剤染料の構造にはスルホン酸基やカルボキシル基は含まれません。例外として、分子内スルホン酸基またはカルボキシル基が対イオンとして作用するカチオン染料があります。溶剤染料は、アゾ染料、アントラキノン染料、金属錯体染料、フタロシアニンなど、様々な染料クラスに存在します。これらはラッカー(例:ザポンラッカー用のザポン染料)、鉱油製品(スーダン染料)、ワックス、インク、透明プラスチックの着色に使用されます。 カラーインデックスでは、 CI溶剤染料として指定されています
例:
- CIソルベントイエロー32
- CIソルベントレッド8
反応染料
染色工程において、反応染料は繊維の官能基と共有結合を形成し、高い湿潤堅牢度を持つ染料を生み出します。セルロース繊維に使用される染料の中で最大のグループを構成していますが、ウールやポリアミドの濃い色合いにも使用されます。[ 33 ]
化学的には、反応性染料は2つの成分、すなわち発色団と1つ以上の反応基(反応性アンカーとも呼ばれる)から構成されます。反応性アンカーシステムとしては、主に以下の2つが用いられます。
- いわゆるビニルスルホン類は、染色中に繊維の求核基とマイケル付加反応を起こし、安定なエーテル結合を形成します。多くのビニルスルホン染料では、ビニルスルホン基は硫酸半エステルとして保護された形で存在しています。アルカリ性染色条件下でのみ、硫酸の脱離によってビニルスルホン基が生成されます。
両方のタイプの反応性アンカーが、単一の反応性染料に同時に存在する場合があります。
アゾ染料は、反応染料に使用される最も一般的な発色団です。しかし、アントラキノン、ホルマザン、フタロシアニン染料といった他の発色団系も重要です。反応染料は、カラーインデックスでは「CI反応染料」として分類されています。
例:
- CIリアクティブブルー21
- CIリアクティブレッド227
- CI リアクティブオレンジ 1
酸性染料
酸性染料は、通常はスルホン酸基などのアニオン置換基を含む親水性染料です。ほとんどの酸性染料はアゾ染料に分類されますが、他の発色団も存在します。主にウール、シルク、ポリアミドの染色に使用され、染色はpH2~6の範囲で行われます。小さな染料分子を使用すると、染料分子が繊維のアンモニウム基と主に塩のような結合を形成することで、均一な染色が実現されます。このような染料の洗濯堅牢度は比較的中程度です。分子サイズが大きくなるにつれて、染料分子の疎水性部分と繊維との間の吸着力によって、染料と繊維の結合が強化されます。これにより湿潤堅牢度は向上しますが、染色の均一性は犠牲になることが多いです
酸性染料は、カラーインデックスでは「CI 酸性染料」と表記されます。例:
- CIアシッドブラック1
- CIアシッドイエロー36
- CI アシッドブルー 117
- CIアシッドブルー3(パテントブルーV)
機能性染料
従来の染料は繊維、皮革、紙の外観を改良するために使用されますが、機能性染料は一般的に美観以外の目的に使用されます。代表的な用途としては、指示薬染料や電圧依存性染料などがあります。[ 34 ]
特殊な染料は
- 特定の波長の光を吸収し、それを熱に変換します(例:化学分析や生化学分析)。[ 34 ]
- 吸収した光を異なる波長で再放射する(リン光バイオマーカーやインク、色素レーザーの蛍光、生化学における化学結合の切断や形成における化学発光など) [ 34 ]
- 光の偏光方向を変える(例えば、周波数倍増や光スイッチとして)
- 電気現象を誘発する(例:レーザープリンタアプリケーション)
- 光化学プロセスを可能にします。
レーザー色素は、一部のレーザー、光学メディア(CD-R)、カメラセンサー(カラーフィルターアレイ)の製造に使用されます。[ 35 ]経済的な観点から、機能性色素はCDやDVDの製造において特に重要です。色素分子はディスクのポリカーボネートに埋め込まれています。バーナーのレーザービームは、色素分子に光エネルギーを吸収させて熱に変換し、ポリカーボネートの局所的な溶融を引き起こします。このわずかに変化した表面構造は、読み取りプロセス中に検出されます。[ 36 ]レーザー色素の例としては、ローダミン6Gやクマリン色素があります。[ 37 ]
生体染色剤
「生体染色剤」または染色剤は、生きた細胞や組織に浸透しても、すぐに目に見える変性変化を引き起こすことなく染色できる染料です。[ 38 ]このような染料は、医療および病理学の分野で、特定の構造(細胞など)を選択的に着色し、周囲の組織と区別して研究(例えば顕微鏡下)でより見やすくするために有用です。視認性は細胞や組織の研究を可能にすることを目的としているため、通常、染料が組織の構造や機能に客観的な観察を損なうような影響を与えないことが重要です
研究前に生物から取り出された細胞に使用するための染料 (超生体染色) と、生体内 (注射またはその他の手段で投与) で使用される染料 (生体染色) は区別されます。後者は (たとえば) より高度な安全基準の対象であり、通常、研究対象の組織だけでなく、短期的には (組織から除去されるまで) あらゆる生化学に悪影響を及ぼさないことが知られている化学物質である必要があります。
「生体染色」という用語は、生体内染色および超生体染色と互換的に使用されることがありますが、どちらの場合も、検査対象となる細胞がまだ生きているという概念に基づいています。より厳密な意味では、「生体染色」という用語は「超生体染色」の正反対の意味を持ちます。生細胞が超生体染色中に染色液を吸収した場合、「生体染色」では染色液を排除します。例えば、生細胞は陰性染色され、死細胞のみが陽性染色されるため、陰性染色される細胞の割合を数えることで生存率を判定できます。染色液によって染色液が生体内染色か超生体染色かが決まるため、超生体染色と生体染色液を組み合わせることで、細胞をより正確に様々なグループ(例えば、生細胞、死細胞、死滅細胞)に分類することができます。[ 39 ]
その他の重要な染料
他にも、次のような多くの分類が確立されています
- 革用染料
- 繊維および紙用蛍光増白剤
- 溶剤染料。木材の染色、着色ラッカー、溶剤インク、着色油、ワックスの製造に使用されます。
- 磁気共鳴画像法のために注入される造影剤は、強い常磁性を持つ薬剤と結合していることを除けば、本質的には衣類用染料と同じである。[ 40 ]
- 見た目を良くするために水冷に使われるメイヘムズ染料は、RIT染料としてブランド名が変更されることが多い。
汚染
繊維、印刷、製紙産業で生産される染料は、河川や水路の汚染源となっています。[ 41 ]推定70万トンの染料が年間生産されています(1990年のデータ)。化学的および生物学的手段を用いたこれらの物質の処分には、多くの注目が集まっています。[ 42 ]
染料の分解と処理
染料は環境に放出される前に、より有害性の低い物質に分解するか、放出される水から分離することができます。これにはいくつかの方法があります。
吸着
吸着は、その簡便性、低コスト、そして吸着剤の入手しやすさから、染料除去における最も一般的かつ効果的な方法の一つです。このプロセスでは、染料分子が活性炭、粘土、ゼオライト、農業廃棄物などの固体材料の表面に吸着します。この方法は、強力な化学薬品や高エネルギーを必要とせず、高い染料除去効率を達成できます。ただし、その性能は染料の種類と吸着剤の表面特性に依存し、使用済みの吸着剤は適切な廃棄または再生が必要となる場合もあります。
膜ろ過
膜ろ過は、半透膜を用いて水から染料分子を分離する技術です。限外ろ過、ナノろ過、逆浸透などの技術は、染料をそのサイズと分子量に基づいて除去することができます。これらの方法は高い分離効率を提供し、再利用可能な水を生成できます。しかし、高価で高圧が必要であり、膜ファウリングが発生しやすいため、寿命と性能が低下します
凝集とフロック形成
この方法では、化学凝集剤(ミョウバン、塩化第二鉄)を使用して染料粒子を不安定化し、凝集させてより大きなフロックを形成します。これらのフロックは、沈殿またはろ過によって除去できます。凝集は、廃水処理場の前処理段階として一般的に使用されています。粒子に結合した染料の除去には効果的ですが、可溶性または非常に安定した染料化合物には効果が低く、大量の化学スラッジが発生します
生物学的処理
生物学的方法は、微生物(細菌、真菌、藻類)の活性を利用して染料分子を分解します。これらのプロセスは費用対効果が高く環境に優しいため、大規模な処理に適しています。しかし、多くの合成染料、特にアゾ染料は、その複雑な構造のために微生物による分解に抵抗性があります。生物学的方法は、多くの場合、長い保持時間を必要とし、pH、温度、毒性物質の存在などの操作条件に敏感です。[ 43 ] [ 44 ]
化学酸化
化学酸化では、オゾン(O)、過酸化水素(H2O)、塩素などの強力な酸化剤を使用して、染料分子をより有害性の低い物質に分解します。高度酸化プロセス(AOP)は、有機汚染物質を完全に無機化できる反応性の高いラジカルを生成します。これらの方法は、幅広い染料に対して迅速かつ効果的ですが、コストが高く、二次汚染物質を生成したり、複雑な装置を必要としたりする場合があります
光触媒分解
光触媒分解は、二酸化チタン(TiO)や酸化亜鉛(ZnO)などの半導体触媒の存在下で光エネルギー(通常は紫外線または太陽光)を用いて染料を分解する、持続可能で先進的な方法です。このプロセスでは、ヒドロキシルラジカルなどの活性酸素種(ROS)が生成され、染料分子は水や二酸化炭素などのより小さく、より有害性の低い副産物に分解されます。この方法はクリーンで再利用可能であり、難分解性染料の処理にも効果的であるため、現代の廃水処理戦略に最適です。不均一光触媒は、染料分解へのアプローチの一つです。[ 45 ] [ 46 ]
イオン交換
イオン交換では、合成樹脂材料を用いて水中の染料イオンを無毒のイオンと交換します。この方法は選択的で効率的であり、低濃度の染料溶液に適しています。また、再生して複数回再利用することも可能です。ただし、その容量には限界があり、大きな非イオン性または複雑な染料分子を除去する効果は低くなります
電気化学処理
電気化学処理は、電流を用いて酸化または還元反応を促進し、染料分子を分解します。追加の化学物質を使用せずに実行でき、染料を完全に除去することができます。このプロセスは幅広い染料に効果があり、自動化も可能です。ただし、大量のエネルギーを必要とし、大規模な処理には設備コストが高くなる可能性があります
参照
参考文献
- ^ a b c Booth, Gerald. 「染料、概説」. Ullmann's Encyclopedia of Industrial Chemistry . Weinheim: Wiley-VCH. doi : 10.1002/14356007.a09_073 . ISBN 978-3-527-30673-2。
- ^バージェス、レベッカ(2017年11月8日)。『色の収穫:植物を見つけて天然染料を作る方法』アーティザンブックス。ISBN 9781579654252。
- ^ブリタニカ百科事典の合成染料
- ^カシンガー、ルース(2003年)「染料:貝類から合成染料まで」21世紀ブックスISBN 9780761321125。
- ^ Cañamares, MV; Leona, M. (2008年8月15日). 「表面増強ラマン散乱分光法によるラッカ酸およびその他の天然アントラキノン染料の研究」 . Castillejo, Marta; Moreno, Pablo; Oujja, Mohamed; et al. (eds.).美術作品の保存におけるレーザー:国際会議Lacona VIIの議事録、マドリード、スペイン、2007年9月17日~21日. CRC Press. pp. 29– 33. ISBN 97802038820852017年11月8日閲覧– Googleブックス経由
- ^ Adrosko, Rita J. (1971年11月8日).天然染料と家庭での染色(旧題:米国における天然染料) . Courier Corporation. ISBN 97804862268802017年11月8日閲覧– Googleブックス経由
- ^バルター、マイケル(2009年9月11日)「衣服が人間を作る」サイエンス誌325 ( 5946): 1329. doi : 10.1126/science.325_1329a . PMID 19745126
- ^クヴァヴァゼ、エリソ;バー・ヨセフ、オファー。アンナ・ベルファー・コーエン。ボアレット、エリザベッタ。ジャケリ、ニノ。マツケビッチ、ジノヴィ。メッシュベリアーニ、テンギズ(2009年9月11日)。「3万年前の野生の亜麻の繊維」。科学。325 (5946): 1359。Bibcode : 2009Sci...325.1359K。土井: 10.1126/science.1175404。PMID 19745144。
- ^ Liles, JN (1990). 『天然染色の芸術と工芸』テネシー大学出版局. pp. 2– 4. ISBN 9780870496707。
- ^ 「ジョン・プラー(1803–1878)」。クーリエ&アドバタイザー。2016年6月7日
- ^カール・ヒュブナー (2006 年 8 月)。 「150ジャーレ・モーヴァン」。Chemie in unserer Zeit。40 (4): 274–275 .土井: 10.1002/ciuz.200690054。
- ^トラヴィス、アンソニー・S. (1990). 「パーキンズ・モーブ:有機化学産業の祖先」.テクノロジーと文化. 31 (1): 51– 82. doi : 10.2307/3105760 . JSTOR 3105760 .
- ^アイランド、マレー・リー (1999). 「オリエンタルカーペット産業における合成染料の普及に伴う諸問題」Icon 5 : 138–159 . JSTOR 23786082 .
- ^ハンガー、K.編。 (2003年)。工業用染料: 化学、特性、用途。ワインハイム: ワイリー-VCH。土井:10.1002/3527602011。ISBN 978-3-527-30426-4。
- ^ Zollinger, H. (2003).色彩化学:有機染料と顔料の合成、特性、応用(第3版). Wiley-VCH. ISBN 978-3-906390-23-9。
- ^ a b 1908年証券取引所年鑑
- ^ ICI染料部門と前身会社のClaus & Co.のアーカイブ。マンチェスター大学図書館所蔵
- ^バロウズ、アンディ、ホルマン、ジョン、パーソンズ、グウェン、プライス、ガレス (2009). 『化学3:無機化学、有機化学、物理化学入門』オックスフォード大学出版局. pp. 1005– 1006. ISBN 978-0-19-927789-6。
- ^クラウス・ハンガー編 (2003) [ [1] Googleブックス工業用染料:化学、特性、応用]、ヴァインハイム:WILEY-VCH Verlag、ISBN 978-3-662-01950-4
{{citation}}:値を確認する|url=(ヘルプ) - ^スタインルーバー、エルマー。 「インディゴとインディゴ色素」。ウルマンの工業化学百科事典。ワインハイム: ワイリー-VCH。土井: 10.1002/14356007.a14_149.pub2。ISBN 978-3-527-30673-2。
- ^シアニン色素に関する記事。Römpp Online。Georg Thieme Verlag、{{{Datum}}}より取得テンプレートのエラー * 不明なパラメーター名 (テンプレート:RömppOnline ): "Abruf"
- ^ Triarylmethan-Farbstoffに関するエントリ。ロンプオンラインで。 Georg Thieme Verlag、{{{データ}}} を取得しました。テンプレートのエラー * 不明なパラメーター名 (テンプレート:RömppOnline ): "Abruf"
- ^ a b Heinrich Zollinger (2003)、[ [2] Google Books Color Chemistry: Syntheses, Properties, and Applications of Organic Dyes and Pigments ] (3. ed.)、Weinheim: WILEY-VCH Verlag、ISBN 3-906390-23-3
{{citation}}:値を確認する|url=(ヘルプ) - ^ Schwefel-Farbstoffeに関する記事。Römpp Online。Georg Thieme Verlag、{{{Datum}}} 取得テンプレートのエラー * 不明なパラメーター名 (テンプレート:RömppOnline ): "Abruf"
- ^カーク・オスマー、ジャクリーン・I・クロシュヴィッツ著:化学技術百科事典。5 . Ausgabe、第9巻、2005年、ISBN 978-0-471-48494-3、S. 349。
- ^ポール・リス、ハインリヒ・ツォリンガー: Leitfaden der Farbstoffchemie. 2. Auflage、Verlag Chemie、ワインハイム、1976、ISBN 3-527-25650-4、S. 181、182。
- ^ Chromierungsfarbstoffeのエントリ。ロンプオンラインで。 Georg Thieme Verlag、{{{データ}}} を取得しました。テンプレートのエラー * 不明なパラメーター名 (テンプレート:RömppOnline ): "Abruf"
- ^ジェイコブ・ハーツフェルド (1900)、[ [3]、p. 55、Google Books Die Bleichmittel、Beizen und Farbstoffe ] (Eigenschaften、Prüfung und praktische Anwendung auf Baumwolle、Wolle、Seide、Halbwolle、Halbseide、Jute、Leinen など) (2 版)、Unikum Verlag、 55–96ページ
{{citation}}:値を確認する|url=(ヘルプ) - ^ヴィットコ・フランケ、ヴォルフガング・ヴァルター: Lehrbuch der Organischen Chemie. S. Hirzel Verlag、シュトゥットガルト、2004 年、ISBN 3-7776-1221-9、S. 684 f。
- ^ “Verordnung (EG) Nr. 1333/2008 2008 年 12 月 16 日 über Lebensmittelzusatzstoffe”。、2019年8月5日閲覧。
- ^ “Zulassung und Verwendung von Lebensmittelzusatzstoffen” . Ernährung und Landwirtschaft 連邦大臣。2019年8月5日に取得。
- ^ Rodriguez-Amaya, Delia B (2016年2月). 「天然食品色素と着色料」. Current Opinion in Food Science . 7 : 20–26 . doi : 10.1016/j.cofs.2015.08.004 .
- ^ H. ゾリンジャー: Chemismus der Reaktivfarbstoffe。で:アンジェウ。化学。 73、Nr. 4、1961、S. 125–136、 doi:10.1002/ange.19610730402。
- ^ a b cジョン・グリフィス: Funktionelle Farbstoff. Ein neuer Farbstoffchemie のトレンド。で: Chemie in unserer Zeit。 27、Nr. 1、1993、S. 21–31、doi:10.1002/ciuz.19930270104。
- ^シルヴァスト、ウィリアム・T.(2008年7月21日)『レーザーの基礎』ケンブリッジ大学出版局、ISBN 97811398555702017年11月8日閲覧– Googleブックス経由
- ^ Klaus Roth: Die Chemie der schillernden Scheiben: CD, DVD & Co. In: Chemie in unserer Zeit. 41、Nr. 4、2007、S. 334–345、 doi:10.1002/ciuz.200700428。
- ^ Duarte, FJ ; Hillman, LW編 (1990).色素レーザーの原理. ニューヨーク.
{{cite book}}: CS1 メンテナンス: 場所の発行元が見つかりません (リンク) - ^ 「VITAL DYEの医学的定義」 www.merriam-webster.com . 2024年10月24日閲覧。
- ^ Ionescu, Sinziana (2023-07-26). 「大腸手術におけるインドシアニングリーンの使用」.大腸手術の最新トピック. IntechOpen. doi : 10.5772/intechopen.100301 . ISBN 978-1-83962-335-6。
 この記事には、CC BY 3.0ライセンスの下で利用可能なテキストが含まれています
この記事には、CC BY 3.0ライセンスの下で利用可能なテキストが含まれています - ^ "patentstorm.us" . Patentstorm.us . 2011年6月12日時点のオリジナルよりアーカイブ。 2017年11月8日閲覧。
- ^ Brindley, Lewis (2009年7月). 「染料廃水汚染に対する新たな解決策」 . Chemistry World . 2018年7月8日閲覧。
- ^ Xu, Xiang-Rong; Li, Hua-Bin; Wang, Wen-Hua; Gu, Ji-Dong (2004). 「フェントン法による水溶液中の染料の分解」 . Chemosphere . 57 (7): 595– 600. Bibcode : 2004Chmsp..57..595X . doi : 10.1016/j.chemosphere.2004.07.030 . PMID 15488921 .
- ^ Lin, Jiuyang; Ye, Wenyuan; Xie, Ming; Seo, Dong Han; Luo, Jianquan; Wan, Yinhua; Van der Bruggen, Bart (2023年10月26日). 「染料含有廃水の環境影響と修復」 . Nature Reviews Earth & Environment . 4 (11): 785– 803. doi : 10.1038/s43017-023-00489-8 . ISSN 2662-138X .
- ^ Anandita; Raees, Kashif; Shahadat, Mohammad; Ali, Syed Wazed (2023-09-06). 「染料分解における微生物のメカニズム的相互作用と本質的に改変された生物の役割:レビュー」 . Water Conservation Science and Engineering . 8 (1): 43. doi : 10.1007/s41101-023-00219-7 . ISSN 2364-5687 .
- ^ Pandit, VK; Arbuj, SS; Pandit, YB; Naik, SD; Rane, SB; Mulik, UP; Gosavic, SW; Kale, BB「新規有機–無機(6,13-ペンタセンキノン/TiO 2)ナノ複合体を用いた太陽光駆動型染料分解」。RSC Adv. 2015, 5, 10326-10331。
- ^ Khan, Sadia; Noor, Tayyaba; Iqbal, Naseem; Yaqoob, Lubna (2024-05-21). 「繊維廃水からの光触媒染料分解:レビュー」 . ACS Omega . 9 (20): 21751– 21767. doi : 10.1021/acsomega.4c00887 . PMC 11112581. PMID 38799325 .
さらに読む
- アベルスハウザー、ヴェルナー著『ドイツの歴史とグローバル企業:BASF:企業の歴史』(2004年)は1865年から2000年までを網羅している。
- ビア、ジョン・J. 『ドイツ染料産業の出現』(1959年)












![フタロシアニン(アザ[18]アヌレン)](http://upload.wikimedia.org/wikipedia/commons/thumb/3/3f/Phtalocyanine_Aza%2818%29annulene.svg/250px-Phtalocyanine_Aza%2818%29annulene.svg.png)